Os anticoagulantes são fármacos que atrasam ou interrompem a cascata de coagulação. As principais classes de anticoagulantes disponíveis incluem as heparinas, os antagonistas dependentes da vitamina K (por exemplo, varfarina), os inibidores diretos da trombina e os inibidores do fator Xa. Os anticoagulantes são usados no tratamento e prevenção de doenças trombóticas e embólicas, incluindo o acidente vascular cerebral isquémico cardioembólico, a síndrome coronária aguda e o tromboembolismo venoso, entre outras condições. Os doentes com fibrilhação auricular ou trombofilias podem necessitar de anticoagulação por tempo indefinido ou vitalícia. Assim, tanto a via de administração, como as interações medicamentosas, a farmacocinética e a disponibilidade dos fatores de reversão devem ser considerados ao selecionar uma terapêutica anticoagulante.
Última atualização: Jan 17, 2024
Os anticoagulantes são uma categoria de fármacos que inibem a cascata de coagulação.
Os anticoagulantes estão indicados para o tratamento e profilaxia de eventos trombóticos, incluindo:
Existem várias classes primárias de anticoagulantes:
A cascata de coagulação consiste numa série de reações que culminam num forte coágulo de fibrina com ligações cruzadas. Esta cascata é também conhecida como hemostase secundária.
Fatores de coagulação :
Diversos fatores de coagulação sofrem uma ativação sequencial ao longo de 1 de 2 vias:
Via comum:
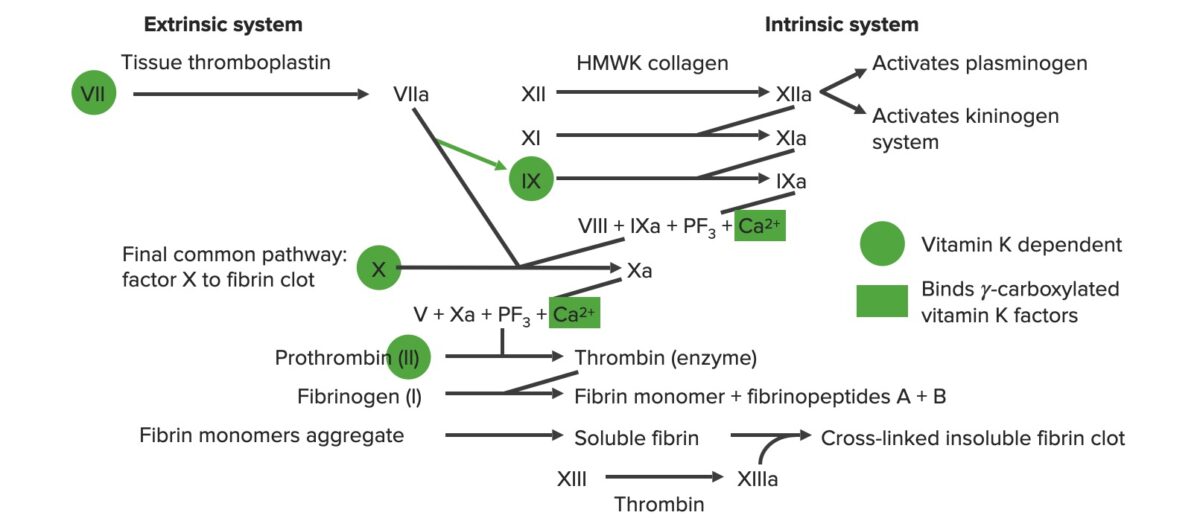
Visão geral da cascata de coagulação
a: forma ativa
PF3 : fator plaquetário 3 (fosfolípidos)
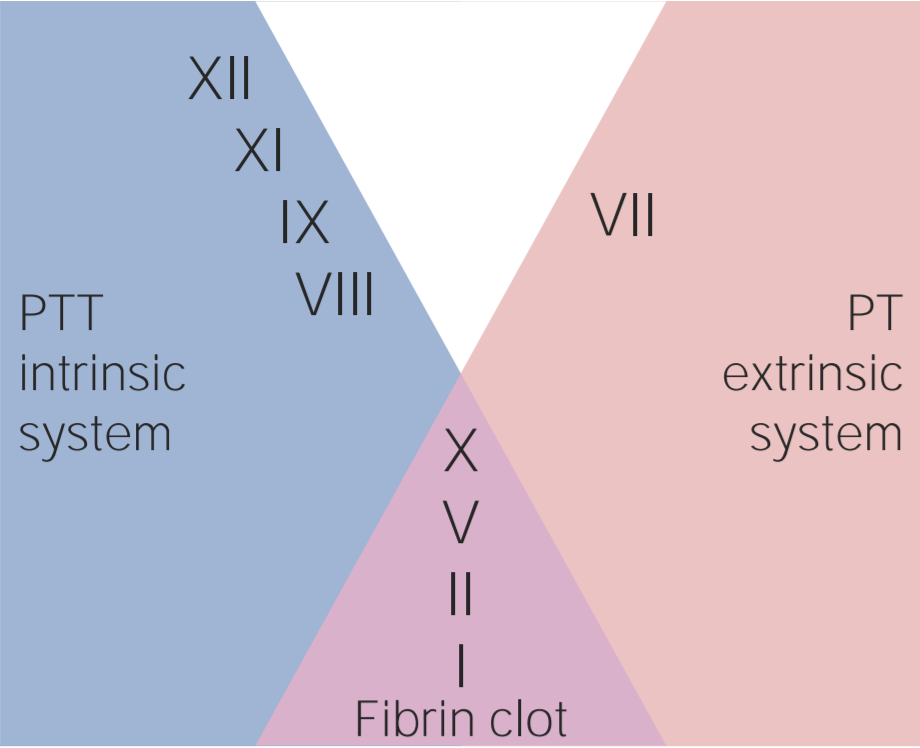
Fatores envolvidos nas vias intrínseca, extrínseca e comum
Imagem de Lecturio.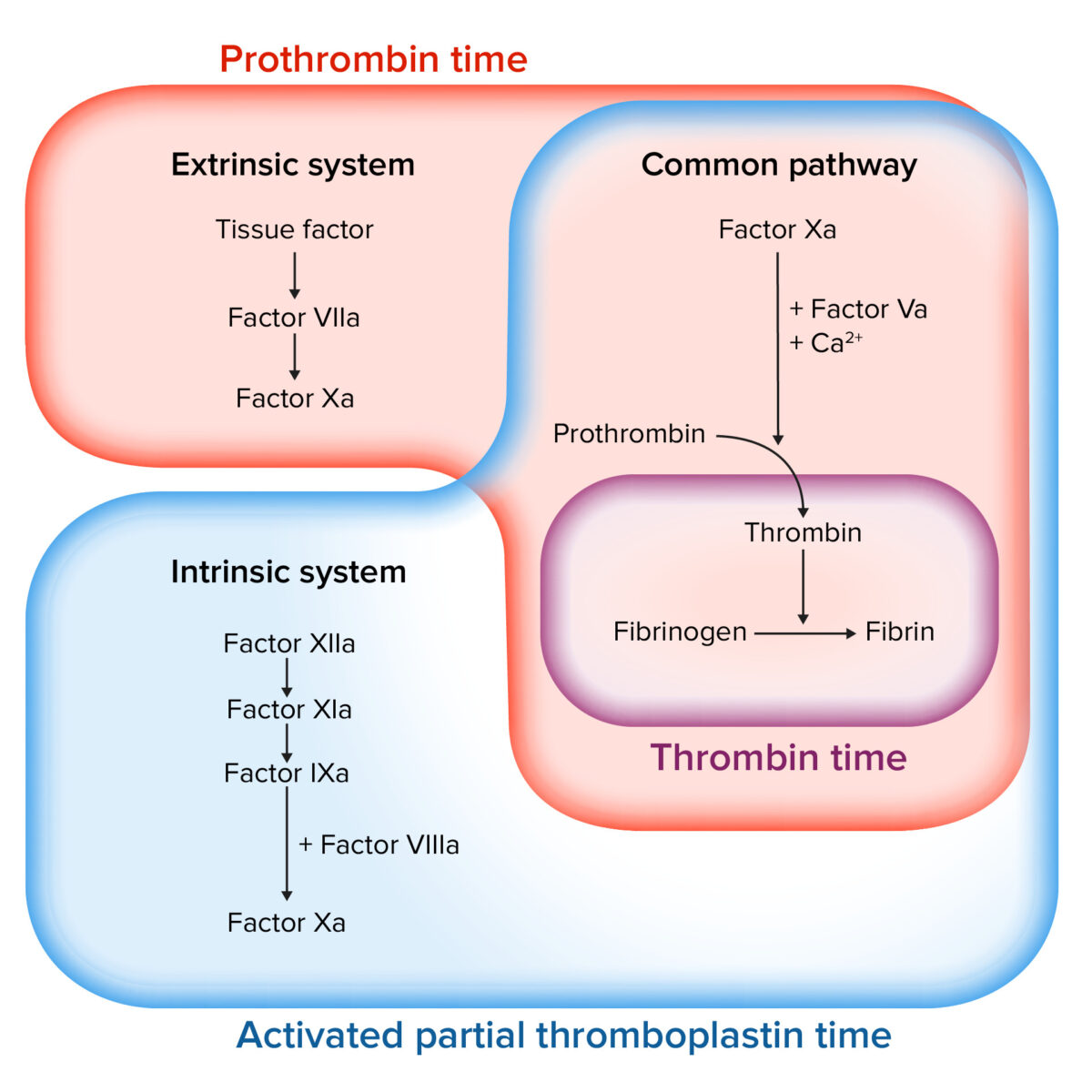
Avaliação da cascata de coagulação
Imagem de Lecturio.As heparinas naturais são um grupo de polissacarídeos grandes, de produção endógena e de tamanhos variados que não são completamente compreendidos. As heparinas têm efeitos anticoagulantes, anti-inflamatórios e possivelmente antiangiogénicos.
| HNF | HBPM | |
|---|---|---|
| Agentes | HNF |
|
| Mecanismo de ação |
Liga-se e potencia a antitrombina
|
|
| Efeitos fisiológicos | Inativação do Fator Xa e da trombina | Inativação do fator Xa e, num grau bastante menor, da trombina |
| Absorção |
Administrada IV (raramente SC):
|
|
| Distribuição | V d = ~ 35 mL/kg | V d = 4,3 L |
| Metabolismo |
|
Fígado |
| Eliminação |
|
|
| Monitorização |
|
|
| Agente de reversão | Sulfato de protamina | Sulfato de protamina |
| Complicações |
|
Menor risco de HITT e de osteoporose do que com a HNF |
| Contraindicações específicas |
|
|
| Notas |
|
|
| Mecanismo de ação |
|
|---|---|
| Absorção |
|
| Metabolismo |
Metabolizada no fígado:
|
| Distribuição |
|
| Eliminação |
|
| Monitorização |
|
| Agente de reversão/antídoto | Vitamina K (leva várias horas a ter efeito) |
| Interações | A varfarina tem inúmeras interações medicamentosas, fitoterápicas e dietéticas:
|
| Contraindicações específicas | Gravidez (a varfarina é teratogénica) |
| Complicações |
|
| Notas | Os doentes com variantes da CYP2C9 têm ↓ atividade enzimática → requerem ↓ dose |
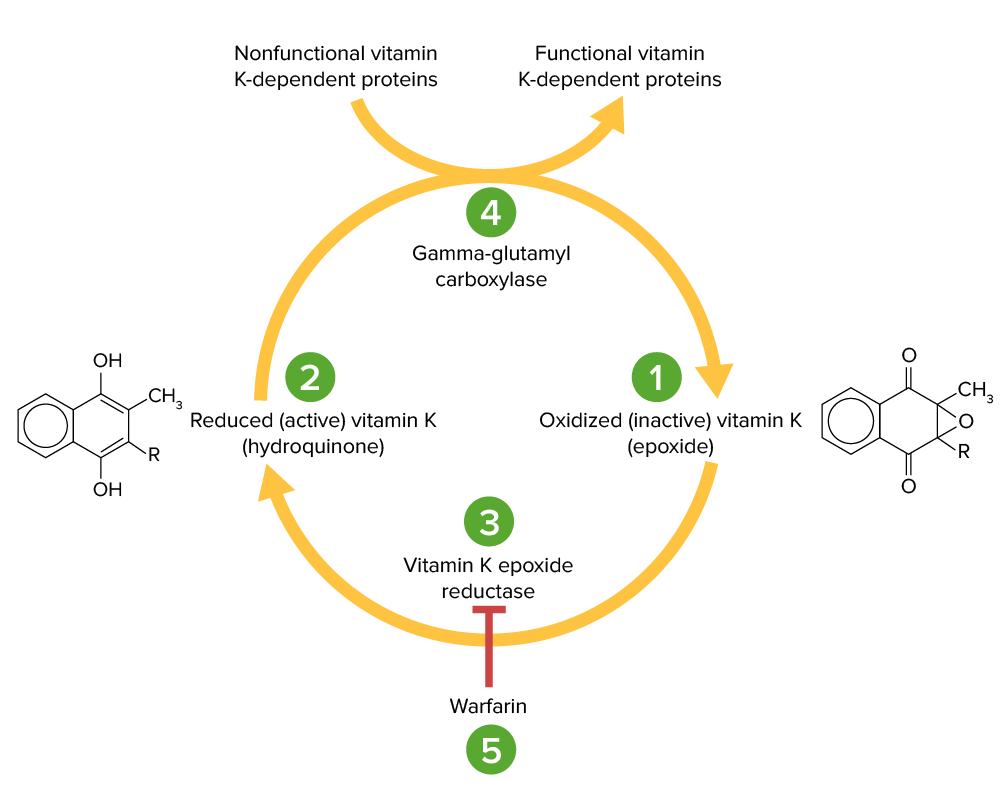
Ciclo da vitamina K:
O epóxido de vitamina K (1) é inativo e convertido na sua forma ativa e reduzida, a vitamina K hidroquinona (2), pela vitamina K epóxido redutase (VKOR; 3). A vitamina K hidroquinona é um cofator na carboxilação de resíduos específicos de glutamato nas proteínas dependentes da vitamina K (fatores II, VII, IX, X, proteína C e S), um processo necessário para as ativar. A reação de carboxilação é catalisada pela gama-glutamil carboxilase (4). A vitamina K hidroquinona é oxidada para a forma de epóxido quando atua como cofator, mas é depois reciclada de novo para a forma de hidroquinona pela VKOR. A varfarina inibe a VKOR (5), de modo que a vitamina K não pode ser reciclada da sua forma oxidada para a forma reduzida. Assim, as proteínas dependentes da vitamina K não podem ser ativadas.
| Agentes orais (DOAC) | Agentes parentéricos | |
|---|---|---|
| Agentes | Dabigatrano (Pradaxa®) |
|
| Mecanismo de ação | Liga-se e inibe funcionalmente a trombina tanto no soro como nos coágulos | |
| Absorção |
|
Início de ação: imediato |
| Distribuição |
|
Bivalirudina:
|
| Metabolismo | Fígado |
|
| Eliminação |
|
|
| Monitorização | aPTT | TCA |
| Antídoto | Idarucizumab (Praxbind®) | Nenhum |
| Contraindicações específicas | Nenhuma (além das contraindicações gerais listadas acima) | |
| Notas | Frequentemente utilizado como alternativa nos doentes com história de HITT | |
| Inibidores diretos do fator Xa (DOACs) | Inibidores indiretos do fator Xa | |
|---|---|---|
| Agentes |
|
|
| Mecanismo de ação | Ligam-se diretamente e inibem o fator Xa |
|
| Absorção |
|
|
| Distribuição |
Rivaroxabano:
|
|
| Metabolismo | Metabolizados principalmente no fígado pela CYP3A4 | Eliminados inalterados |
| Eliminação |
|
|
| Monitorização |
|
|
| Antídoto | Andexanet alfa | Nenhum |
| Contraindicações específicas | Nenhuma (além das contraindicações gerais listadas acima) | Trombocitopenia associada a um teste de anticorpos antiplaquetários positivo |
| Notas | Pentassacarídeo sintético com um local funcional semelhante à heparina. |
Fatores a ter em conta antes de reverter um anticoagulante:
| Fármaco | Tempo antes do procedimento para suspensão do anticoagulante |
|---|---|
| Varfarina | 5 dias |
| Heparina | 4 horas |
| HBPM |
|
| DOACs: Dabigatrano, rivaroxabano, apixabano, edoxabano |
|
| Fármaco | Agente de reversão |
|---|---|
| Varfarina |
|
| Heparina e HBPMs | Sulfato de protamina |
| Dabigatrano | Idarucizumab (Praxbind®) |
| Argatroban, bivalirudina | Nenhum |
| Apixabano, rivaroxabano | Andexanet alfa |
| Fondaparinux | Nenhum, considerar fator VII recombinante ativado |
Alguma das aplicações terapêuticas mais comuns dos anticoagulantes incluem: