Los anticoagulantes son medicamentos que retardan o interrumpen la cascada de la coagulación. Las principales clases de anticoagulantes disponibles incluyen heparinas, antagonistas dependientes de la vitamina K (e.g., warfarina), inhibidores directos de la trombina e inhibidores del factor Xa. Los anticoagulantes se utilizan en el tratamiento y prevención de enfermedades trombóticas y embólicas, incluido el accidente cerebrovascular isquémico cardioembólico, el síndrome coronario agudo y el tromboembolismo venoso, entre otras afecciones. Los pacientes con fibrilación auricular o trombofilias pueden requerir anticoagulación indefinida o de por vida. En consecuencia, se debe considerar la vía de administración, las interacciones con otros medicamentos, la farmacocinética y la disponibilidad de agentes de reversión al seleccionar la terapia anticoagulante.
Última actualización: Ene 17, 2024
Los anticoagulantes son una categoría de medicamentos que inhiben la cascada de la coagulación.
Los anticoagulantes están indicados en el tratamiento y profilaxis de eventos trombóticos que incluyen:
Existen varias clases de anticoagulantes principales:
La cascada de coagulación es una serie de reacciones que finalmente genera un fuerte coágulo reticulado de fibrina. Esta cascada también se conoce como hemostasia secundaria.
Factores de coagulación:
Varios factores de la coagulación se activan secuencialmente por 1 de 2 vías:
Vía común:
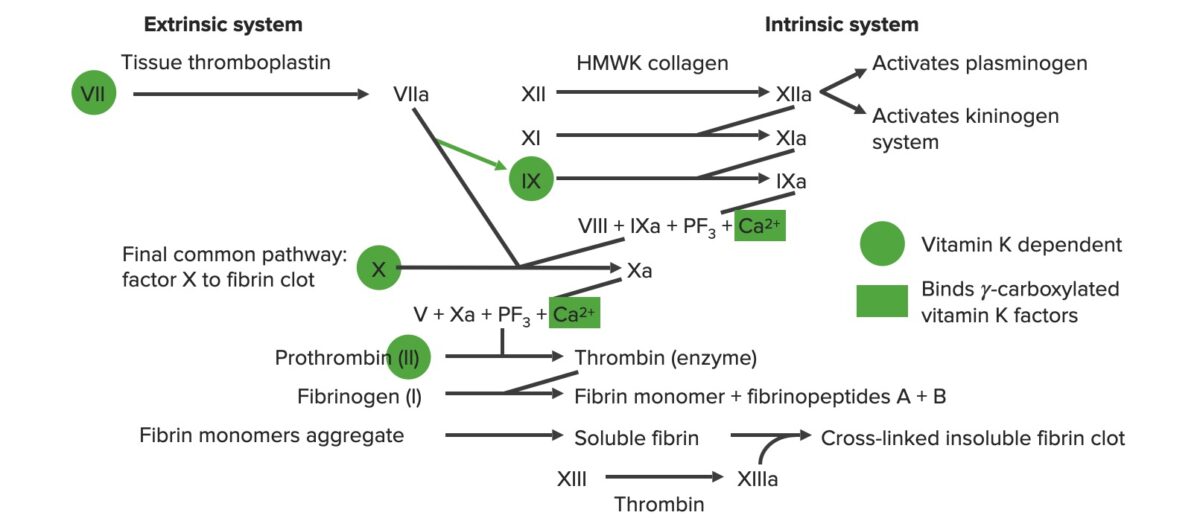
Resumen de la cascada de la coagulación
a: forma activada
PF3: factor plaquetario 3 (fosfolípidos)
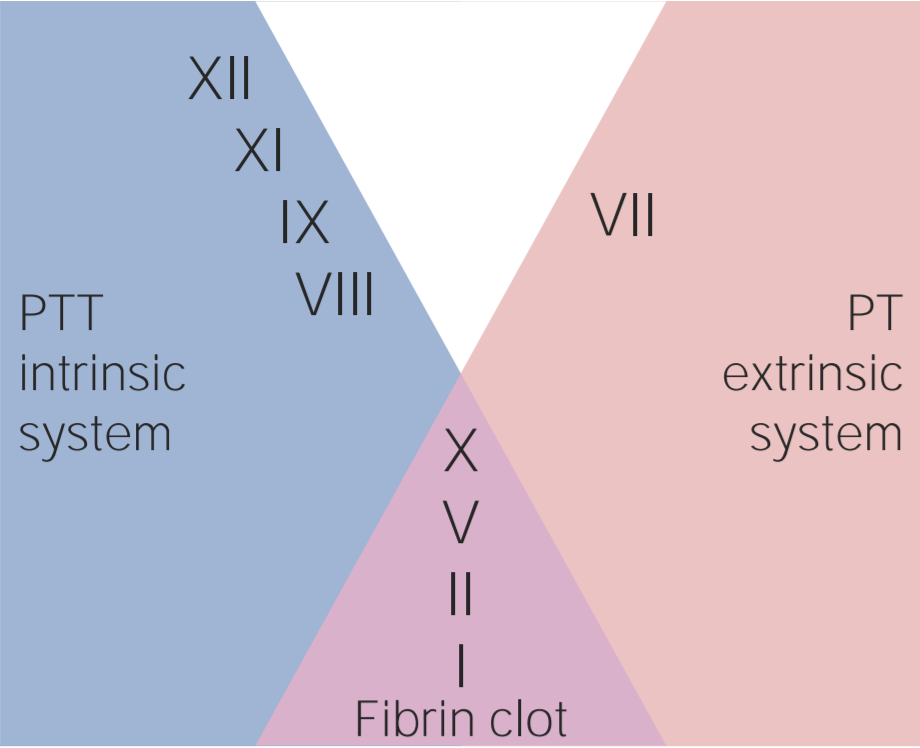
Factores involucrados en las vías intrínseca, extrínseca y común
Imagen por Lecturio.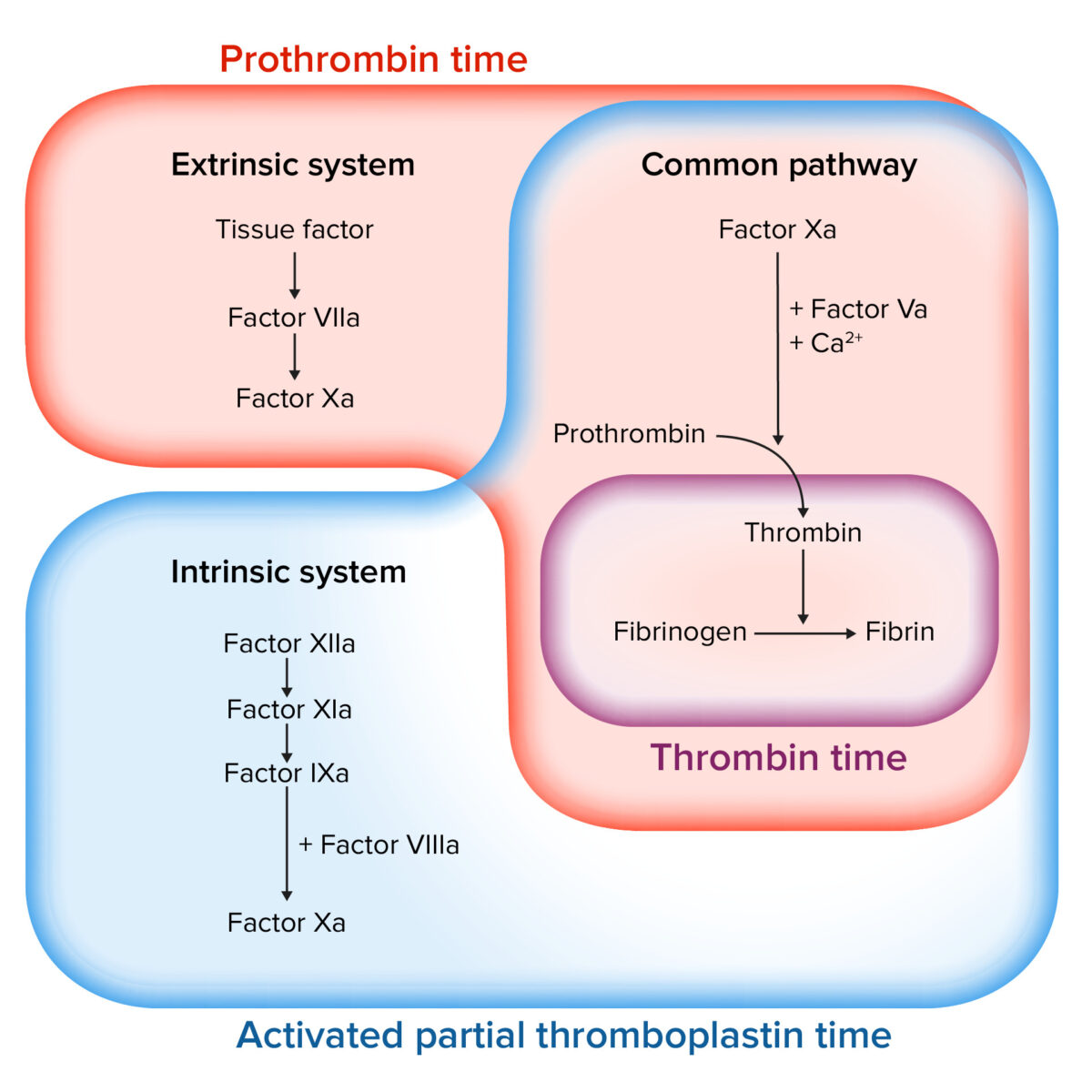
Estudio de la cascada de la coagulación
Imagen por Lecturio.Las heparinas naturales son un grande grupo de polisacáridos producidos endógenamente de diferentes tamaños que no se conocen por completo. Las heparinas tienen efectos anticoagulantes, antiinflamatorios y posiblemente antiangiogénicos.
| HNF | HBPM | |
|---|---|---|
| Medicamentos | HNF |
|
| Mecanismo de acción |
Se une y potencializa a la antitrombina
|
|
| Efectos fisiológicos | Inactivación del Factor Xa y la trombina | Inactivación del Factor Xa y, en mucha menor medida, de la trombina |
| Absorción |
Administrada por vía intravenosa (raramente subcutánea):
|
|
| Distribución | Vd = ~ 35 mL/kg | Vd = 4,3 L |
| Metabolismo |
|
Hepático |
| Eliminación |
|
|
| Monitoreo |
|
|
| Agente reversible | Sulfato de protamina | Sulfato de protamina |
| Complicaciones |
|
Menores riesgos de TTIH y osteoporosis que HNF |
| Contraindicaciones específicas |
|
|
| Nota |
|
|
| Mecanismo de acción |
|
|---|---|
| Absorción |
|
| Metabolismo |
Metabolismo hepático:
|
| Distribución |
|
| Eliminación |
|
| Monitoreo |
|
| Agente de reversión/antídoto | Vitamina K (tarda varias horas en hacer efecto) |
| Interacciones | La warfarina tiene numerosas interacciones medicamentosas, herbales y dietéticas:
|
| Contraindicaciones específicas | Embarazo (la warfarina es teratogénica) |
| Complicaciones |
|
| Notas | Los pacientes con variantes del CYP2C9 tienen una ↓ actividad enzimática → requieren ↓ dosis |
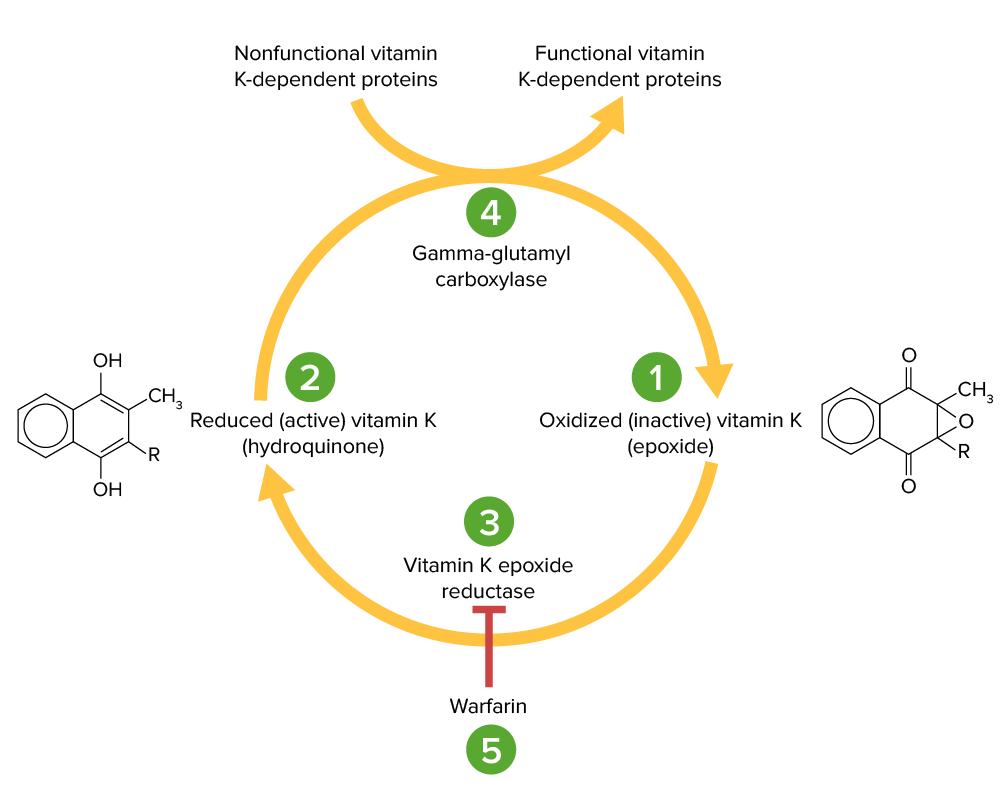
Ciclo de la vitamina K:
La vitamina K epóxido (1) es inactiva y se convierte en su forma activa reducida, la vitamina K hidroquinona (2), mediante la vitamina K epóxido reductasa (VKOR; 3). La vitamina K hidroquinona es un cofactor en la carboxilación de residuos de glutamato específicos dentro de las proteínas dependientes de la vitamina K (factores II, VII, IX, X, proteína C y S), un proceso que es necesario para activarlas. La reacción de carboxilación es catalizada por la gamma-glutamil carboxilasa (4). La vitamina K hidroquinona se oxida a la forma epóxido cuando actúa como cofactor, pero luego es reciclada de nuevo a la forma hidroquinona por el VKOR. La warfarina inhibe el VKOR (5), de modo que la vitamina K no puede reciclarse de su forma oxidada a la reducida. Así, las proteínas dependientes de la vitamina K no pueden activarse.
Imagen por Lecturio.| Medicamentos orales (ACOD) | Medicamentos parenterales | |
|---|---|---|
| Medicamentos | Dabigatrán (Pradaxa®) |
|
| Mecanismo de acción | Se unen a la trombina y la inhiben funcionalmente tanto en el suero como en los coágulos | |
| Absorción |
|
Inicio de acción: inmediato |
| Distribución |
|
Bivalirudina:
|
| Metabolismo | Hepático |
|
| Eliminación |
|
|
| Monitoreo | TTPa | ACT |
| Antídoto | Idarucizumab (Praxbind®) | Ninguno |
| Contraindicaciones específicas | Ninguna (más allá de las contraindicaciones generales enumeradas anteriormente) | |
| Nota | A menudo se utilizan como alternativa en pacientes con antecedentes de TTIH | |
| Inhibidores directos del factor Xa (ACOD) | Inhibidores indirectos del factor Xa | |
|---|---|---|
| Medicamentos |
|
|
| Mecanismo de acción | Se unen directamente e inhiben el factor Xa |
|
| Absorción |
|
|
| Distribución |
Rivaroxabán:
|
|
| Metabolismo | Principalmente hepático por el CYP3A4 | Eliminado sin cambios |
| Eliminación |
|
|
| Monitoreo |
|
|
| Antídoto | Andexanet alfa | Ninguno |
| Contraindicaciones específicas | Ninguna (más allá de las contraindicaciones generales enumeradas anteriormente) | Trombocitopenia asociada con una prueba de anticuerpos antiplaquetarios positiva |
| Nota | Un pentasacárido sintético con un sitio funcional similar a la heparina |
Factores a considerar antes de revertir un anticoagulante:
| Medicamento | Tiempo previo al procedimiento por el cual se debe suspender el medicamento |
|---|---|
| Warfarina | 5 días |
| Heparina | 4 horas |
| HBPM |
|
| ACOD: dabigatrán, rivaroxabán, apixabán, edoxabán |
|
| Medicamento | Agente para la reversión |
|---|---|
| Warfarina |
|
| Heparina y HBPM | Sulfato de protamina |
| Dabigatrán | Idarucizumab (Praxbind®) |
| Argatrobán, bivalirudina | Ninguno |
| Apixabán, Rivaroxabán | Andexanet alfa |
| Fondaparinux | Ninguno, considerar factor VII activado recombinante |
Algunos de los usos terapéuticos más comunes de los anticoagulantes incluyen: