A trombocitemia essencial (TE) é um tipo de neoplasia mieloproliferativa caracterizada por trombocitose clonal ligada a mutações somáticas que envolvem a Janus quinase 2 (JAK2), a calreticulina (CALR) e o oncogene do vírus da leucemia mieloproliferativa (MPL). Os doentes podem ser assintomáticos ou apresentar sintomas vasomotores, como cefaleias, eritromelalgia e distúrbios visuais transitórios. O curso clínico pode ser complicado por eventos trombo-hemorrágicos, bem como pela progressão para mielofibrose e LMA. O diagnóstico é baseado em achados laboratoriais de trombocitose, biópsia de medula óssea e estudos genéticos. O tratamento visa reduzir a contagem de plaquetas usando agentes citorredutores (hidroxiureia) e diminuir os episódios de trombose com aspirina e anticoagulação sistémica com base na estratificação do risco de trombose.
Última atualização: Jun 14, 2022
A trombocitemia essencial (TE) é uma neoplasia mieloproliferativa crónica caracterizada pela produção excessiva de plaquetas e um aumento da tendência trombótica e hemorrágica. Outros nomes são trombocitose essencial e trombocitose primária.
A hematopoiese começa com uma célula estaminal hematopoiética, que é estimulada a dividir-se e diferenciar por estímulos químicos apropriados (fatores de crescimento hematopoiético).
Produção de plaquetas:
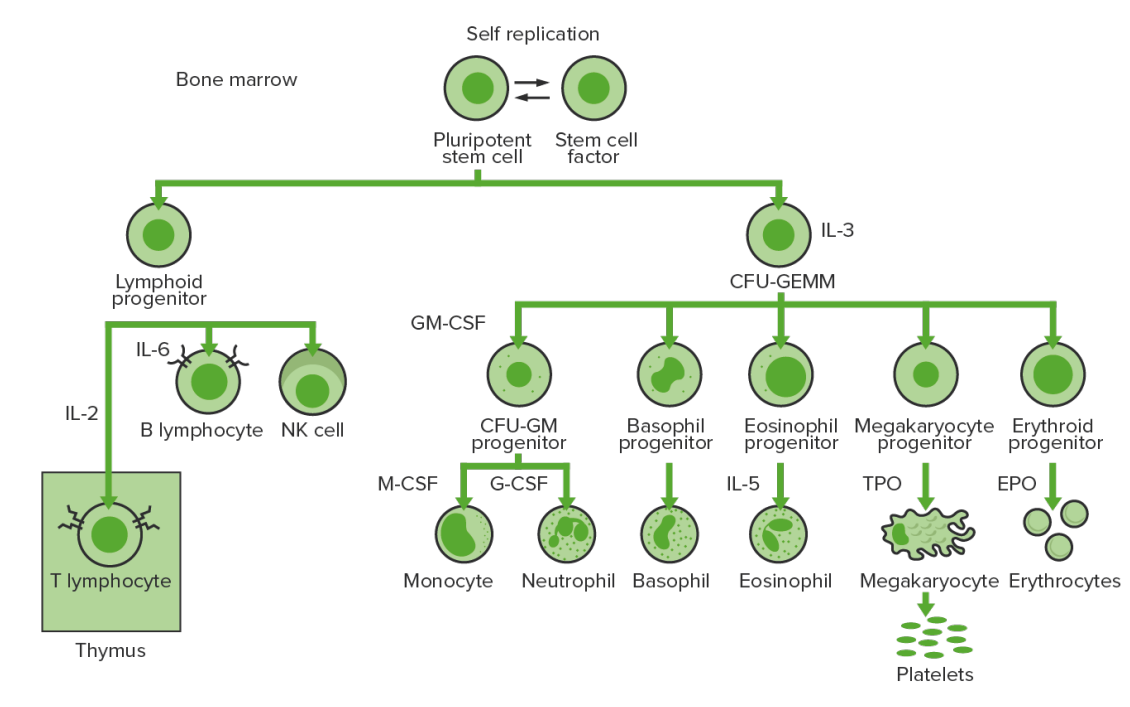
Hematopoiese na medula óssea: proliferação e diferenciação dos elementos sanguíneos.
CFU-GEMM, pela sigla em inglês: unidade formadora de colónias de granulócitos, eritrócitos, monócitos, megacariócitos
CFU-GM, pela sigla em inglês: unidade formadora de colónias de granulócitos-macrófagos
GM-CSF, pela sigla em inglês: fator estimulador de colónias de granulócitos-macrófagos
M-CSF, pela sigla em inglês: fator estimulador de colónias de macrófagos
G-CSF, pela sigla em inglês: fator estimulador de colónias de granulócitos
NK: “natural killer”
TPO: trombopoietina
Aumento da incidência devido a:
O aumento da diátese hemorrágica na TE é devido a:
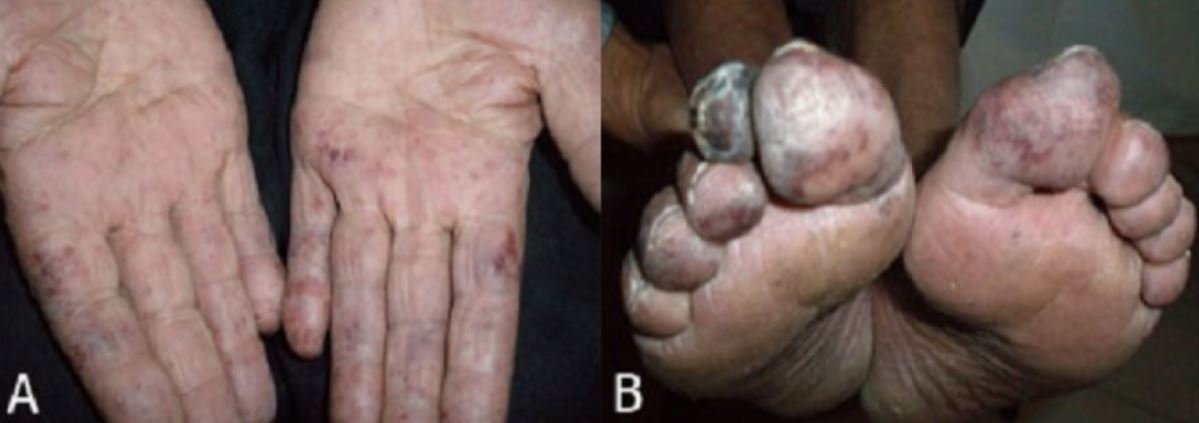
Achados físicos da trombocitemia essencial:
Livedo reticular, áreas de isquemia azulada e mosqueada dos dedos (A) e gangrena do dedo do pé (B)
O diagnóstico requer todos os 4 critérios major ou os 3 primeiros critérios major e 1 critério minor.
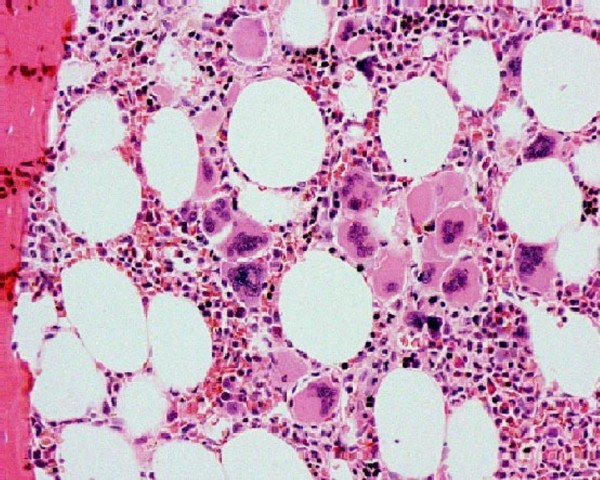
Biópsia da medula óssea na trombocitemia essencial:
Podem ser observados megacariócitos aumentados.
As neoplasias mieloproliferativas podem ser comparadas com a seguinte classificação da OMS:
| Doença | Mutações | Pontos chave |
|---|---|---|
| LMC | BCR-ABL1 (cromossoma Filadélfia) | Proliferação de granulócitos maduros e em maturação |
| TE | JAK2, CALR ou MPL | Produção clonal excessiva de plaquetas |
| Policitemia vera (PV) | JAK2 | Aumento da massa de hemácias |
| Mielofibrose primária (MFP) | JAK2, CALR ou MPL | Fibrose obliteradora da medula óssea |
Outros tipos:
| Risco de trombose | Características | Tratamento |
|---|---|---|
| Risco muito baixo |
|
|
| Baixo risco |
|
|
| Risco intermediário |
|
|
| Risco alto |
|
|