A síndrome de Cushing ou hipercortisolismo é um distúrbio que cursa com características resultantes da exposição crónica ao excesso de glicocorticoides. A síndrome de Cushing pode ser exógena, devido à ingestão crónica de glicocorticoides, ou endógena, devido ao aumento da secreção adrenal de cortisol ou da produção de hormona adrenocorticotrófica (ACTH, pela sigla em inglês) pela glândula pituitária ou por fontes ectópicas. O hipercortisolismo exógeno ou iatrogénico é a causa mais comum. As características clínicas típicas do hipercortisolismo incluem obesidade central, pele fina e friável, estrias abdominais, hipertensão secundária, hiperglicemia e fraqueza muscular proximal. A abordagem diagnóstica inicial é estabelecer o hipercortisolismo através de testes de cortisol urinário e salivar assim como com o teste de supressão de dexametasona em baixa dose. Assim que os níveis elevados de cortisol são confirmados, a etiologia é determinada com base nos níveis de ACTH, nos testes bioquímicos confirmatórios e em estudos de imagem subsequentes. As opções de tratamento dependem da causa e incluem cirurgia e terapêutica médica.
Última atualização: Jun 13, 2022
A síndrome de Cushing ou hipercortisolismo é um distúrbio que cursa com características resultantes da exposição crónica ao excesso de glicocorticoides.
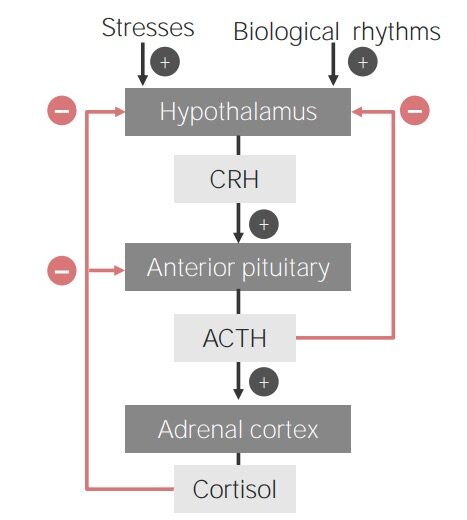
Fluxograma a demonstrar o eixo hipotálamo-hipófise-adrenal
Imagem por Lecturio.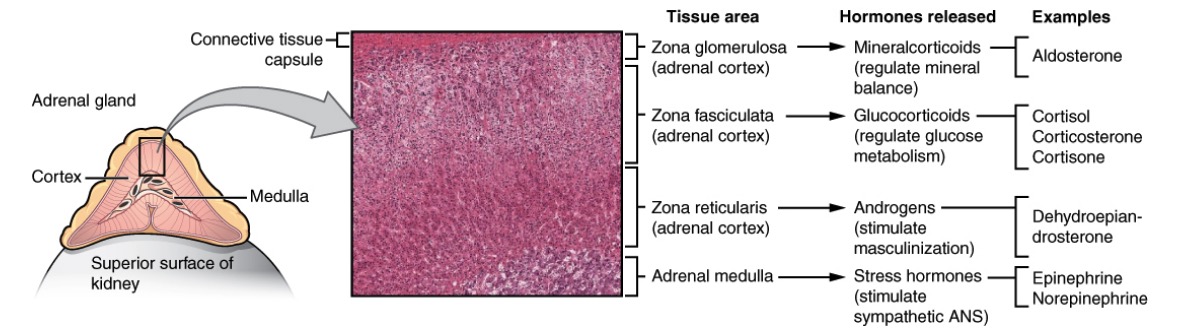
Anatomia, histologia e fisiologia de diferentes zonas da glândula suprarrenal:
O córtex tem a zona glomerulosa que produz mineralocorticoides (“sal”), a zona fasciculada que produz glicocorticoides (“açúcar”) e a zona reticular que produz androgénios (“hormonas sexuais”). A medula suprarrenal produz epinefrina e norepinefrina (“stress”).
| Pele |
|
|---|---|
| Gordura Corporal | Face em lua cheia, obesidade central, pescoço de búfalo (almofada de gordura dorsocervical) |
| Osso | Baixa estatura (diminuição do crescimento linear em crianças), osteopenia, osteoporose, ↑ risco de necrose avascular |
| Músculo | Miopatia proximal, fraqueza |
| Metabolismo | Glicose elevada/diabetes, dislipidemia |
| Sistema Reprodutor | Amenorreia em mulheres, diminuição da libido |
| Sistema Cardiovascul | Aterosclerose, hipertensão, edema |
| Sistema GI | Úlceras |
| Neuropsiquiátricos | Irritabilidade, depressão, labilidade emocional, distúrbios do sono, psicose |
| Sistema oftalmológico | Cataratas (os esteroides afetam a transcrição génica das células epiteliais do cristalino) |
| Sistema imunológico | Aumento da contagem de leucócitos, aumento da suscetibilidade à infeção |
Para recordar as características clínicas mais comuns da síndrome de Cushing, lembrar de “CUSHINGOID” (Cushingoide):
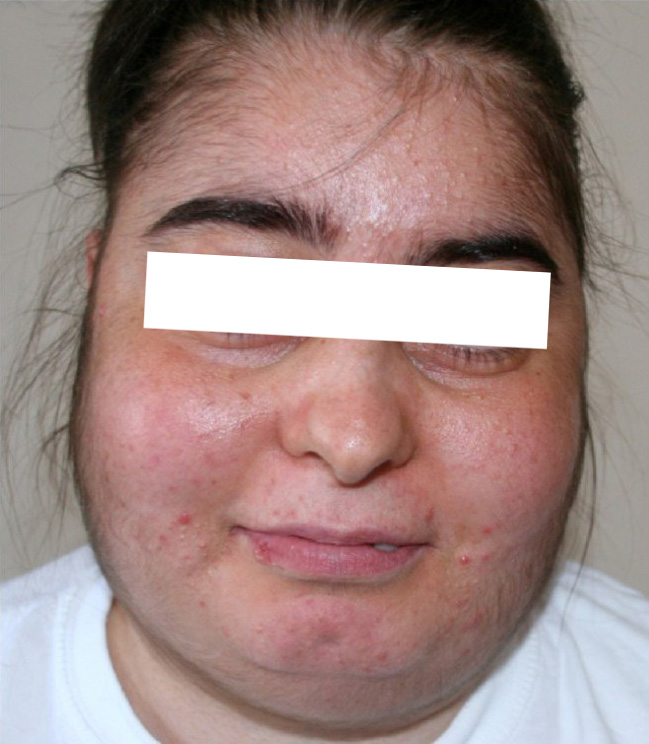
Características da síndrome de Cushing: mulher com apresentação de hirsutismo, acne e face lunar
Imagem: “Patient’s facial appearance” por Ozlem Celik et al. Licença: CC BY 2.5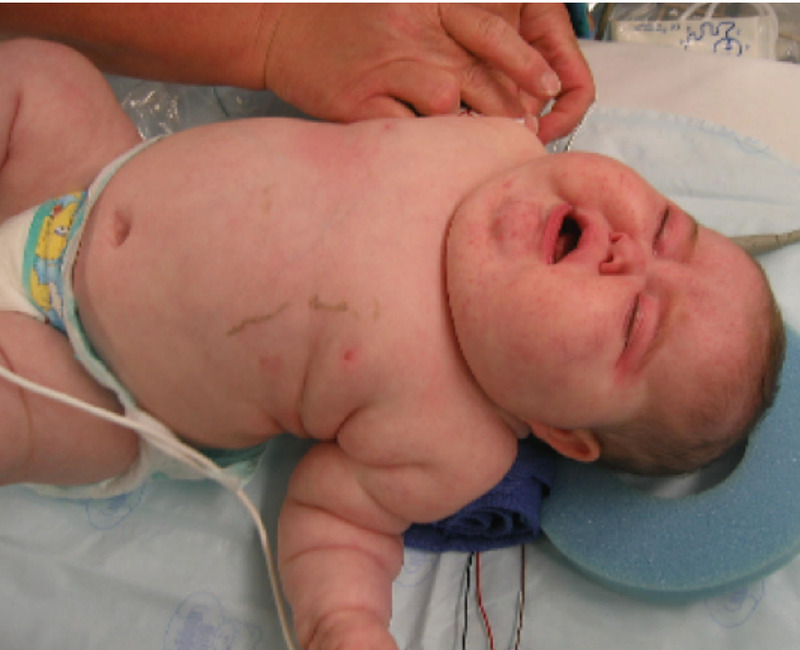
Recém-nascido com síndrome de Cushing:
As características observadas incluem face em lua cheia, plétora, acne, obesidade central e diminuição do tónus muscular.
As características clínicas aumentam a suspeita diagnóstica:
Excluir o uso de glicocorticoides exógenos:
Exames iniciais para diagnóstico de hipercortisolismo:
Resultados alterados solicitam avaliação adicional:
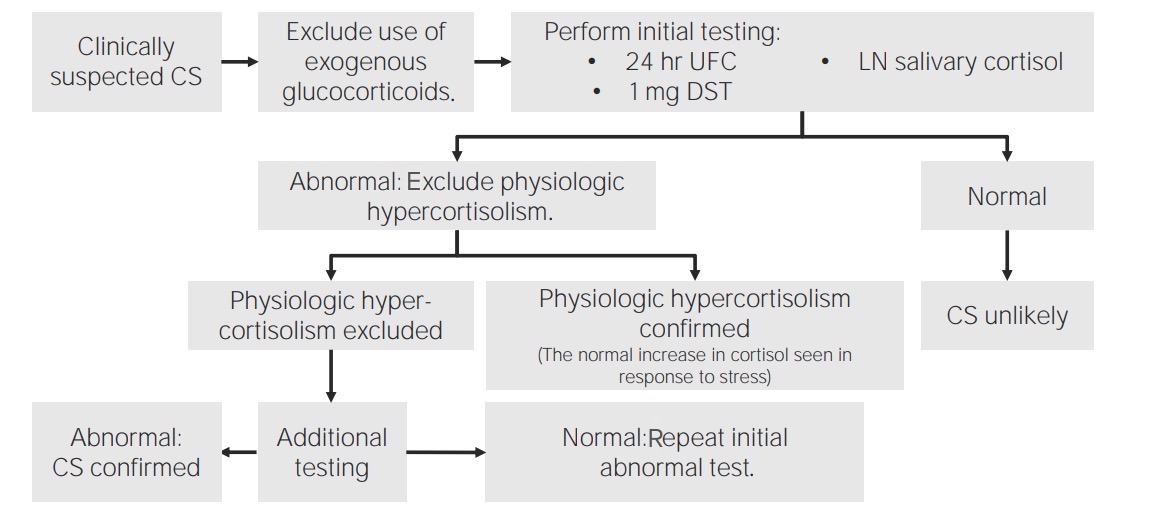
Algoritmo para diagnosticar hipercortisolismo ou síndrome de Cushing (SC):
Em doentes com suspeita clínica de SC, o 1º passo é descartar o uso exógeno de glicocorticoides. Uma vez excluídos, os testes iniciais para verificar a presença de níveis elevados de cortisol incluem o cortisol salivar noturno (LN, pela sigla em inglês), o cortisol urinário livre em 24 horas (UFC, pela sigla em inglês) e o teste de supressão com 1 mg de dexametasona (DST, pela sigla em inglês). Uma vez confirmados os níveis elevados de cortisol, avaliar se a elevação é decorrente de hipercortisolismo fisiológico. Uma vez excluídas as causas fisiológicas, prossiguir com testes adicionais para identificar a etiologia (que pode ser primária ou secundária).
Após confirmar a presença de níveis elevados de cortisol, a determinação da etiologia começa com a ACTH.
| Nível de ACTH | Etiologia e exames complementares | Identificação da causa |
|---|---|---|
| ↓ ACTH: independente da ACTH | Glândula suprarrenal (possível adenoma, carcinoma, hiperplasia) | Obter TC/RM da glândula suprarrenal. |
| ↑ ou ACTH intermediária: provavelmente dependente de ACTH | Doença de Cushing:
|
Obter RM da hipófise. |
Síndrome de ACTH ectópica (como cancro do pulmão, tumor carcinoide):
|
Exame para pesquisa de malignidade:
|