A lesão hepática induzida por fármacos (DILI, pela sigla em inglês) é a causa mais comum de insuficiência hepática aguda (FHA, pela sigla em inglês). Os fármacos hepatotóxicos podem causar lesão nos hepatócitos diretamente de forma dose-dependente previsível ou através de reações idiossincráticas (que podem ser mediadas por processos imunes ou não imunes). Os mecanismos de lesão podem ter os seguintes efeitos: hepatite, colestase, lesões vasculares ou alterações sobrepostas. A apresentação pode ser aguda ou crónica, com toxicidade grave que se manifesta como insuficiência hepática fulminante. O diagnóstico de DILI requer uma história completa e exames laboratoriais, incluindo testes de função hepática (LFT, pela sigla em inglês) e níveis de fármacos, se disponíveis. O tratamento consiste na suspensão do medicamento, terapia de suporte e monitorização de complicações. O paracetamol, uma das causas mais comuns de DILI, tem um tratamento específico, N-acetilcisteína (NAC).
Última atualização: Jan 17, 2024
O fígado lida com o metabolismo de fármacos/toxinas, tornando-o suscetível a lesões. Os próprios fármacos passam por processos para serem inativados e se tornarem solúveis em água (para uma adequada excreção renal ou biliar).
Reação de Fase I:
Reação de fase II:
Reação de fase III:
Hepatotoxinas intrínsecas/diretas:
Reações idiossincráticas:
Podem ocorrer potenciais sobreposições de mecanismos associados aos fármacos à medida que ocorrem alterações hepatocelulares e colestáticas mistas.
Mecanismos potenciais de como os fármacos causam lesão nas células do fígado:
Mecanismos potenciais de como os fármacos afetam a via de excreção biliar:
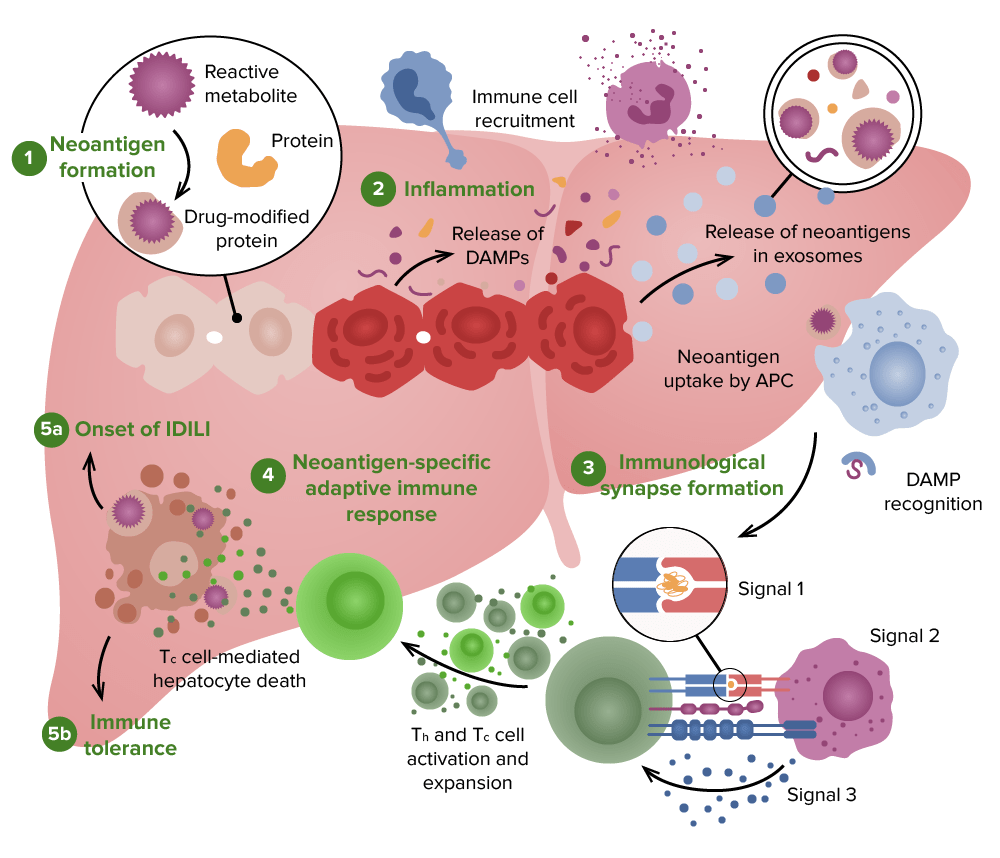
Fisiopatologia possível de uma doença hepática induzida por fármacos:
1. Pode ser formado um metabolito reativo pelos hepatócitos, que se pode ligar covalentemente a proteínas para formar neoantigénios.
2. A libertação de neoantigénios e as moléculas de padrão molecular associado a dano (DAMP, pela sigla em inglês) dos hepatócitos danificados, que podem levar à ativação das células apresentadoras de antigénio (APCs, pela sigla em inglês) e recrutamento de células do sistema imune inato.
3. A ativação de APC leva à expressão de sinal 1 e sinal 2
4. As células T-helper (Th) e T-citotóxicas (Tc) são ativadas, levando a uma resposta do sistema imune adaptativo.
5. 5a: A resposta imune dominante é uma lesão hepática induzida por fármacos idiossincrática (IDILI, pela sigla em inglês) e geralmente uma resposta imune mediada por células.
5b: Contudo, se a ligação do fármaco ou do péptido modificador de fármaco não for muito forte, a resposta imune adaptativa levará a tolerância imune, prevenindo ou limitando a lesão hepática.
Insuficiência hepática aguda:
Lesão hepática crónica :
A lesão hepática crônica é definida como tendo uma duração > 3 meses, assemelhando-se assim à doença hepática crónica ou cirrose:
Testes de função hepática:
Níveis de fármacos:
| Tipo de lesão | Análise sanguínea |
|---|---|
| Hepatite |
|
| Colestase |
|
| Misto |
|
Padrões histológicos de lesão:
| Padrão de lesão | Exemplos |
|---|---|
| Hepatite aguda |
|
| Hepatite crónica/fibrose |
|
| Hepatite colestática (mista) |
|
| Colestase |
|
| Esteatose ou esteato-hepatite |
|
| Granulomas |
|
| Lesões vasculares |
|
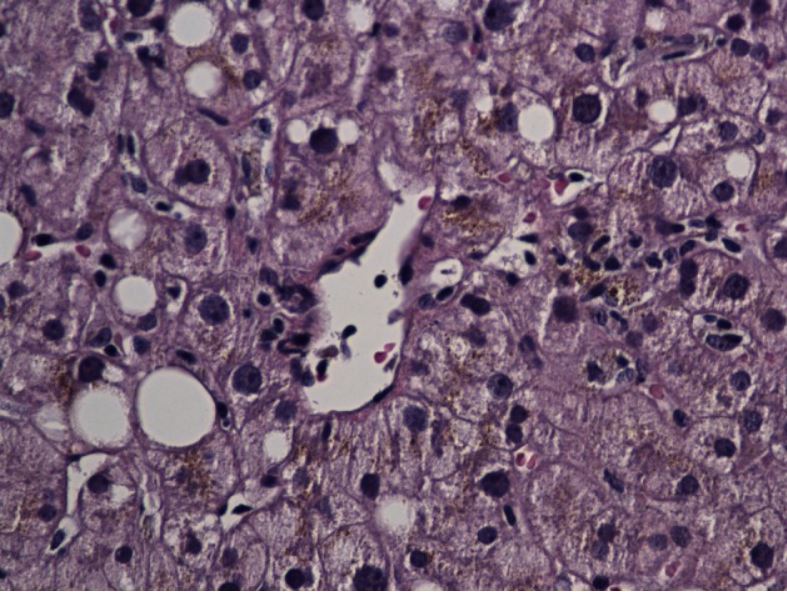
Amostra de biópsia hepática a mostrar hepatite lobular secundária ao ibuprofeno
Imagem : “A rare coexistence: drug-induced hepatitis and meningitis in association with Ibuprofen” por Nayudu SK, Kavuturu S, Niazi M, Daniel M, Dev A, Kumbum K. Licença: CC BY 2.0.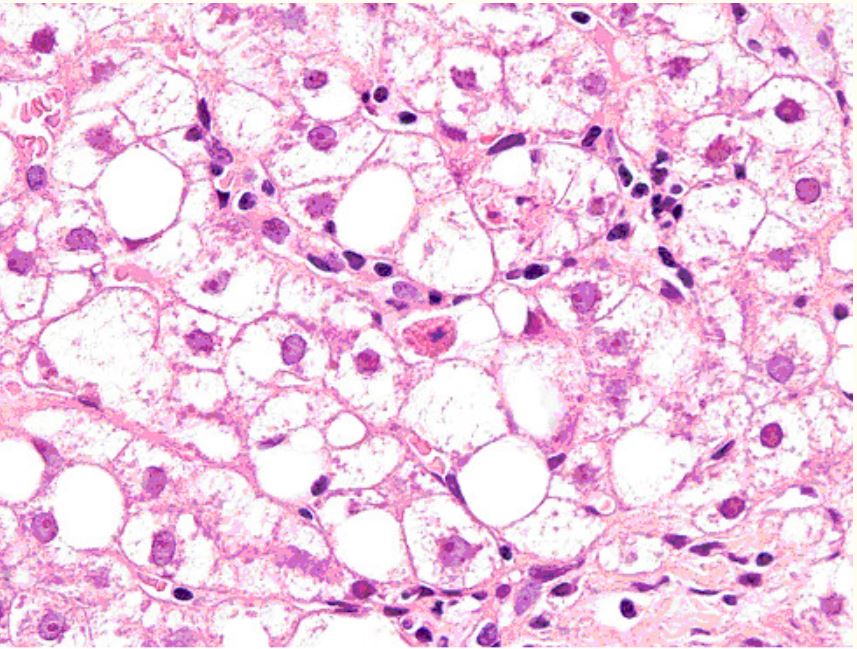
Biópsia hepática de um paciente com infeção pelo vírus da imunodeficiência humana (HIV) a tomar estavudina:
Os exames laboratoriais mostraram ALT/AST elevada; imagem mostrou corpos acidófilos e degeneração espumosa dos hepatócitos (esteatose).
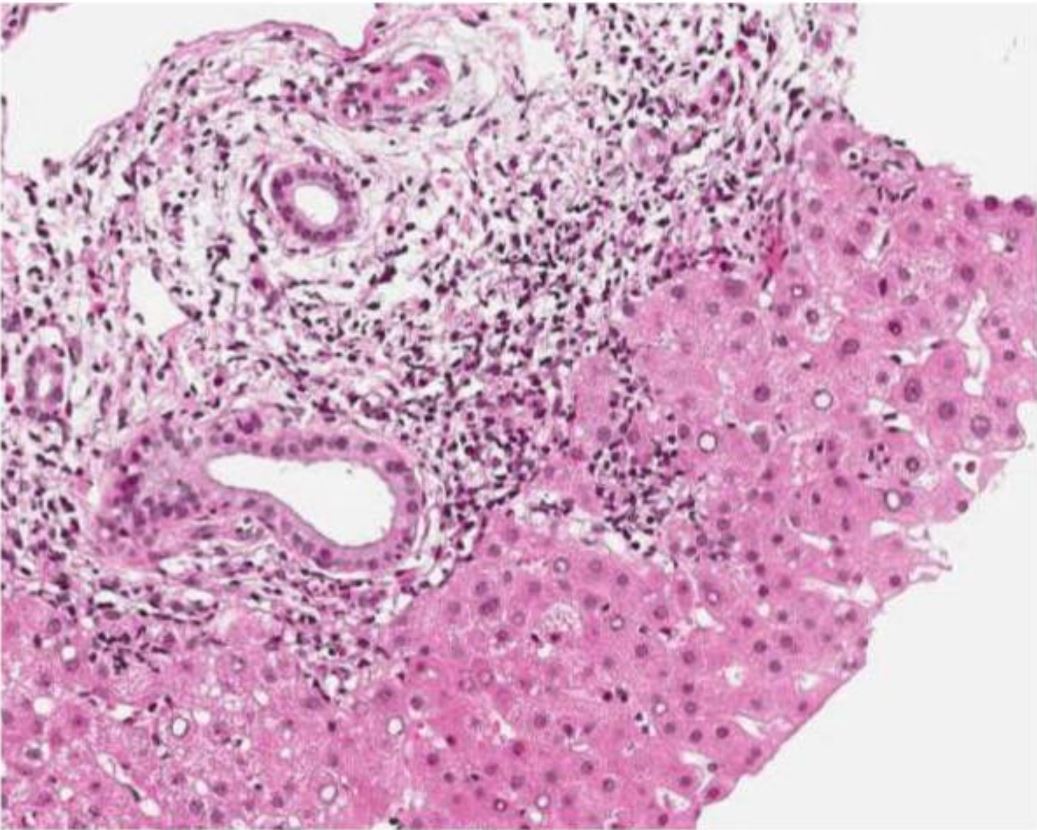
Biópsia hepática de um paciente com enzimas hepáticas elevadas após tratamento de infecção por Helicobacter pylori (claritromicina e amoxicilina):
A imagem mostra a inflamação portal.
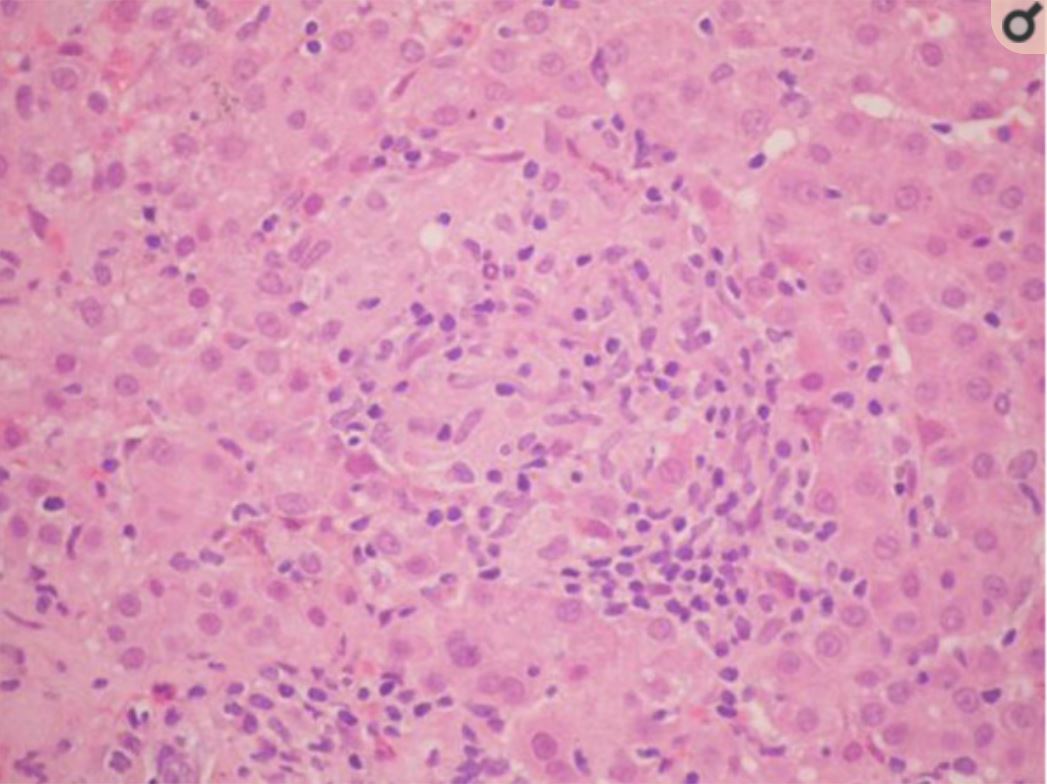
Imagem de hepatite granulomatosa induzida por albendazol:
parênquima hepático com macrófagos epitelioides que formaram granulomas sem necrose, intercalados com linfócitos
Tratamentos específicos limitados para a DILI:
Patogénese:
Apresentação clínica:
Diagnóstico:
Tratamento inicial:
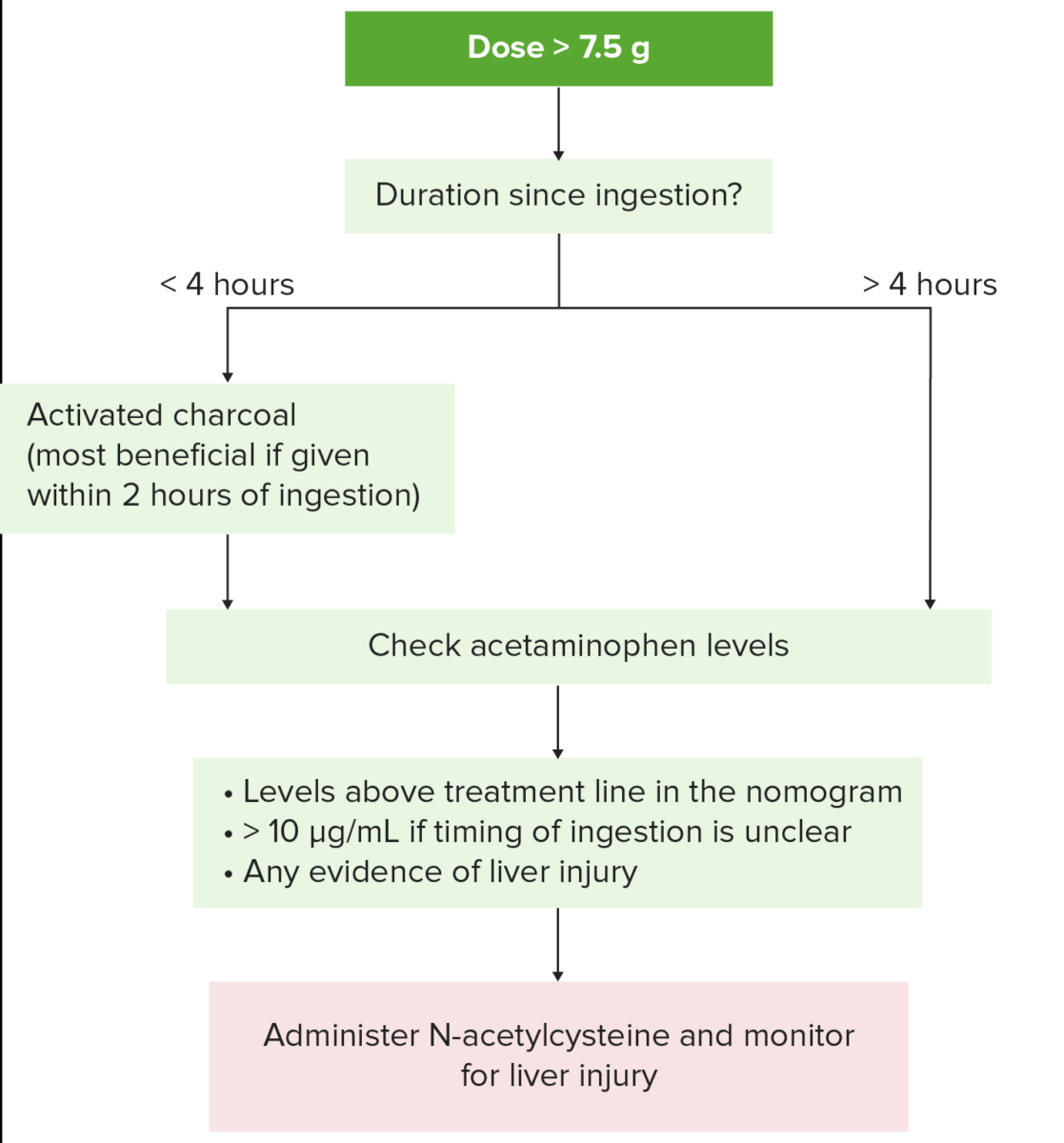
Tratamento da toxicidade do paracetamol:
1. Obter a história, identificar os agentes envolvidos e determinar a gravidade e a possível toxicidade do medicamento.
Se a ingestão de paracetamol (dose potencialmente tóxica> 7,5 g) foi< 4 horas, é administrado carvão ativado para evitar a absorção do fármaco residual.
O paciente deve estar alerta para proteger a via aérea e evitar a aspiração.
2. Obtenção dos níveis séricos de paracetamol (recomendado 4 horas após a ingestão; o 2º nível de fármaco é obtido mais tarde se foi ingerida a preparação de libertação prolongada).
3. A N-acetil-cisteína é administrada nos seguintes casos:
Níveis acima da linha de tratamento no nomograma
O tempo de ingestão não é claro e os níveis séricos de paracetamol estão > 10 µg/mL
Evidência de hepatotoxicidade
Suspeita de dose única de> 7,5 g ou 150 mg/kg e o resultado dos níveis de paracetamol não estarão disponíveis em pelo menos 8 horas.
Tratamento:
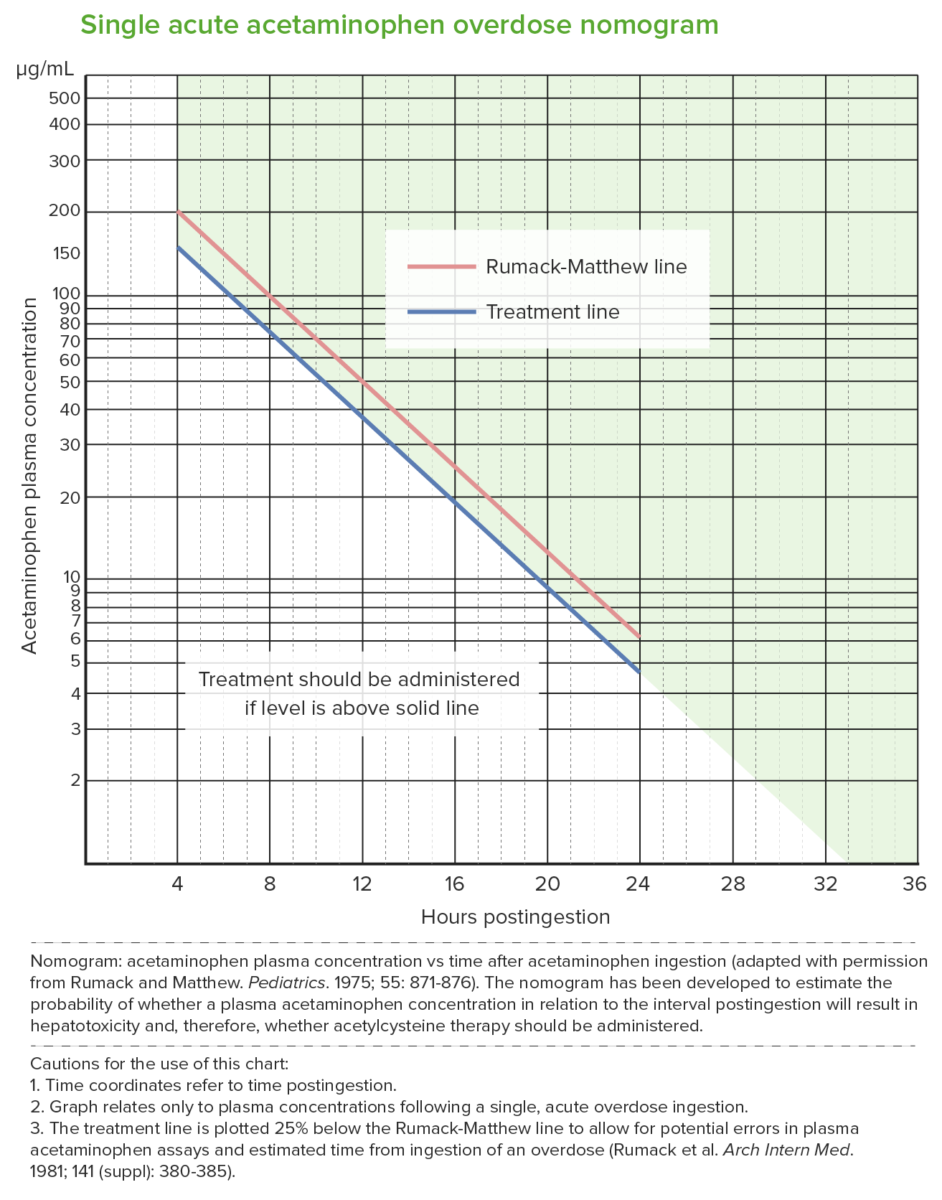
Nomograma de Rumack-Matthew (nomograma de toxicidade para o paracetamol):
O nomograma é usado após uma única ingestão aguda de paracetamol e prevê a hepatotoxicidade potencial a partir de 4 horas após a ingestão. Níveis medidos antes das 4 horas podem não ser confiáveis.
O nomograma não pode ser usado para ingestões que ocorreram> 24 horas antes da apresentação.
A linha superior (vermelha) é a linha Rumack-Mateus; valores acima desta linha desenvolvem toxicidade (observada em 60%).
A linha inferior (azul) é a linha de tratamento (a Food and Drug Administration dos EUA exigiu que a linha de tratamento estivesse 25% abaixo da linha original).
O tratamento com NAC é administrado quando o nível de paracetamol está na linha de tratamento 4 horas após a ingestão (que está abaixo do limite de toxicidade).