A medula óssea, o local primário da hematopoiese, é encontrada nas cavidades dos ossos esponjosos e nos canais medulares dos ossos longos. Existem 2 tipos: medula vermelha (hematopoiética com abundantes células sanguíneas) e medula amarela (predominantemente preenchida com adipócitos). A composição da medula humana muda com a idade. Nos jovens, toda a medula óssea é vermelha, pois há aumento da produção de células sanguíneas. À medida que a idade aumenta, há uma mudança gradual para a variedade de medula amarela. A medula amarela pode reverter para medula vermelha quando a hematopoiese é necessária (por exemplo, anemia Anemia Anemia is a condition in which individuals have low Hb levels, which can arise from various causes. Anemia is accompanied by a reduced number of RBCs and may manifest with fatigue, shortness of breath, pallor, and weakness. Subtypes are classified by the size of RBCs, chronicity, and etiology. Anemia: Overview and Types). A medula vermelha, por hematopoiese, produz cerca de 6 bilhões de células por quilograma por dia. O processo depende de células hematopoiéticas (células estaminais e progenitoras) produzindo células efetoras maduras (linfócitos, plaquetas, granulócitos, eritrócitos) com o auxílio de elementos não hematopoiéticos. A produção é regulada por citocinas libertadas no ambiente da medula óssea e feedback dos tecidos-alvo. A estrutura da medula permite que a hematopoiese ocorra na área extravascular e, após a diferenciação em estadios, as células sanguíneas são libertadas na circulação.
Last updated: Mar 27, 2025
A medula óssea é o tecido esponjoso encontrado nos canais medulares dos ossos longos e nas cavidades dos ossos esponjosos.
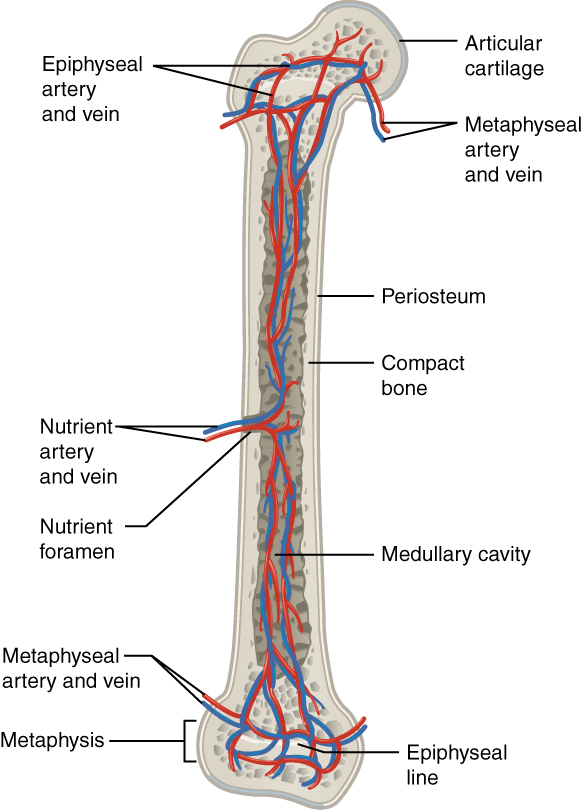
A imagem mostra o suprimento de sangue (artéria e veia)
Imagem : “609 Body Supply to the Bone” por OpenStax College. Licença: CC BY 3.0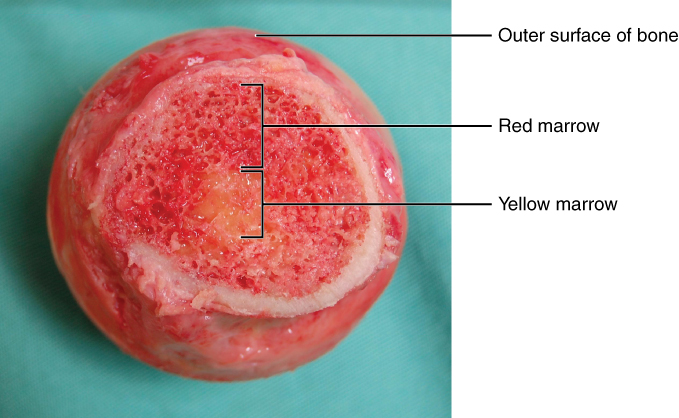
Medula óssea:
Corte transversal que mostra as porções de medula vermelha e amarela do osso
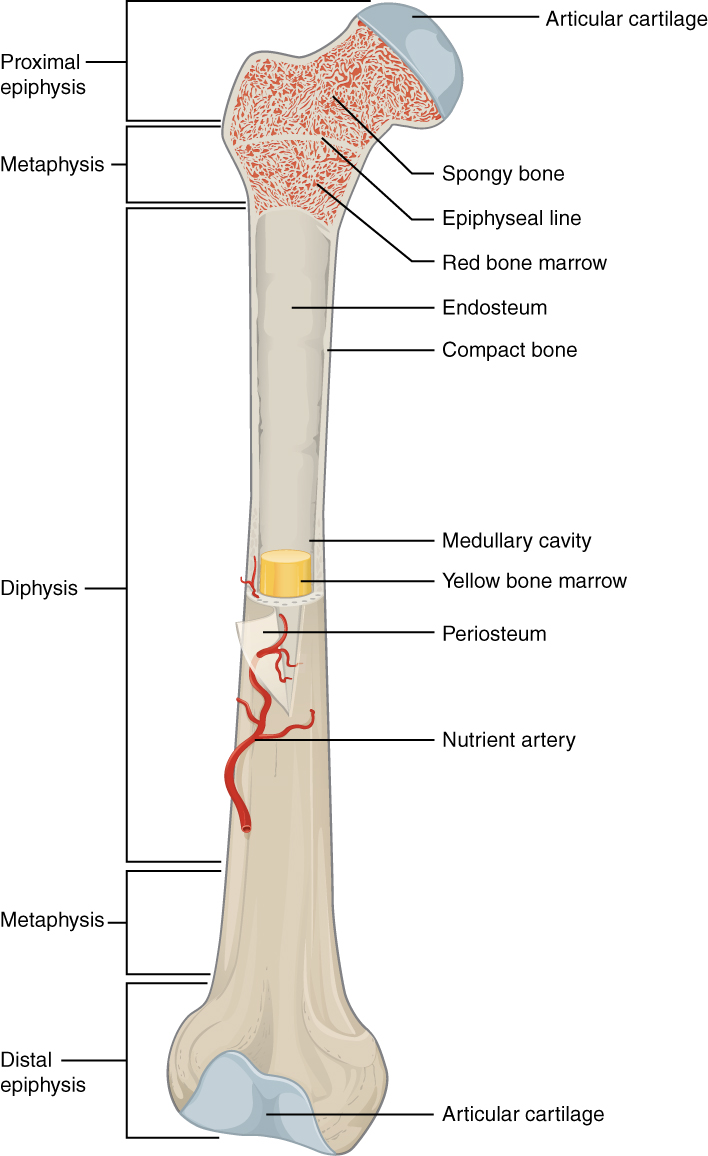
Medula óssea dentro do fémur
Imagem : “603 Anatomy of Long Bone” por OpenStax College. Licença: CC BY 3.0Estruturas que fornecem um microambiente que suporta a diferenciação de células hematopoiéticas e proliferação de células sanguíneas:
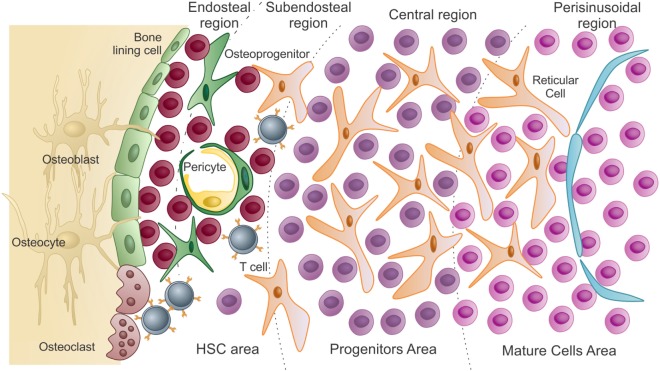
Apresentação esquemática do microambiente da medula óssea:
Na área das células estaminais hematopoiéticas (CTH, pela sigla em inglês) estão as células estaminais hematopoiéticas e os progenitores não comprometidos. Estes estão em estreita associação com osteoblastos endosteais e células de revestimento ósseo. À medida que as HSCs saem da quiescência para estados proliferativos, elas migram e colonizam a região subendosteal, depois a região central da medula (progenitores).
As células diferenciadas atingem a área madura, mais próxima dos sinusoides. Para serem libertadas na circulação, estas células maduras passam pelo endotélio (revestindo os sinusoides) por migração transcelular.
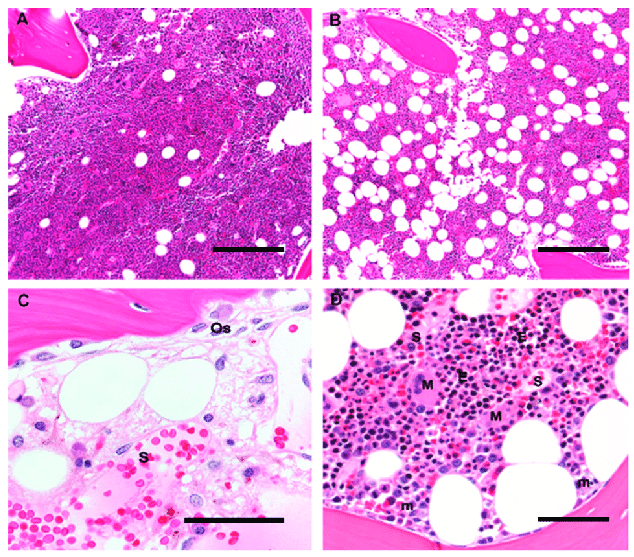
Arquitetura histológica da medula óssea humana: As imagens mostram as diferentes células e estruturas que estão na medula.
A e B: Ampliação original 10x; barra de escala 100 μm
A: Biópsia de medula óssea de uma criança de 5 anos é> 90% celular, com predominância de hematopoiese de trilinhagem e tecido adiposo pouco misturado.
B: Biópsia de medula óssea de um adulto de 60 anos é composta por 50% de elementos hematopoiéticos e 50% de tecido adiposo maduro misto.
C: Uma medula pós-quimioterapia mostra osso trabecular com osteoblastos (Os) apostos e uma fina camada osteoide de colagénio não mineralizado. Os sinusoides (S) são preenchidos com hemácias e possuem células estromais com núcleos ovoides. As células mononucleares dispersas incluem plasmócitos, mastócitos e macrófagos; ampliação original 60×; barra de escala 25 μm
D: As colónias eritroides (E) aparecem como colónias de células redondas com núcleos escuros e estão localizadas longe do osso trabecular, próximas aos vasos sinusoidais de paredes finas (S); os megacariócitos (M) também estão localizados em contacto próximo com os sinusoides, enquanto os precursores mieloides imaturos (m) estão localizados próximos ao osso trabecular. Ampliação original 20×; barra de escala 50 μm
A hematopoiese começa com uma HSC, estimulada a dividir-se e diferenciar com estímulos químicos apropriados (fatores de crescimento hemopoiéticos).
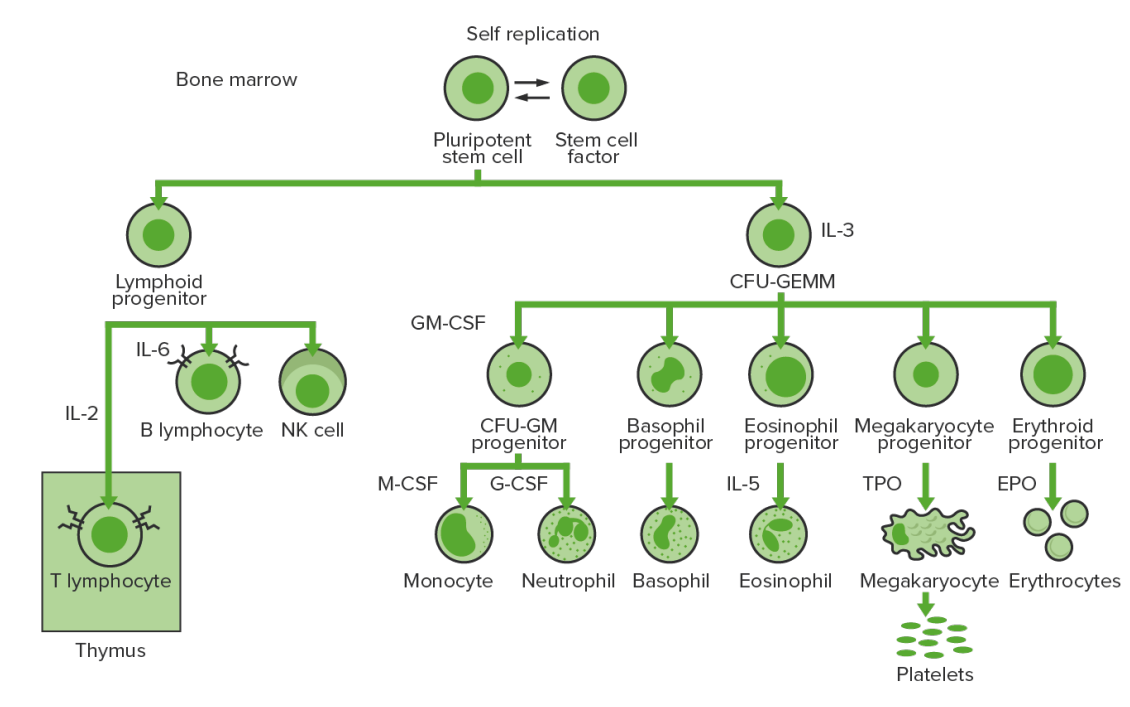
Hematopoiese da medula óssea: proliferação e diferenciação dos elementos figurados do sangue
UFC-GEMM: unidade formadora de colónias: granulócito, eritrócito, monócito, megacariócito
UFC-GM: unidade formadora de colónias: granulócito-macrófago
GM-CSF: fator estimulador de colónias de granulócitos-macrófagos
M-CSF: fator estimulador de colónias de macrófagos
G-CSF: fator estimulador de colónias de granulócitos
NK: “natural killer”
TPO: trombopoietina
| Citocinas/fatores de crescimento | Atividades | Origem |
|---|---|---|
| Eritropoietina ( EPO EPO Glycoprotein hormone, secreted chiefly by the kidney in the adult and the liver in the fetus, that acts on erythroid stem cells of the bone marrow to stimulate proliferation and differentiation. Erythrocytes: Histology) | Estimula a eritropoiese, incluindo a diferenciação |
|
| Trombopoietina (TPO) | Estimula a trombopoiese |
|
| Fator de células estaminais (SCF, pela sigla em inglês) | Estimula todas as células progenitoras hematopoiéticas | Células estromais da medula óssea |
| Fator estimulador de colónias de granulócitos-macrófagos ( GM-CSF GM-CSF An acidic glycoprotein of mw 23 kda with internal disulfide bonds. The protein is produced in response to a number of inflammatory mediators by mesenchymal cells present in the hemopoietic environment and at peripheral sites of inflammation. GM-CSF is able to stimulate the production of neutrophilic granulocytes, macrophages, and mixed granulocyte-macrophage colonies from bone marrow cells and can stimulate the formation of eosinophil colonies from fetal liver progenitor cells. GM-CSF can also stimulate some functional activities in mature granulocytes and macrophages. White Myeloid Cells: Histology, pela sigla em inglês) | Estimula as células progenitoras mieloides |
|
| Fator estimulante de colónias de granulócitos (FG-CSF, pela sigla em inglês) | Estimula as células precursoras de neutrófilos |
|
| Fator estimulador de colónias de monócitos ( M-CSF M-CSF A mononuclear phagocyte colony-stimulating factor (M-CSF) synthesized by mesenchymal cells. The compound stimulates the survival, proliferation, and differentiation of hematopoietic cells of the monocyte-macrophage series. M-CSF is a disulfide-bonded glycoprotein dimer with a mw of 70 kda. It binds to a specific high affinity receptor. White Myeloid Cells: Histology, pela sigla em inglês) | Estimula as células precursoras de monócitos |
|
| Interleucina (IL) | Atividades | Origem |
|---|---|---|
| IL-1 | Regulação da secreção de citocinas de muitos leucócitos |
|
| IL-2 |
|
Células T auxiliares |
| IL-3 | Mitogénio para todas as células progenitoras de granulócitos e megacariócitos/eritrócitos | Células T auxiliares |
| IL-4 |
|
Células T auxiliares |
| IL-5 | Desenvolvimento e ativação de eosinófilos | Células T auxiliares |
| IL-6 |
|
|
| IL-7 IL-7 A proinflammatory cytokine produced primarily by T-lymphocytes or their precursors. Several subtypes of interleukin-17 have been identified, each of which is a product of a unique gene. Severe Combined Immunodeficiency (SCID) | Estimulação de todas as células estaminais linfoides | Células estromais da medula óssea |
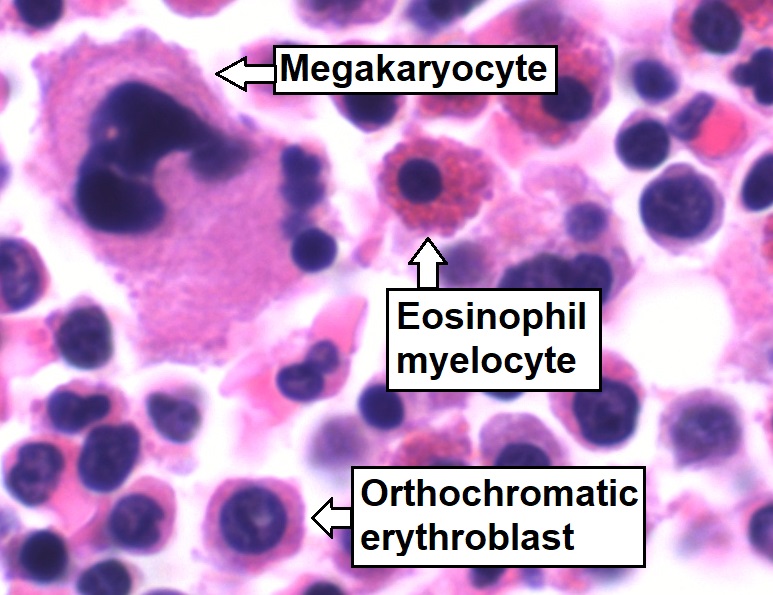
Aspirado de medula óssea que mostra hematopoiese de trilinhagem normal: células mielomonocíticas (mielócito eosinofílico marcado), células eritroides (eritroblasto ortocromático marcado) e células megacariocíticas
Imagem : “Trilineage hematopoiesis” por Mikael Häggström. Licença: CC0 1.0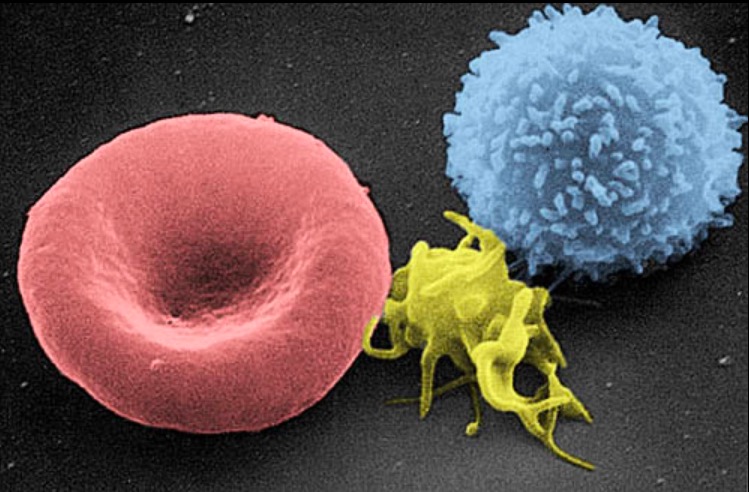
Imagem de micrografia eletrónica de scanning de uma célula sanguínea: da esquerda para a direita, um glóbulo vermelho humano, um trombócito (plaquetas) e um leucócito
Imagem : “Electron micrograph of blood cells” por Electron Microscopy Facility at The National Cancer Institute at Frederick. Licença: Public Domain