A anemia Anemia Anemia is a condition in which individuals have low Hb levels, which can arise from various causes. Anemia is accompanied by a reduced number of RBCs and may manifest with fatigue, shortness of breath, pallor, and weakness. Subtypes are classified by the size of RBCs, chronicity, and etiology. Anemia: Overview and Types aplásica ( AA AA Amyloidosis) é uma condição rara que condiciona risco de vida, caracterizada por pancitopenia e hipocelularidade da medula óssea (na ausência de células anormais), refletindo o dano nas células-estaminais hematopoiéticas. A anemia Anemia Anemia is a condition in which individuals have low Hb levels, which can arise from various causes. Anemia is accompanied by a reduced number of RBCs and may manifest with fatigue, shortness of breath, pallor, and weakness. Subtypes are classified by the size of RBCs, chronicity, and etiology. Anemia: Overview and Types aplásica pode ser adquirida ou hereditária. No entanto, a maioria dos casos de AA AA Amyloidosis é adquirida e causada por um dano autoimune nas células-estaminais hematopoiéticas. Causas adquiridas e associações de AAs especificamente conhecidas incluem medicamentos, produtos químicos, altas doses de radiação de corpo inteiro, infeções víricas, doenças imunológicas e gravidez. Os síndromes hereditários ou constitucionais associadas à AA AA Amyloidosis incluem anemia Anemia Anemia is a condition in which individuals have low Hb levels, which can arise from various causes. Anemia is accompanied by a reduced number of RBCs and may manifest with fatigue, shortness of breath, pallor, and weakness. Subtypes are classified by the size of RBCs, chronicity, and etiology. Anemia: Overview and Types de Fanconi, disqueratose congénita e síndrome de Down. As opções terapêuticas incluem transfusões de suporte, imunossupressão e transplante de medula óssea.
Last updated: Dec 15, 2025
Condições hereditárias:
AA AA Amyloidosis adquirida:
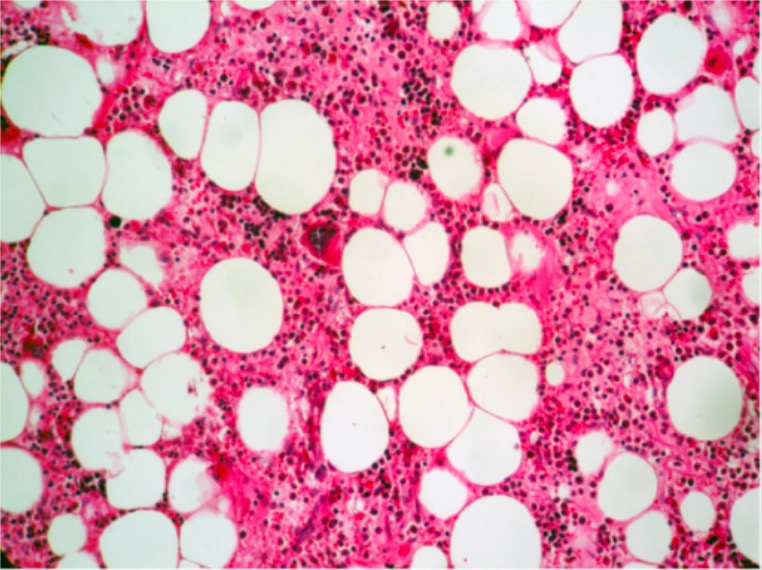
Hematopoiese normal (todas as 3 linhas celulares presentes) com um megacariócito no centro do campo (H&E, 200x)
Imagem : “Histologic findings” por Department of Pathology, Ibn Sina University Hospital, Rabat, Morocco. Licença: CC BY 2.0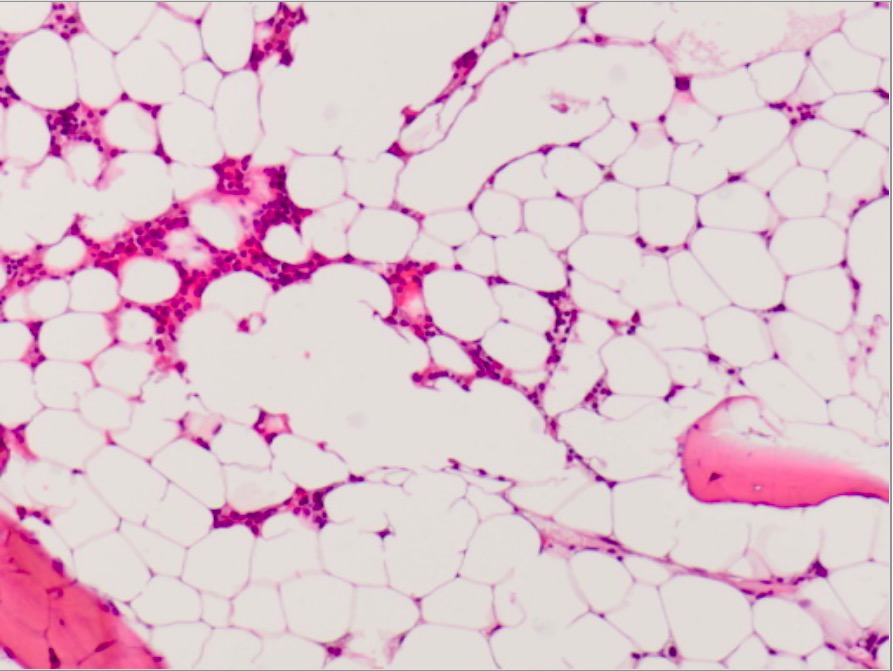
Fotografia microscópica da medula óssea com AA:
Medula óssea marcadamente hipocelular de um paciente com AA adquirido (mostra apenas hematopoiese escassa e principalmente células de gordura)
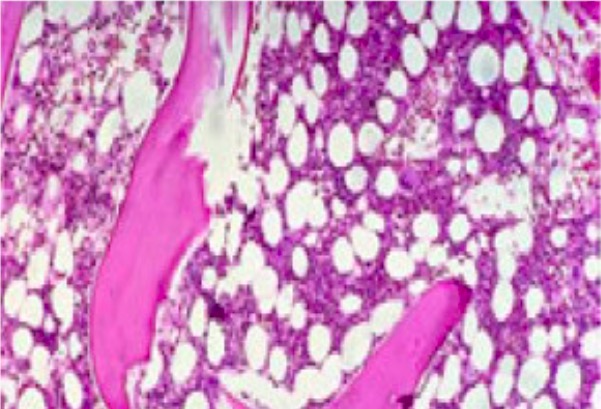
Medula óssea com celularidade de aproximadamente 50% (consistente com a medula óssea de uma pessoa saudável de 50 anos)
Imagem : “Mild hypoblastic marrow” por Hasnaa Aboelwafa et al. Licença: CC BY 2.0 , recortado por Lecturio.Pancitopenia com medula óssea hipocelular: