A tricoleucemia é uma leucemia de células B crónica e rara, caracterizada pela acumulação de pequenos linfócitos B maduros com projeções citoplasmáticas semelhantes a fios de cabelo visíveis ao microscópio. Estas células alteradas acumulam-se no sangue periférico, medula óssea (causando fibrose) e polpa vermelha do baço, causando citopenias, incluindo anemia, trombocitopenia, neutropenia e monocitopenia. A tricoleucemia geralmente afeta homens de meia-idade e apresenta-se com astenia, fadiga, infeções oportunistas e esplenomegalia (geralmente grave). O diagnóstico é realizado pela identificação de células pilosas no esfregaço de sangue periférico, citopenias características no hemograma com contagem diferencial, biópsia de medula óssea e imunofenotipagem. O tratamento consiste na observação de doentes assintomáticos e administração de análogos de purinas em doentes sintomáticos. A doença e os seus tratamentos podem causar imunossupressão; deste modo, a prevenção e o tratamento imediato de infeções também são importantes.
Última atualização: Mar 28, 2022
A tricoleucemia, também conhecida como leucemia de células pilosas, é uma leucemia de células B crónica e rara, caracterizada pela acumulação de pequenos linfócitos B maduros com projeções citoplasmáticas semelhantes a fios de cabelo visíveis ao microscópio.
A tricoleucemia é uma neoplasia clonal de células B. A etiologia exata é desconhecida, mas várias exposições ambientais parecem aumentar o risco do desenvolvimento desta doença.
A problemática subjacente na tricoleucemia é o aumento da produção de linfócitos B pela medula óssea, excluindo os outros tipos de células sanguíneas. Estas células B anormais são incapazes de proteger o organismo de agentes invasores infeciosos da mesma forma que as células B normais.
A patogénese não é completamente compreendida, mas a maioria dos casos parece surgir de células B de memória ativadas tardiamente, que adquirem uma mutação ativadora do gene BRAF V600E.
O diagnóstico é baseado na identificação de células pilosas no esfregaço de sangue periférico, imunohistoquímica e/ou citometria de fluxo e, eventualmente, na biópsia de medula óssea.
Os achados laboratoriais podem incluir:
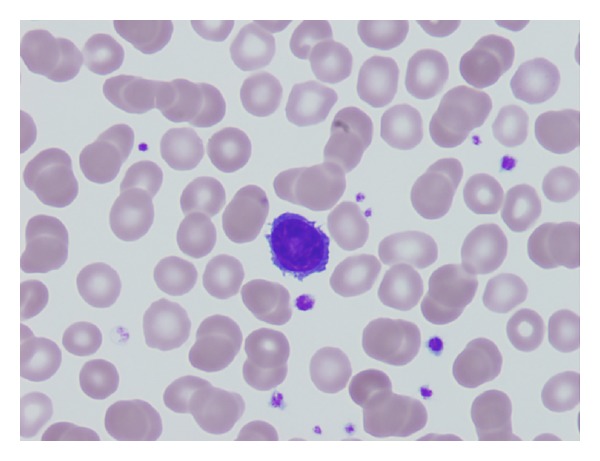
Esfregaço de sangue periférico que revela uma célula pilosa
Imagem: “Primary hairy cell leukemia/lymphoma of the breast: a case report and review of the literature” por Pilichowska M, Shariftabrizi A, Mukand-Cerro I, Miller K. License: CC BY 3.0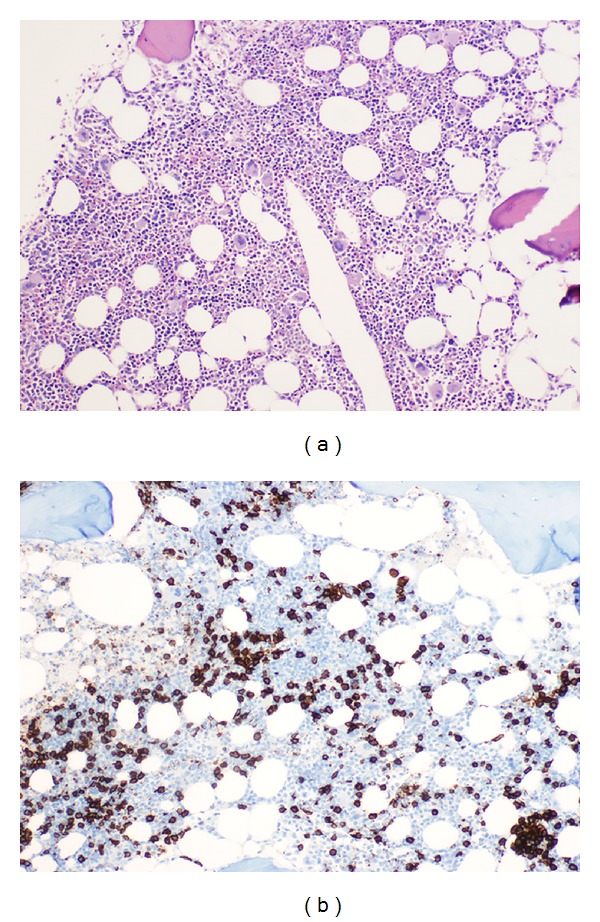
Biópsia de medula óssea:
(a): Infiltrado difuso bastante impercetível de pequenos linfócitos maduros (H&E, 200×).
(b): A coloração imunohistoquímica para CD20 revela a presença de células B no infiltrado (imunoperoxidase, 200×).
Os doentes assintomáticos devem ser observados, sem realização de tratamento.
O tratamento está indicado nas seguintes situações clínicas: