A terapia direcionada exerce atividade antineoplástica contra células cancerígenas ao interferir com propriedades únicas encontradas em tumores ou neoplasias malignas. Os tipos de fármacos podem ser moléculas pequenas, capazes de entrar nas células, ou anticorpos monoclonais, que têm alvos fora ou na superfície das células. Entre as áreas das células malignas que são bloqueadas ou inibidas por terapia direcionada estão as vias de sinalização (como visto nos inibidores da proteína cinase), que levam a uma diminuição da proliferação e subsequente apoptose das células tumorais. Outra forma de reduzir as células cancerígenas é ao eliminar a capacidade de reparação do DNA (visto nos inibidores da poli(ADP-ribose) polimerase), bloquear a ligação ligando-recetor (inibidores de fatores de crescimento) e aumentar a atividade imune contra a neoplasia (imunoterapias). Estes agentes são utilizados em vários tipos de cancro e em combinação com agentes quimioterápicos tradicionais.
Última atualização: Jun 1, 2022
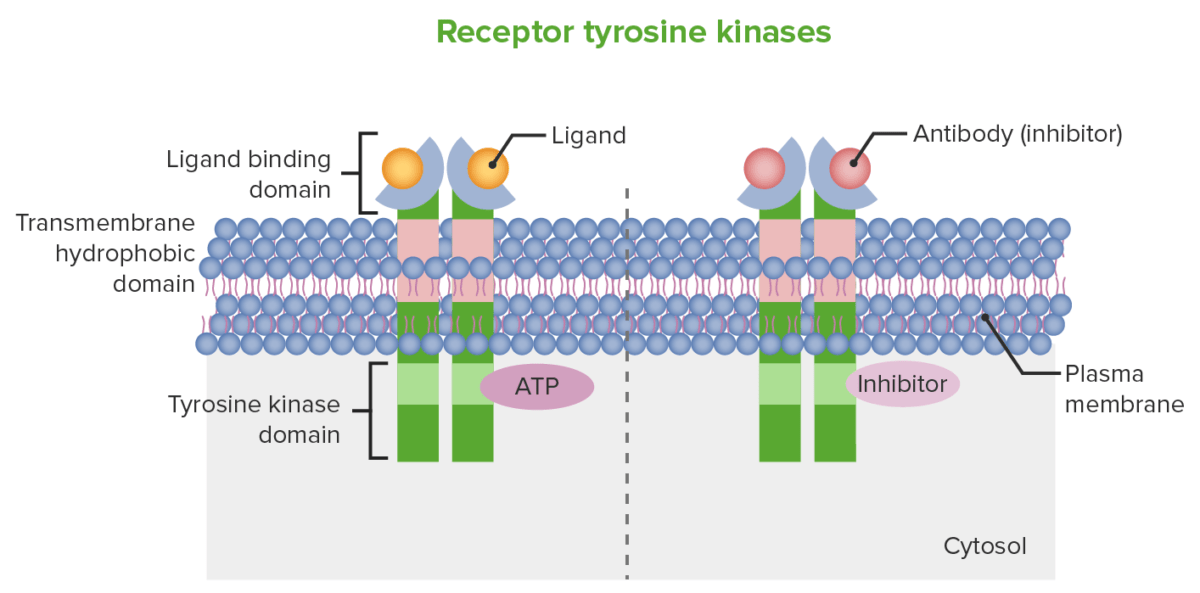
Mecanismo esquemático para inibição do recetor de tirosina cinase: À esquerda, a imagem mostra a estrutura do recetor da célula. Na superfície da célula encontra-se o domínio ligante e o domínio cinase (nesta imagem, tirosina cinase) está presente intracelularmente. À direita, a imagem mostra como um anticorpo monoclonal pode produzir atividade antineoplásica, que é através da inibição mediada por anticorpos do domínio de ligação ao ligando. Pequenas moléculas, que conseguem entrar nas células, são capazes de produzir inibição do domínio de ligação à ATP (tirosina cinase).
Imagem por Lecturio.| Imatinib | Dasatinib | Nilotinib | |
|---|---|---|---|
| Farmacodinâmica |
|
||
| Farmacocinética |
|
||
| Indicações |
|
||
| Efeitos adversos |
|
|
|
| Contraindicações |
|
||
| Vemurafenib | Dabrafenib* | |
|---|---|---|
| Farmacodinâmica | Inibem a atividade de BRAF cinase mutada (incluindo a mutação V600) | |
| Farmacocinética |
|
|
| Indicações |
|
|
| Efeitos adversos |
|
|
| Contraindicações | Hipersensibilidade ao fármaco | |
| Trametinib | Cobimetinib | |
|---|---|---|
| Farmacodinâmica | Inibe a ativação de MEK e a atividade cinase | |
| Farmacocinética |
|
|
| Indicações |
|
Melanoma |
| Efeitos adversos |
|
|
| Contraindicações | Hipersensibilidade ao fármaco | |
| Ruxolitinib | Barcitinib | |
|---|---|---|
| Farmacodinâmica | Inibem JAK | |
| Farmacocinética |
|
|
| Indicações |
|
|
| Efeitos adversos |
|
|
| Contraindicações | Hipersensibilidade ao fármaco | |
| Palbociclib | Abemaciclib | |
|---|---|---|
| Farmacodinâmica | Inibidor da CDK; impede a progressão pelo ciclo celular, levando a uma paragem na fase G1 | |
| Farmacocinética |
|
|
| Indicações | Cancro da mama avançado | |
| Efeitos adversos |
|
|
| Contraindicações | Hipersensibilidade ao fármaco | |
| Ibrutinib | Acalabrutinib | |
|---|---|---|
| Farmacodinâmica | Inibição de BTK, o que leva à redução da proliferação de células B e do crescimento tumoral | |
| Farmacocinética |
|
|
| Indicações |
|
|
| Efeitos adversos |
|
|
| Contraindicações | Hipersensibilidade ao fármaco | |
| Crizotinib | Alectinib | Ceritinib | |
|---|---|---|---|
| Farmacodinâmica | Inibe a ALK, prevenindo a proliferação e sobrevivência de tumores ALK-positivos | ||
| Farmacocinética |
|
|
|
| Indicações |
|
||
| Efeitos adversos |
|
||
| Contraindicações | Hipersensibilidade ao fármaco | ||
| Cetuximab | Panitumumab | |
|---|---|---|
| Farmacodinâmica |
|
|
| Farmacocinética |
|
|
| Indicações |
|
|
| Efeitos adversos |
|
|
| Contraindicações | Hipersensibilidade ao fármaco ou aos seus componentes | |
| Afatinib | Erlotinib | Gefitinib | |
|---|---|---|---|
| Farmacodinâmica | Inibidor da tirosina quinase de EGFR | ||
| Farmacocinética |
|
|
|
| Indicações | CPNPC (com mutações) |
|
CPNPC (com mutações no EGFR) |
| Efeitos adversos |
|
||
| Contraindicações | Hipersensibilidade ao fármaco ou aos seus componentes | ||
| Bevacizumab | Ziv-aflibercept | Sorafenib | |
|---|---|---|---|
| Farmacodinâmica | Anticorpo monoclonal para o ligando do VEGF | Proteína de fusão recombinante que atua como um recetor falso | Inibe as tirosina cinases de VEGFR (e também PDGF) |
| Farmacocinética |
|
|
|
| Indicações |
|
CCR metastático |
|
| Efeitos adversos |
|
||
| Contraindicações |
|
Nenhuma indicada |
|
| Trastuzumab | Pertuzumab | Lapatinib | |
|---|---|---|---|
| Farmacodinâmica | Anticorpo monoclonal que liga ao HER2 (domínio extracelular) | Inibidor duplo de cinases (inibe o EGFR e o HER2) | |
| Farmacocinética |
|
|
|
| Indicações |
|
Cancro da mama | Cancro da mama |
| Efeitos adversos |
|
|
|
| Contraindicações | Hipersensibilidade ao fármaco | ||
| Olaparib | Rucaparib | Niraparib | |
|---|---|---|---|
| Farmacodinâmica | Inibidor da enzima PARP | ||
| Farmacocinética |
|
|
|
| Indicações |
|
|
Cancro do ovário, da trompa de Falópio ou peritoneal primário |
| Efeitos adversos comuns |
|
||
| Efeitos adversos |
|
|
|
| Contraindicações | Hipersensibilidade ao fármaco | Nenhuma indicada | Hipersensibilidade ao fármaco |
| Fármacos | Atividade |
|---|---|
Inibidores de proteína cinase:
|
Inibem a ação das enzimas proteína cinases |
Inibidores dos recetores de fatores de crescimento:
|
|
| Inibidores de PARP | ↓ Capacidade de reparação do DNA |
| Inibidores de BCL2 | Promovem a apoptose de células cancerígenas (que dependem desta via) |
| Inibidores de CD20 | Ligam-se ao antigénio da superfície celular e iniciam a lise de células B |
| Inibidores da via Hedgehog | Ligam-se à componente proteica e inibem a transdução de sinal da via Hedgehog, ↓ a proliferação das células (no carcinoma basocelular) |
| Inibidores de pontos de controlo imunes | Inibem os pontos de controlo imunes (CTLA4, PD-1), permitindo a ativação e proliferação de células T |
| Inibidores de mTOR | Inibem a atividade da mTOR cinase, levando à redução da síntese de proteínas, proliferação celular e angiogénese |
| Inibidores do proteassoma | Bloqueam a atividade proteassómica, interrompendo a sinalização e aumentando a apoptose celular |
| Asparaginase | Esgota a asparagina, reduzindo assim a fonte de células leucémicas |
| Talidomida |
|