A miocardiopatia hipertrófica (MCH) é a miocardiopatia hereditária mais MAIS Androgen Insensitivity Syndrome frequentemente herdada, caracterizada por um aumento da espessura (hipertrofia) assimétrico da parede ventricular esquerda, disfunção diastólica e, muitas vezes, obstrução da saída do ventrículo esquerdo. A miocardiopatia hipertrófica é causada por várias mutações genéticas que afetam os componentes contráteis do coração, conhecidos como sarcómeros. A hereditariedade da MCH é tipicamente autossómica dominante, embora também ocorram mutações esporádicas. Os pacientes podem ser assintomáticos, apresentar dispneia e dor torácica ou sofrer morte súbita cardíaca sem sintomas prévios. O diagnóstico é feito com base no ECG ECG An electrocardiogram (ECG) is a graphic representation of the electrical activity of the heart plotted against time. Adhesive electrodes are affixed to the skin surface allowing measurement of cardiac impulses from many angles. The ECG provides 3-dimensional information about the conduction system of the heart, the myocardium, and other cardiac structures. Electrocardiogram (ECG), ecocardiograma, testes Testes Gonadal Hormones de stress cardíaco e ressonância magnética cardíaca. A MCH sintomática é tratada normalmente com beta-bloqueadores como terapêutica de 1ª linha. O tratamento adicional depende da presença de obstrução da via de saída do ventrículo esquerdo.
Last updated: Dec 15, 2025
Aproximadamente 60%–70% dos casos são causados por mutações que afetam as proteínas dos miofilamentos grossos ou finos dos sarcómeros (componentes contráteis do coração).
Muitos indivíduos afetados pela MCH são assintomáticos ao longo das suas vidas. Para alguns, normalmente durante a adolescência, a morte súbita cardíaca é o 1º sintoma.
Sintomas:
Antecedentes familiares:
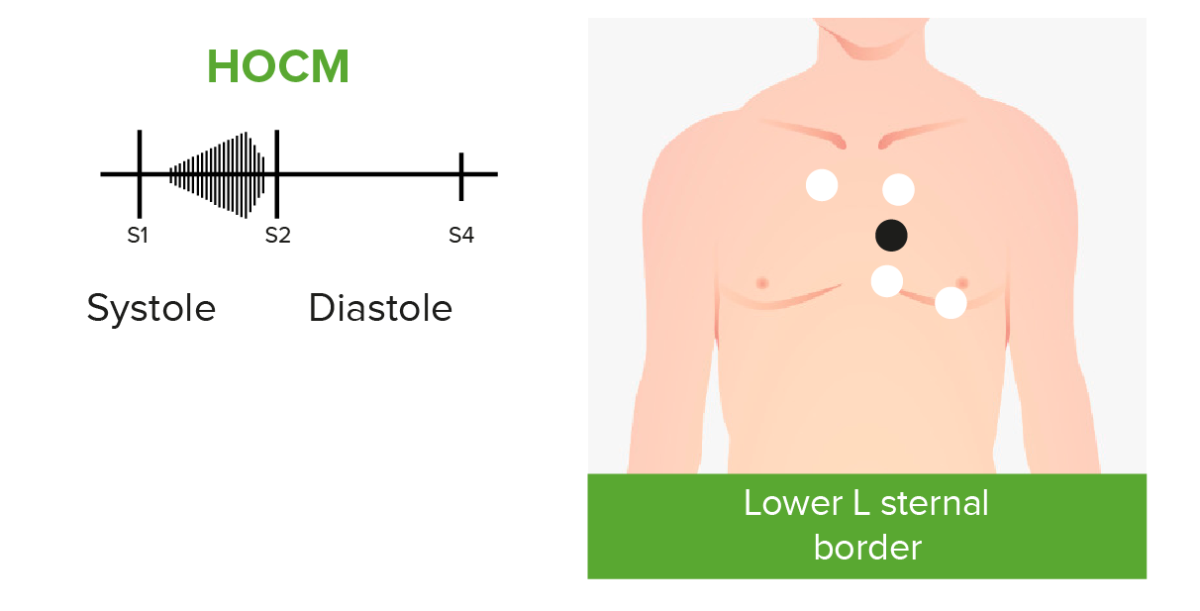
Fonocardiogramas de sons cardíacos anormais causados pela miocardiopatia hipertrófica obstrutiva (MCHO):
Os pacientes com MCHO e obstrução da via de saída do ventrículo esquerdo podem apresentar um sopro sistólico crescendo-decrescendo, mais audível no ápice e no bordo esternal esquerdo inferior.
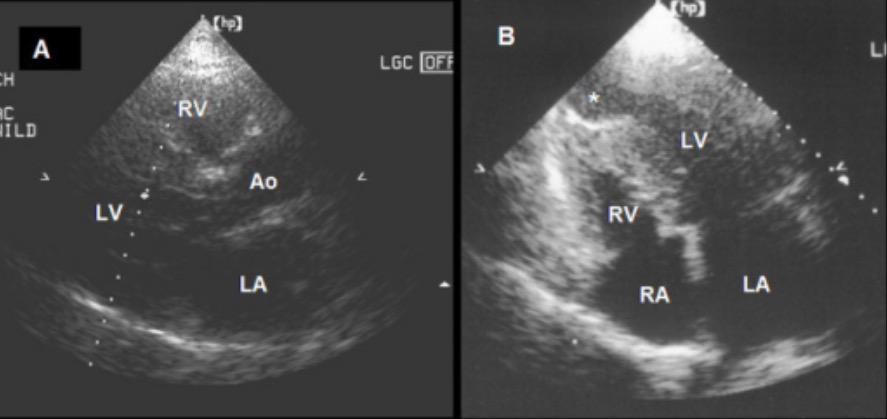
A: Imagem do eixo longo paraesternal que mostra miocardiopatia hipertrófica septal assimétrica na diástole final
B: Uma imagem de 4 câmaras que mostra uma combinação de miocardiopatia hipertrófica basal e médio-ventricular e um aneurisma apical.
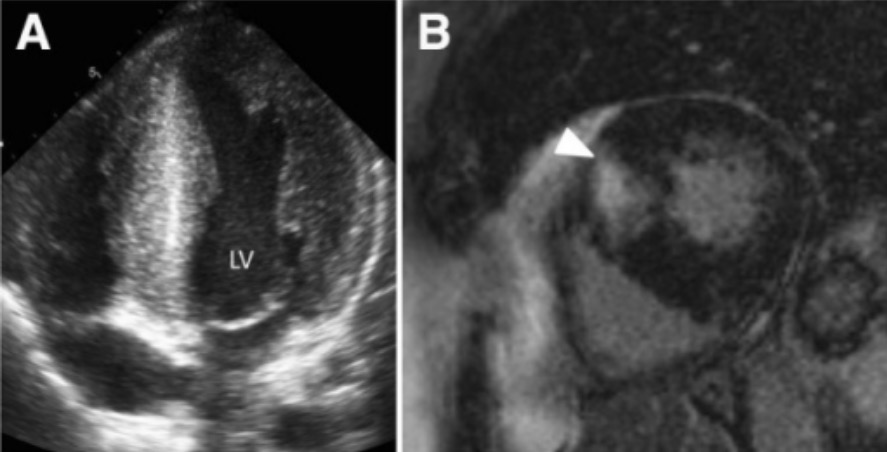
Miocardiopatia hipertrófica: hipertrofia ventricular esquerda (VE) com > 15 mm de espessura das paredes septal e lateral (painel A)
Imagem: “Hypertrophic cardiomyopathy” por Victoria Delgado et al. Licença: CC BY 4.0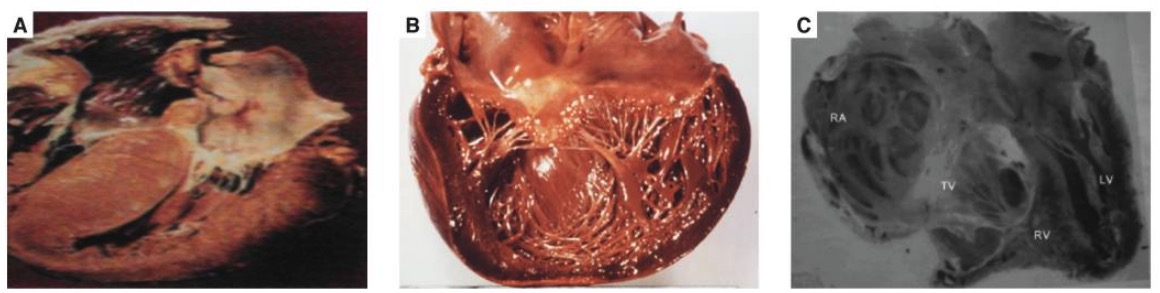
Miocardiopatia hipertrófica
B: miocardiopatia dilatada
C: fibrose endomiocárdica
Não é conhecido nenhum tratamento farmacológico que melhore o prognóstico.
Objetivos do tratamento:
Casos assintomáticos:
No estabelecimento de sintomas de insuficiência cardíaca sem obstrução da via de saída do ventrículo esquerdo:
No quadro de sintomas de insuficiência cardíaca e obstrução da via de saída do ventrículo esquerdo: