O vírus da imunodeficiência humana (VIH), um vírus de RNA de cadeia simples pertencente à família Retroviridae, é o agente etiológico da síndrome da imunodeficiência adquirida (SIDA). O vírus da imunodeficiência humana é uma infeção sexualmente transmissível ou transmitida pelo sangue que ataca células de linfócitos T CD4+, macrófagos e células dendríticas, levando a uma eventual imunodeficiência. A apresentação é marcada por sintomas constitucionais como linfadenopatia e febre. A progressão posterior predispõe a infeções oportunistas e malignidades. O diagnóstico é por imunoensaio enzimático para VIH-1 e VIH-2. Testes adicionais incluem carga viral do VIH, genotipagem e contagem de linfócitos T CD4+ para determinar a terapia e avaliar a resposta ao tratamento e a progressão da doença. É recomendado o tratamento imediato com terapia antirretroviral combinada.
Última atualização: Jun 24, 2025
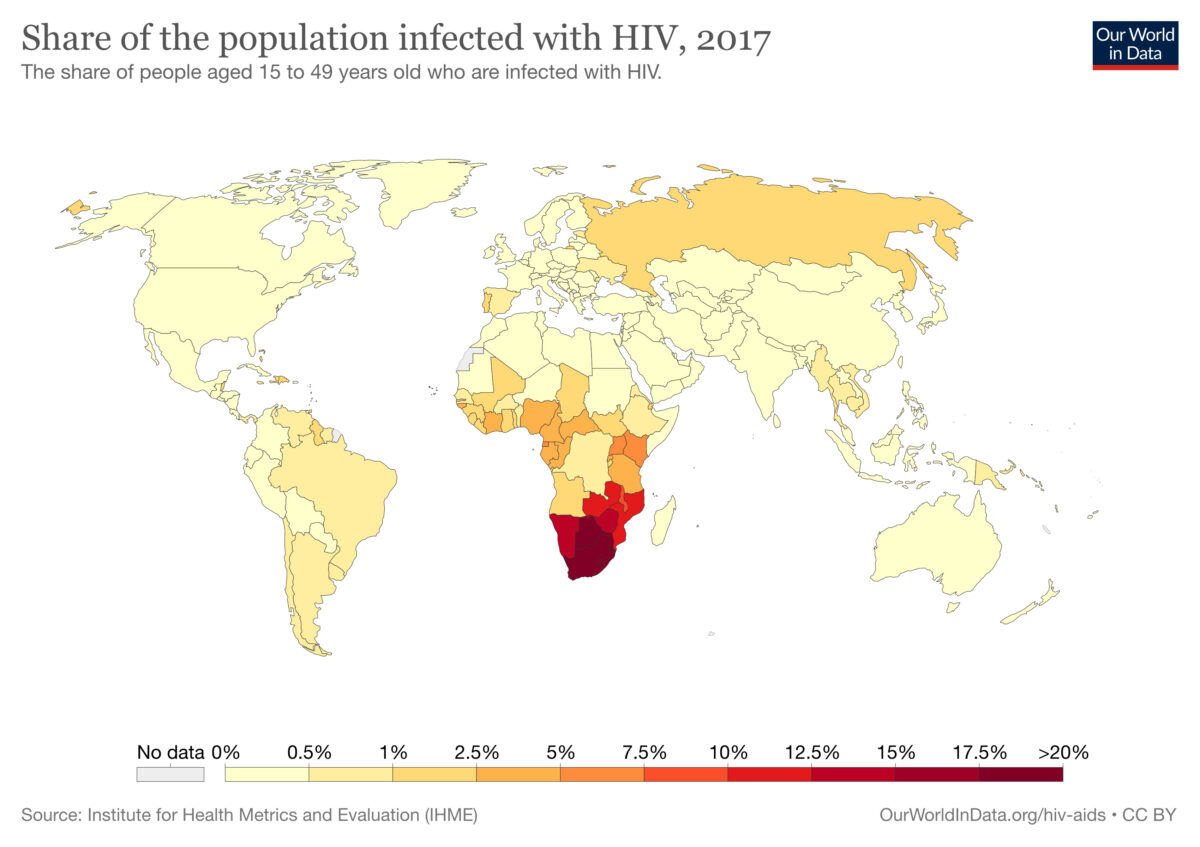
Distribuição mundial de infeções por HIV de 2017 (em pessoas de 15 a 49 anos):
As cores indicam a percentagem da população com infeção pelo vírus da imunodeficiência humana (VIH) em cada país. As informações sobre o percentual correspondente da população (cor designada) estão abaixo do mapa-mundo.
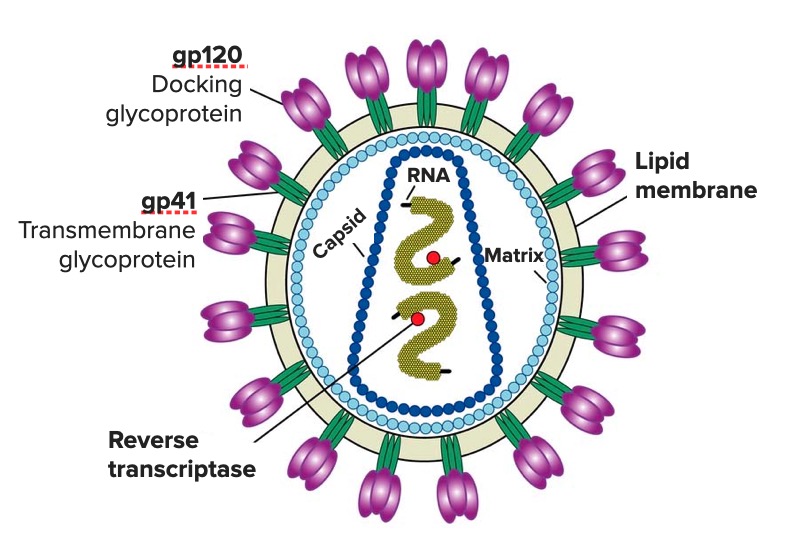
Diagrama do vírus VIH que apresenta a estrutura do seu genoma e as suas principais enzimas e glicoproteínas (gp120 e gp41)
Imagem: “Diagram of the HIV virus” por US National Institute of Health. Licença: Public DomainSexual:
Parenteral:
Vertical:
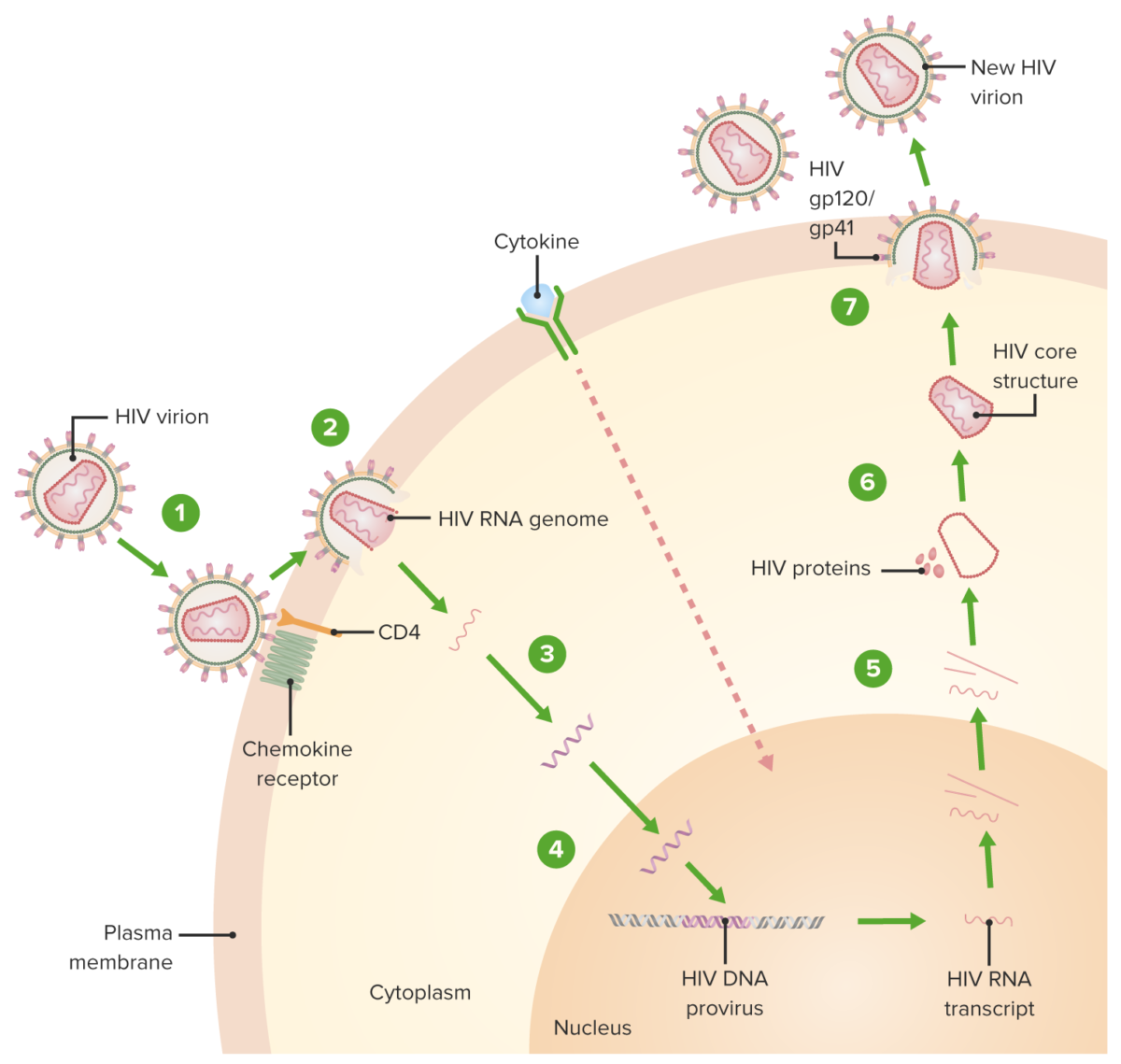
Ciclo de replicação do VIH:
1. O vírion liga-se ao recetor CD4 e a um recetor de quimiocina, seguido por uma mudança conformacional que facilita a fusão do vírion e da célula hospedeira.
2. Um invólucro de proteína do capsídeo (ao redor do RNA viral e proteínas) é não revestido à medida que o vírion atravessa o citoplasma.
3. Ocorre a síntese de DNA pró-viral mediada por transcriptase reversa.
4. O DNA viral é transportado através do núcleo e integrado ao DNA do hospedeiro, facilitado pela integrase.
5. O DNA viral é transcrito e formam-se múltiplas cópias do novo RNA do VIH que são transportadas para o citoplasma. O novo RNA do VIH torna-se o genoma de um novo vírus. Também ocorre a ativação de citocinas da célula.
6. Novo RNA viral + proteínas + enzimas movem-se para a superfície da célula e formam uma partícula não infecciosa.
7. A partícula (RNA viral + proteínas) eventualmente saí da célula hospedeira com o VIH imaturo. A proteína protease viral (enzima) cliva as poliproteínas recém-sintetizadas produzindo um VIH maduro.
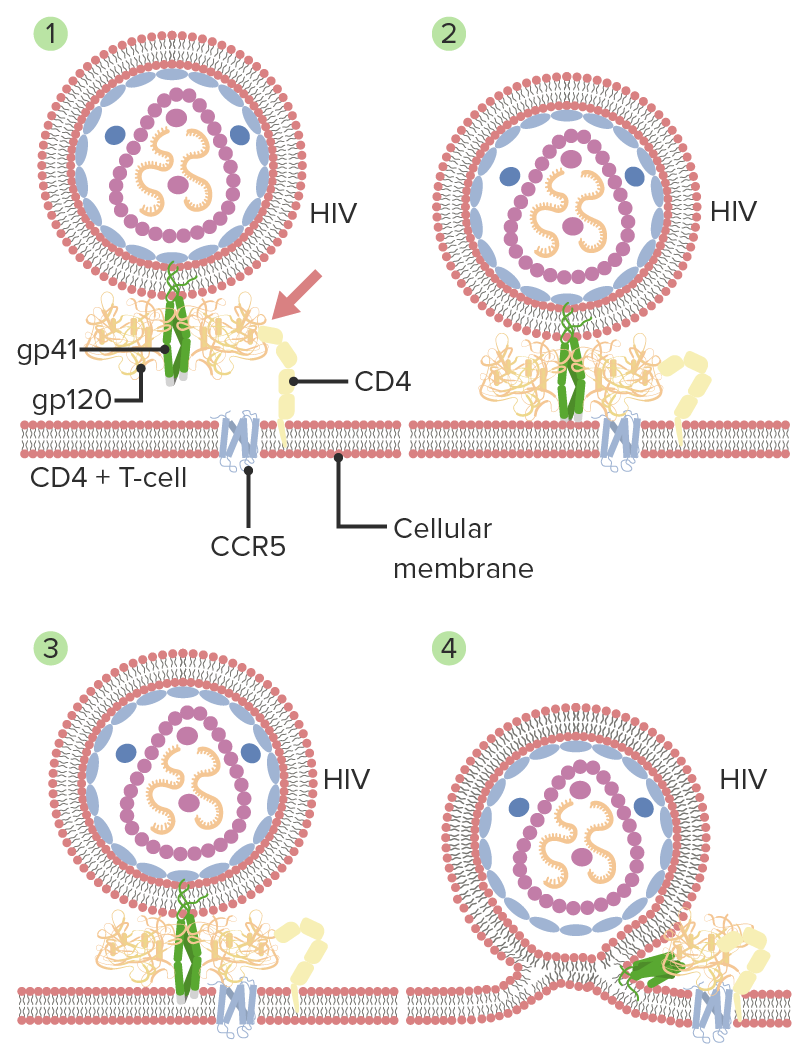
Mecanismo de entrada do VIH e fusão da membrana:
1. VIH Gp120 interage com CD4 (célula hospedeira).
2. Segue-se uma interação secundária com outro recetor CCR5, com uma mudança conformacional na gp120.
3. As pontas da gp41 são inseridas na membrana celular.
4. Gp41 dobra-se ao meio e forma “bobinas” enroladas. As membranas viral e celular unem-se, levando à fusão.
Fase aguda (infeção, disseminação, síndrome retroviral):
Fase crónica/latência clínica:
SIDA:
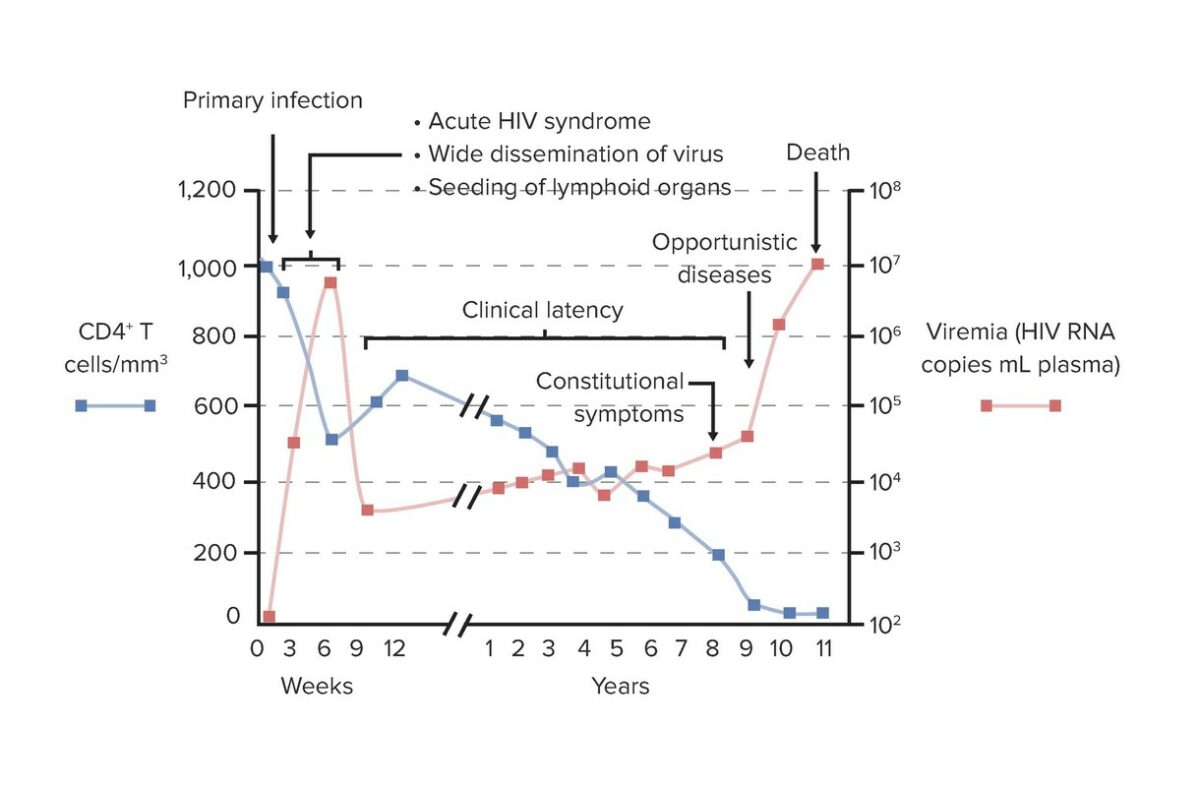
Gráfico da relação entre contagem de células T CD4+ e carga viral durante o curso clínico da infeção pelo VIH e SIDA:
Na infeção primária/aguda (infeção inicial, disseminação e síndrome retroviral aguda), observa-se um aumento da carga viral (viremia) com diminuição das células T CD4+. Este período dura semanas. No período de latência clínica, ocorre replicação viral de baixo nível, mas sustentada, e é observado o declínio gradual das células CD4+. A progressão para SIDA é o resultado da falha das defesas do hospedeiro, com a depleção de células T CD4+ e aumento da carga viral. Este processo predispõe a infeções oportunistas.
A classificação dos Centros de Controlo e Prevenção de Doenças (CDC, pela sigla em inglês) observa que a contagem de linfócitos T CD4 + é:
| Categorias/estadio de células T CD 4+ | 1 | 2 | 3 |
|---|---|---|---|
| Categorias clínicas | CD4+ ≥ 500 células/µL | CD4+ 200–499 células/µL | CD4+ <200 células/µL* |
| A: Assintomático, VIH agudo, linfadenopatia persistente | A1 | A2 | A3 |
| B: Sintomático, não A ou C | B1 | B2 | B3 |
| C: SIDA, incluindo infeções oportunistas, doenças neurológicas e tumores | C1 | C2 | C3 |
Síndrome retroviral aguda (fase aguda):
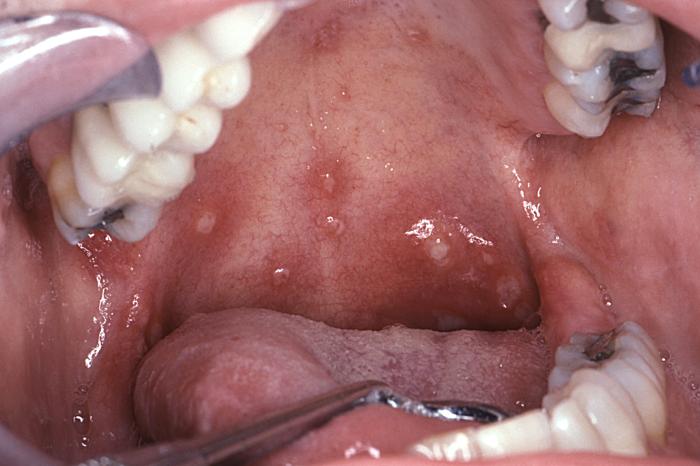
Estomatite aftosa típica da síndrome retroviral aguda
Imagem : “6055” por CDC/ Sol Silverman, Jr., DDS. Licença: Public Domain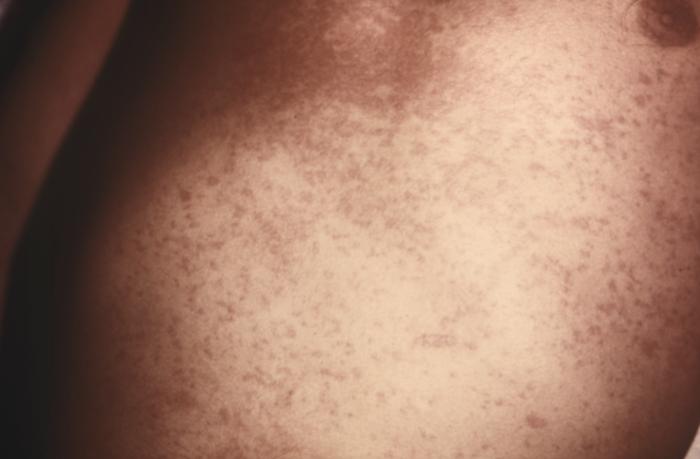
Exantema maculopapular viral visto na síndrome retroviral aguda
Imagem : “14925” por CDC/Dr. Gavin Hart. Licença: Public DomainInfeção crónica (latência clínica):
SIDA:
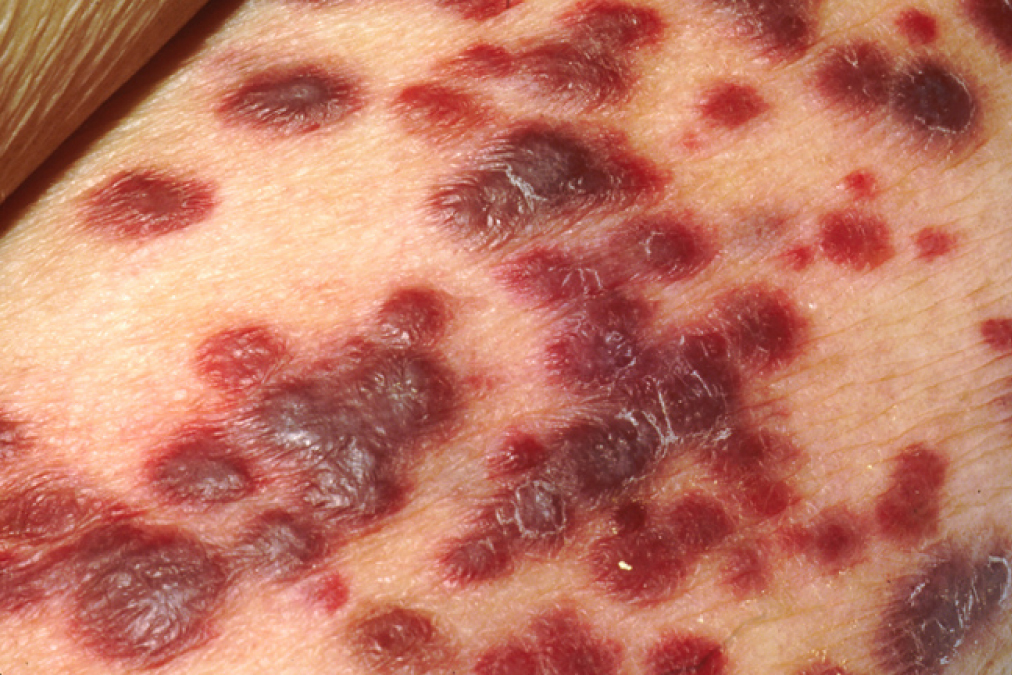
Lesões cutâneas do sarcoma de Kaposi
Imagem: “Kaposi’s sarcoma” por OpenStax College. Licença: CC BY 3.0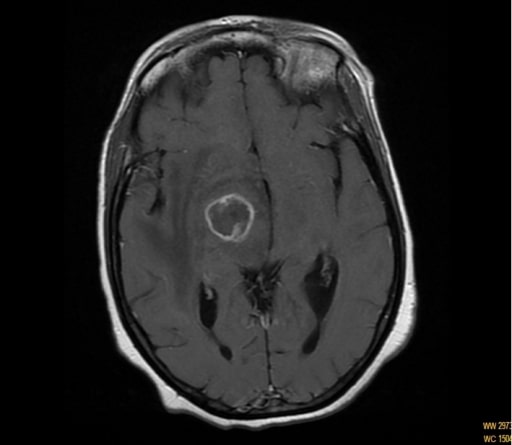
Toxoplasmose e SIDA:
Ressonância magnética (RM) mostrando realce do anel da lesão cápsula-talâmica num paciente com hemicoréia-hemibalismo
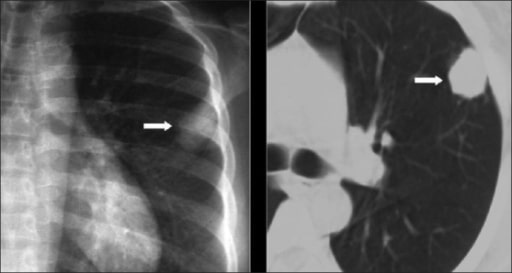
Criptococose:
Radiografia de tórax e tomografia computadorizada (TC) mostram um nódulo pulmonar solitário. O diagnóstico de criptococose foi confirmado por biópsia.

Complexo Mycobacterium avium : Um homem com VIH avaliado por dor abdominal superior severa do lado direito. Apesar do tratamento, desenvolveu um abcesso gânglio linfático supraclavicular aumentado. Aspirado revelou MAC.
Imagem : “Left supraclavicular abscessed lymph node” por Department of Internal Medicine, Division of Infectious Diseases, University of Michigan Health System, Ann Arbor, Michigan, USA. Licença: CC BY 2.0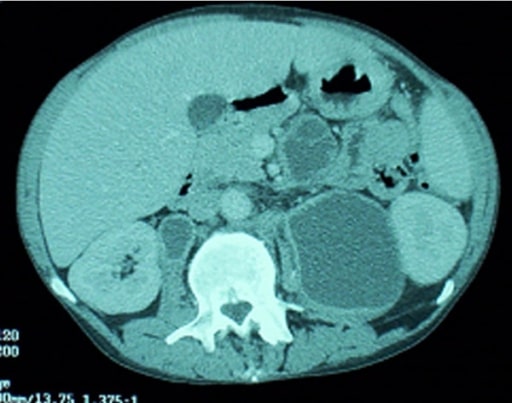
Complexo Mycobacterium avium :
Um homem com VIH avaliado por dor abdominal superior severa do lado direito. Uma TC abdominal revelou múltiplos gânglios linfáticos intra-abdominais necróticos aumentados.
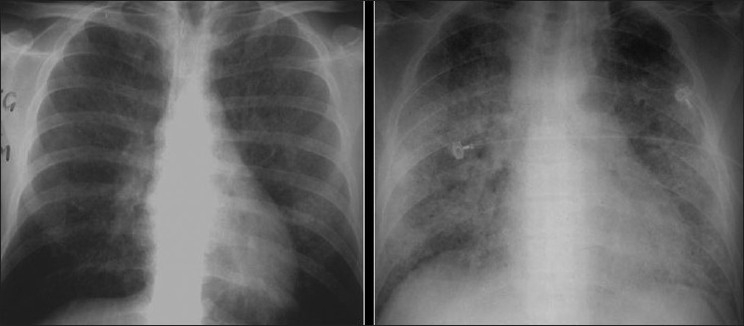
Pneumonia por Pneumocystis:
2 radiografias de tórax mostram aspecto em vidro fosco. Os achados da radiografia de tórax à direita mimetizam edema pulmonar.
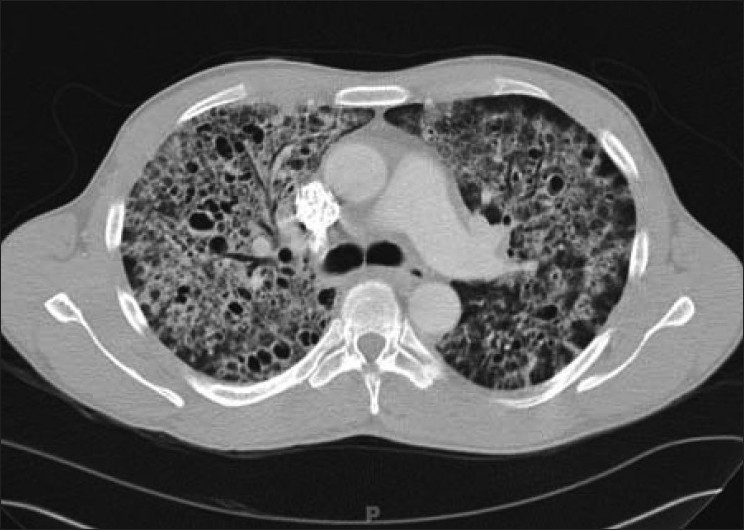
TC de tórax que mostra a marca registada da pneumonia por Pneumocystis num cenário clínico de comprometimento imunológico:
Observar a atenuação em vidro fosco com distribuição geográfica ou em mosaico.
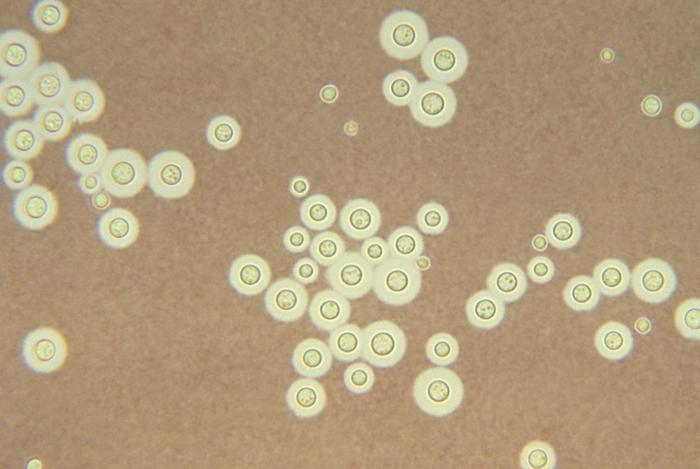
Montagem em tinta da Índia de cryptococcus:
Observar a cápsula ao redor da levedura a brotar.
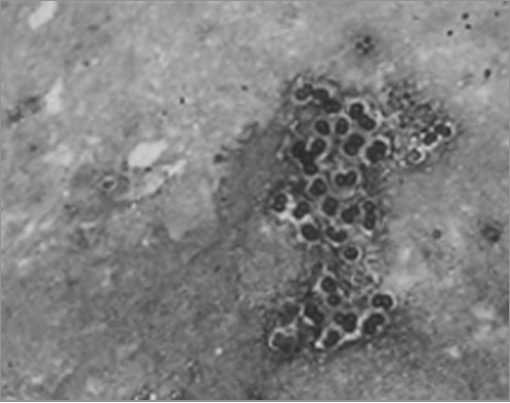
P. jiroveci :
Coloração com prata metenamina que demonstra aglomerados de quistos de P. jiroveci na expetoração
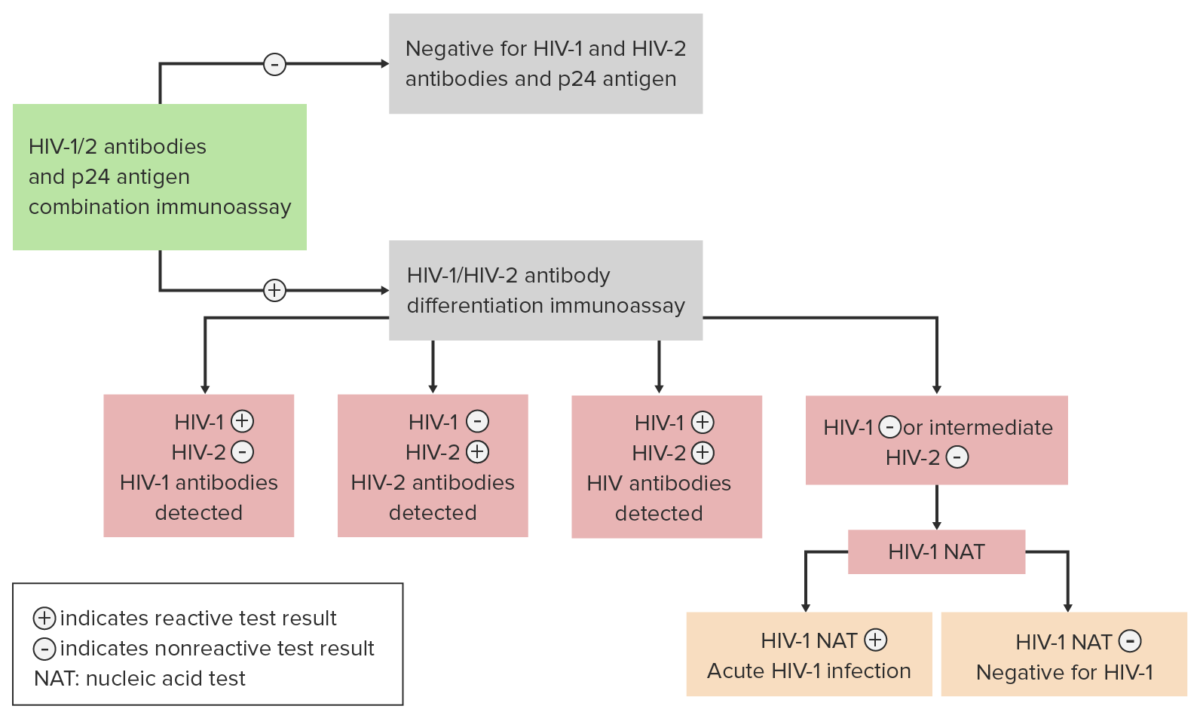
Algoritmo para o diagnóstico e diferenciação entre uma infeção por VIH pelo subtipo VIH-1 e subtipo VIH-2
Imagem por Lecturio.| Estadio | <1 ano | 1-5 anos | ≥ 6 anos |
|---|---|---|---|
| 0 | N / D | N / D | N / D |
| 1 | ≥ 1.500 células/µL | ≥ 1.000 células/µL | ≥ 500 células/µL |
| 2 | 750–1.499 células/µL | 500–999 células/µL | 200–499 células/µL |
| 3 (SIDA) | <750 células/µL | <500 células/µL | <200 células/µL |