El virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology de la inmunodeficiencia humana (VIH), un virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology de ARN monocatenario perteneciente a la familia Retroviridae Retroviridae The human immunodeficiency virus (HIV) is a species of Lentivirus, a genus of the family Retroviridae, which causes HIV infections and acquired immunodeficiency syndrome (AIDS). The virus has high genetic variability and is divided into 2 major types, HIV type 1 (HIV-1) and HIV type 2 (HIV-2). The human immunodeficiency virus is a single-stranded, positive-sense, enveloped RNA virus, which targets and destroys WBCs, leading to frequent opportunistic infections and, eventually, death. Human Immunodeficiency Virus (HIV) , es el agente etiológico del síndrome de inmunodeficiencia adquirida (SIDA). El virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology de la inmunodeficiencia humana es una infección de transmisión sexual o transmitida por la sangre que ataca a los LOS Neisseria linfocitos T CD4+, los LOS Neisseria macrófagos y las células dendríticas, lo que conduce a una posible inmunodeficiencia. La presentación está marcada por síntomas constitucionales como linfadenopatía y fiebre. Una mayor progresión predispone a infecciones oportunistas y neoplasias malignas. El diagnóstico se realiza mediante inmunoensayo enzimático para VIH-1 y -2. Las pruebas adicionales incluyen la carga viral del VIH, el genotipado y el recuento de linfocitos T CD4+ para determinar la terapia y evaluar la respuesta al AL Amyloidosis tratamiento y la progresión de la enfermedad. Se recomienda el tratamiento inmediato con terapia antirretroviral combinada.
Last updated: Jun 24, 2025
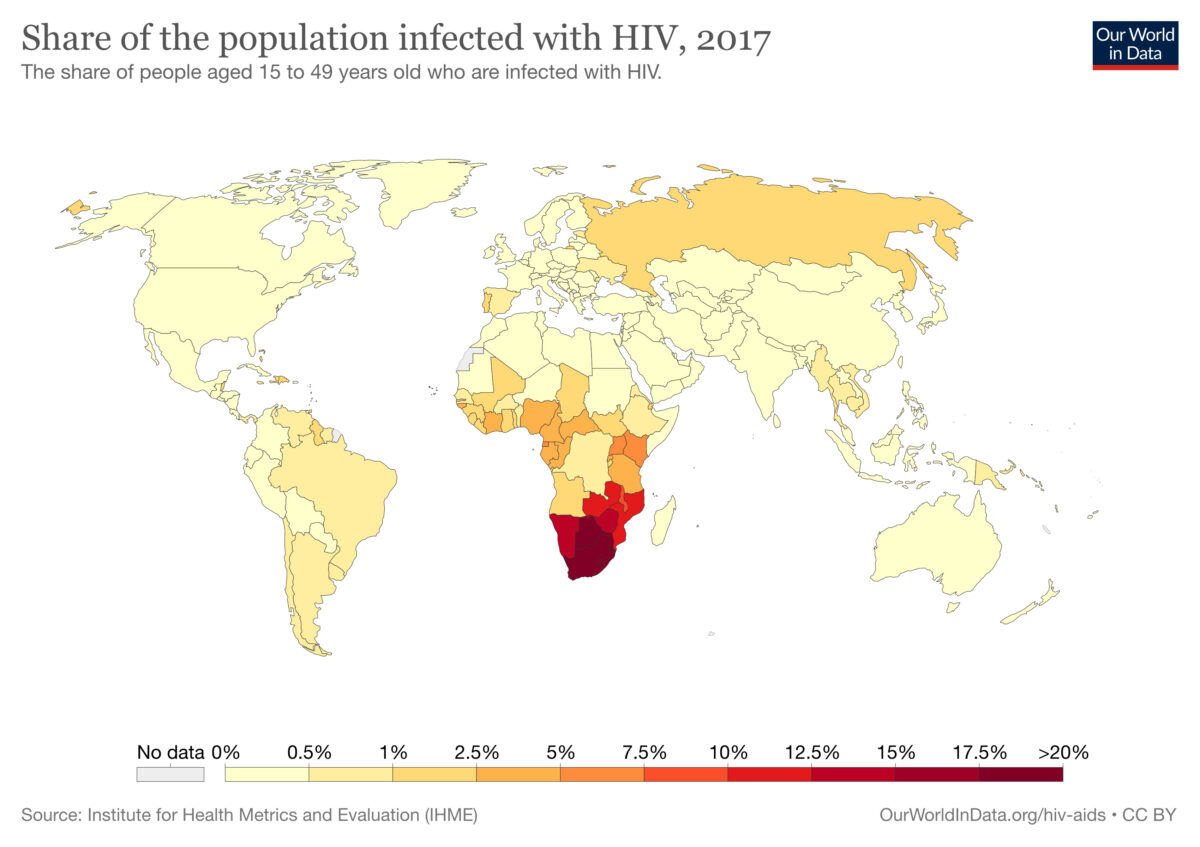
Mapa mundial de infecciones por VIH en 2017 (en personas de 15 a 49 años):
Los colores indican el porcentaje de población con infección por el virus de la inmunodeficiencia humana (VIH) en cada país. La información sobre el porcentaje de población correspondiente (color designado) se encuentra debajo del mapa mundial.
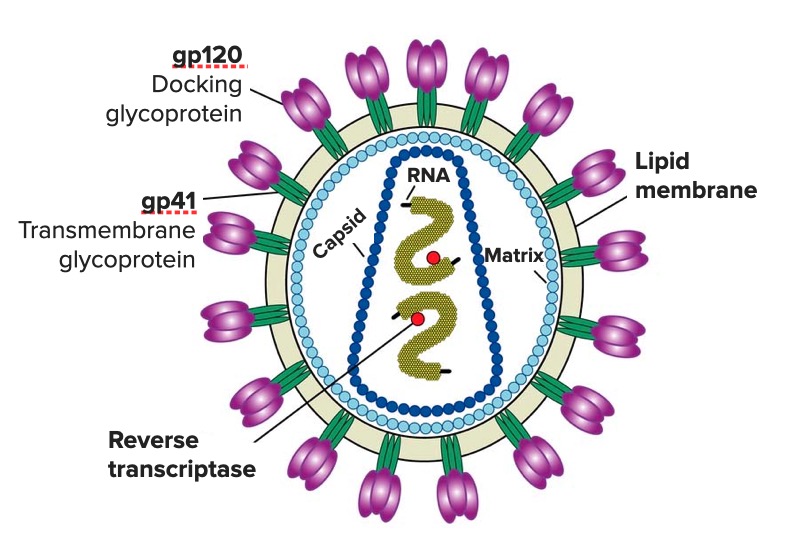
Diagrama del virión del VIH con la estructura de su genoma y sus principales enzimas y glicoproteínas (gp120 y gp41)
Imagen: “Diagram of the HIV virus” por el US National Institute of Health. Licencia: Dominio PúblicoSexual:
Parenteral:
Vertical:
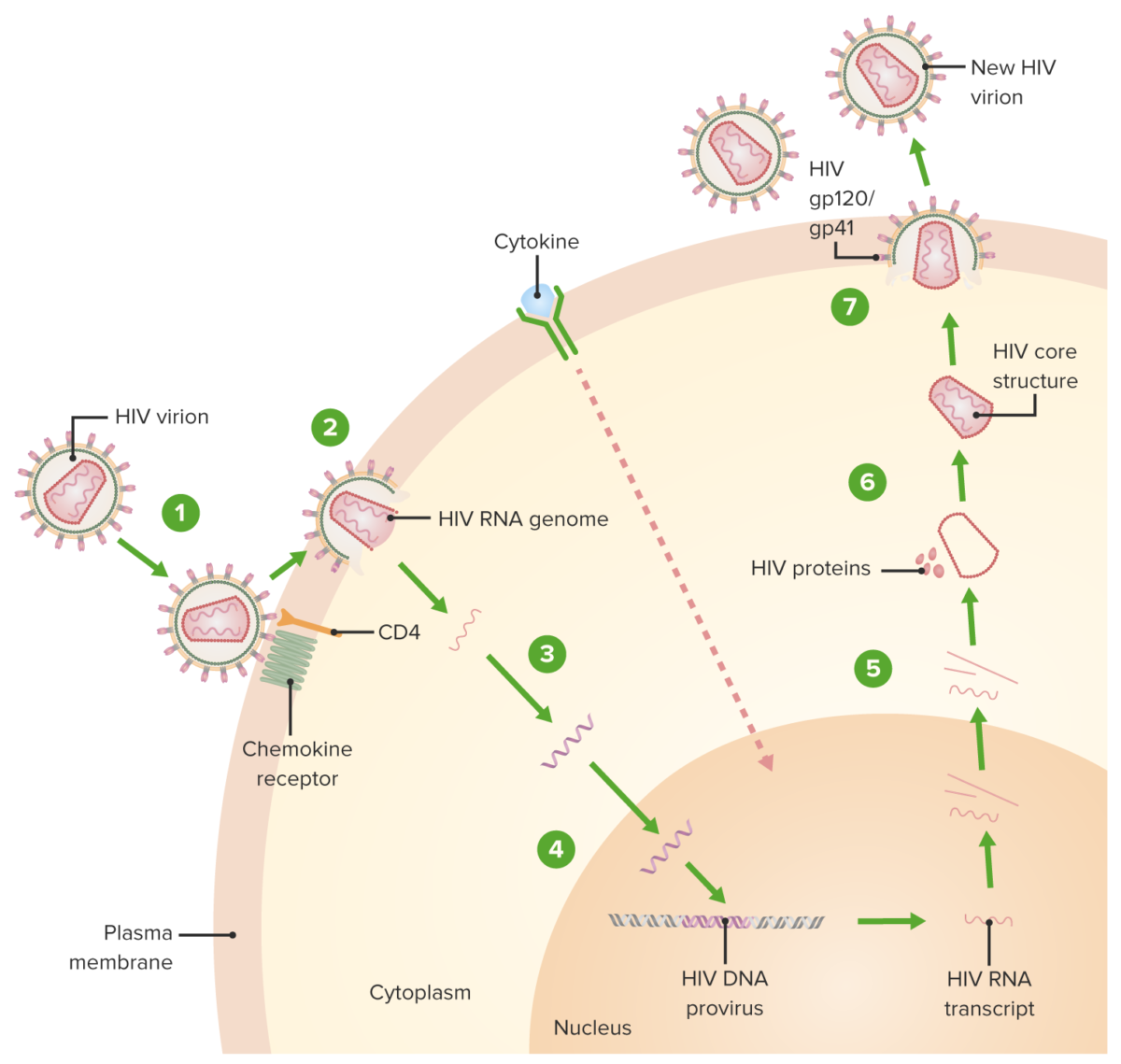
Ciclo de replicación del VIH:
1. El virión se une al receptor CD4 y un receptor de quimioquinas, seguido de un cambio conformacional que facilita la fusión del virión y la célula huésped.
2. Una capa de proteína de la cápside (que rodea el ARN y las proteínas virales) queda sin recubrimiento a medida que el virión atraviesa el citoplasma.
3. Se produce la síntesis de ADN proviral mediada por transcriptasa inversa.
4. El ADN viral se transporta a través del núcleo y se integra en el ADN del huésped, facilitado por la integrasa.
5. Se transcribe el ADN viral y se forman y transportan múltiples copias del nuevo ARN del VIH al citoplasma. El nuevo ARN del VIH se convierte en el genoma de un nuevo virus. También se produce la activación de citocinas de la célula.
6. El nuevo ARN viral + proteínas + enzimas se mueven a la superficie celular y forman una partícula no infecciosa.
7. Las partículas (ARN viral + proteínas) eventualmente brotan de la célula huésped con el VIH inmaduro. La proteína viral proteasa (enzima) luego escinde poliproteínas recién sintetizadas produciendo un VIH maduro.
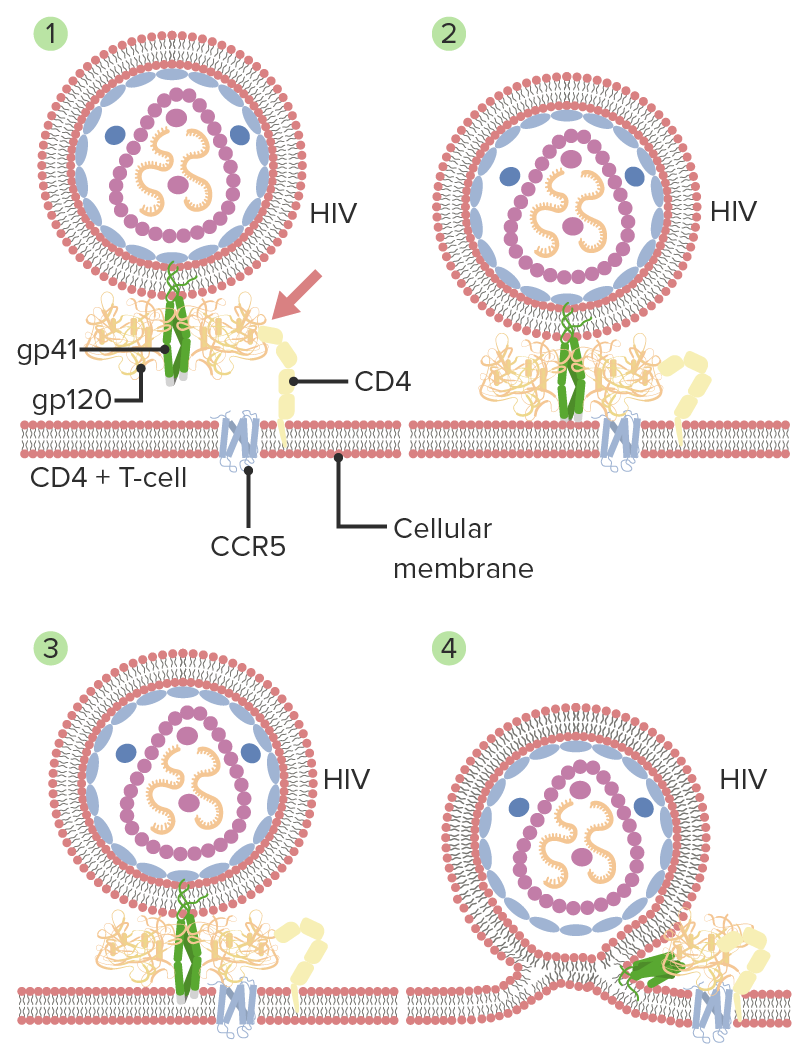
Mecanismo de entrada del VIH y fusión de membranas:
1. Gp120 del VIH interactúa con CD4 (célula huésped).
2. Sigue una interacción secundaria con otro receptor CCR5, con un cambio conformacional en gp120.
3. Las puntas de gp41 se insertan en la membrana celular.
4. Gp41 se pliega por la mitad y forma bobinas enrolladas. Las membranas virales y celulares se unen, lo que lleva a la fusión.
Fase aguda (infección, diseminación, síndrome retroviral):
Fase crónica/latencia clínica:
SIDA:
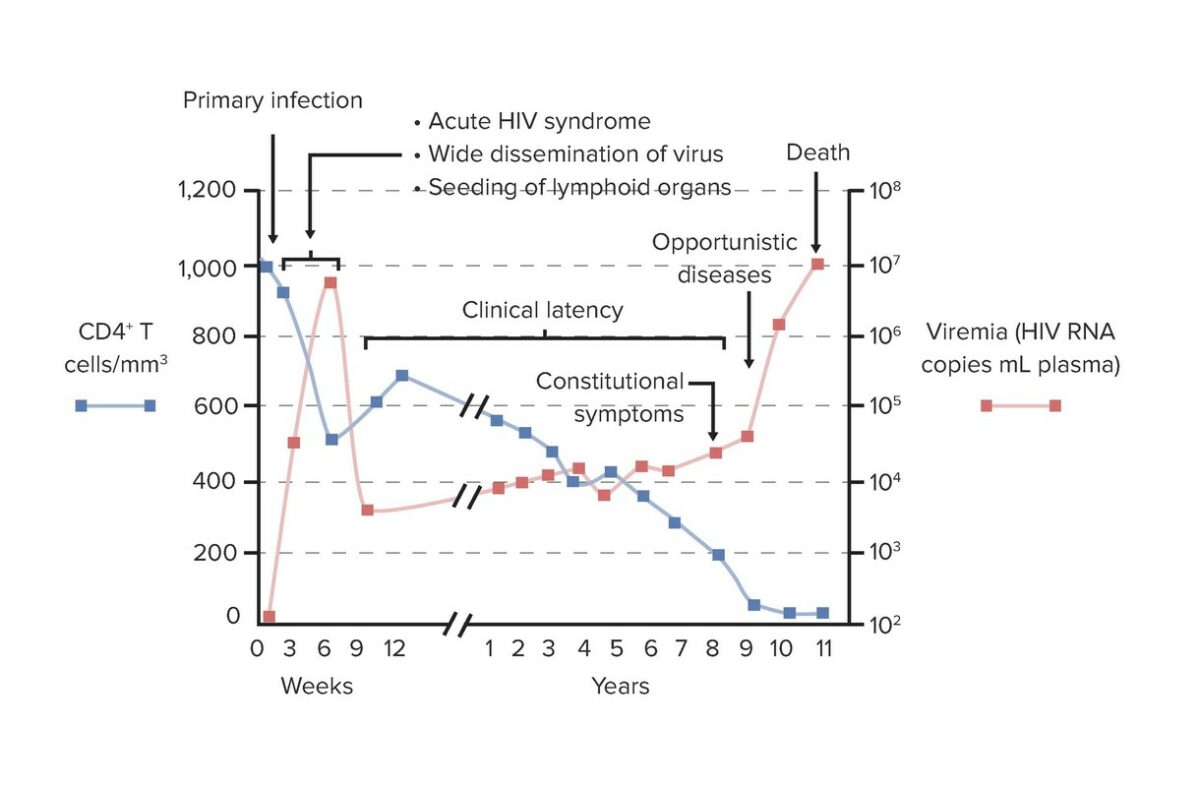
Gráfico de la relación entre el recuento de linfocitos T CD4+ y la carga viral durante el curso clínico de la infección por VIH y SIDA:
En la infección primaria/aguda (infección inicial, diseminación y síndrome retroviral agudo), se observa un aumento de la carga viral (viremia) con disminución de los linfocitos T CD4+. Este período dura semanas. En el período de latencia clínica, se produce una replicación viral de bajo nivel, pero sostenida, y se observa una disminución gradual de los linfocitos CD4+. La progresión al SIDA es el resultado de la descomposición de las defensas del huésped, con linfocitos T CD4+ agotados y carga viral en aumento. Este proceso predispone a infecciones oportunistas.
La clasificación de los LOS Neisseria Centros para el Control y la Prevención de Enfermedades (CDC por sus siglas en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum inglés) señala que el recuento de linfocitos T CD4+ es:
| Categorías/etapa de linfocitos T CD 4+ | 1 | 2 | 3 |
|---|---|---|---|
| Categorías clínicas | CD4+ ≥ 500 células/µL | CD4+ 200–499 células/µL | CD4+ <200 células/µL* |
| A: asintomático, VIH agudo, linfadenopatía persistente | A1 | A2 | A3 |
| B: sintomático, no A o C | B1 | B2 | B3 |
| C: SIDA, incluidas infecciones oportunistas, enfermedades neurológicas y tumores | C1 | C2 | C3 |
Síndrome retroviral agudo (fase aguda):
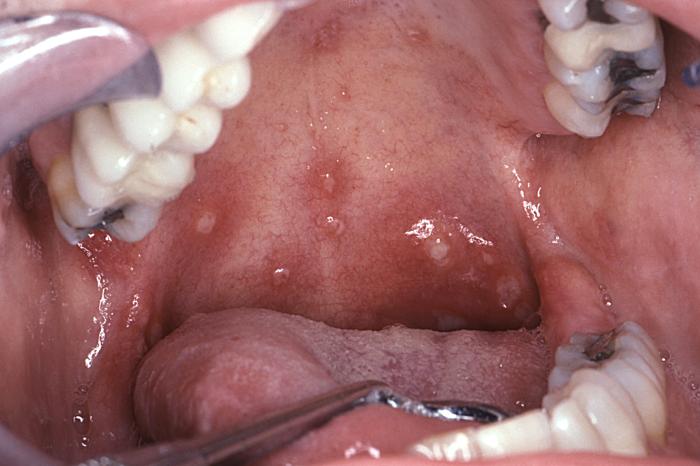
Estomatitis aftosa típica de la que se observa en el síndrome retroviral agudo
Imagen: “6055” por CDC/ Sol Silverman, Jr., DDS. Licencia: Dominio Público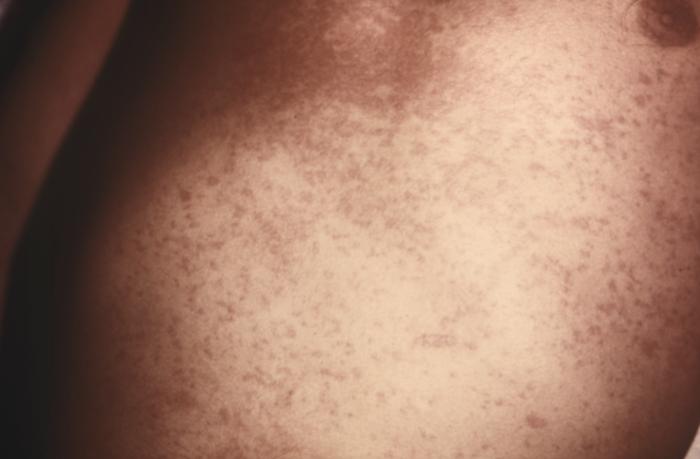
Exantema maculopapular viral observado en el síndrome retroviral agudo
Imagen: “14925” por CDC/ Dr. Gavin Hart. Licencia: Dominio PúblicoInfección crónica (latencia clínica):
SIDA:
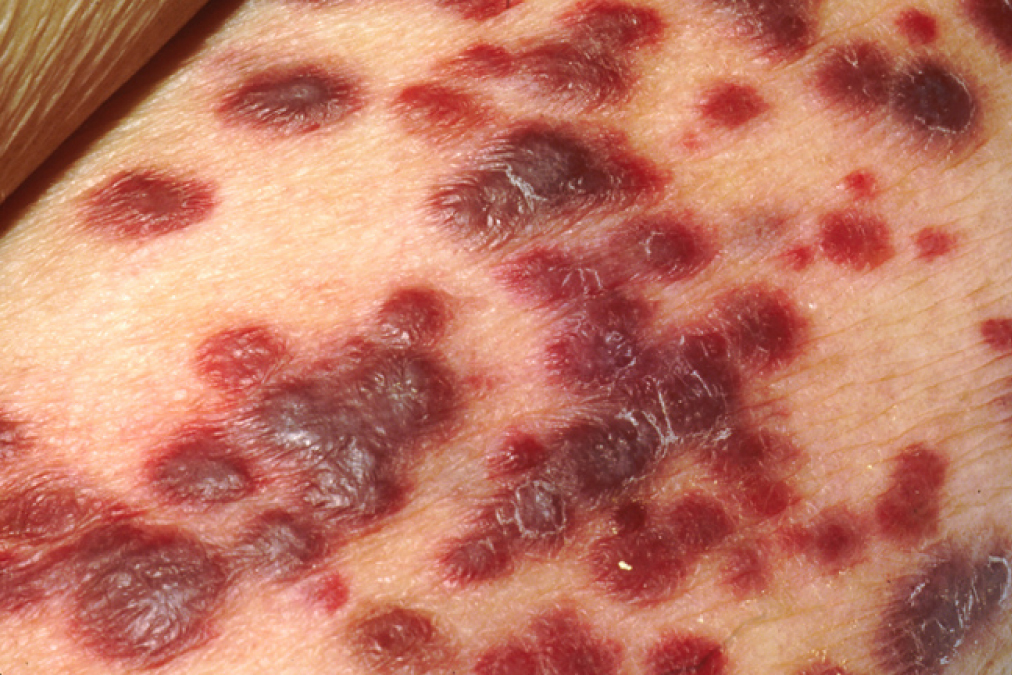
Lesiones cutáneas del sarcoma de Kaposi
Imagen: “Kaposi‘s sarcoma” por OpenStax College. Licencia: CC BY 3.0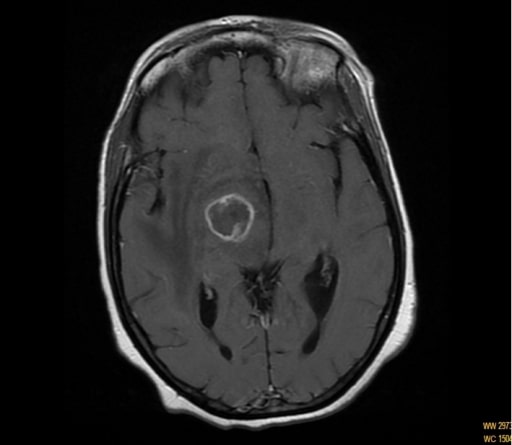
Toxoplasmosis y SIDA:
Imágenes por resonancia magnética (RM) que muestran realce en anillo de la lesión de la cápsula talámica en un paciente con hemicorea-hemibalismo
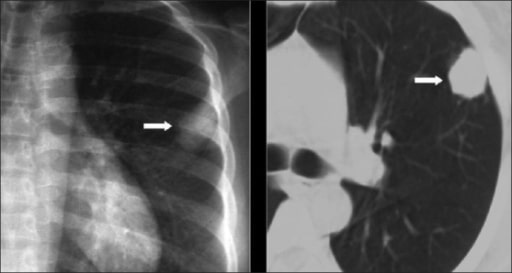
Criptococosis:
La radiografía de tórax y la tomografía computarizada (TC) muestran un nódulo pulmonar solitario. El diagnóstico de criptococosis se confirmó mediante biopsia.

Complejo Mycobacterium avium: Un hombre con VIH evaluado por dolor severo en el lado derecho del abdomen superior. A pesar del tratamiento, desarrolló un absceso de ganglio linfático supraclavicular aumentado de tamaño. Aspirado reveló MAC.
Imagen: “Left supraclavicular abscessed lymph node” por el Departamento de Medicina Interna, División de Enfermedades Infecciosas, Sistema de Salud de la Universidad de Michigan, Ann Arbor, Michigan, EE. UU. Licencia: CC BY 2.0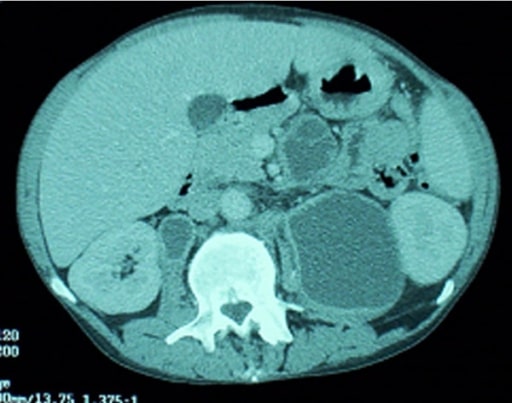
Complejo Mycobacterium avium:
Un hombre con VIH evaluado por dolor abdominal superior severo en el lado derecho. Una tomografía computarizada abdominal reveló múltiples ganglios linfáticos intraabdominales necróticos agrandados.
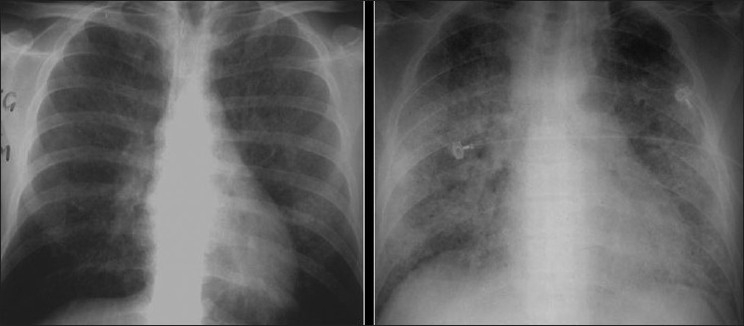
Neumonía por Pneumocistis:
2 radiografías de tórax muestran apariencia de vidrio esmerilado. Los hallazgos de la radiografía de tórax derecho simulan edema pulmonar.
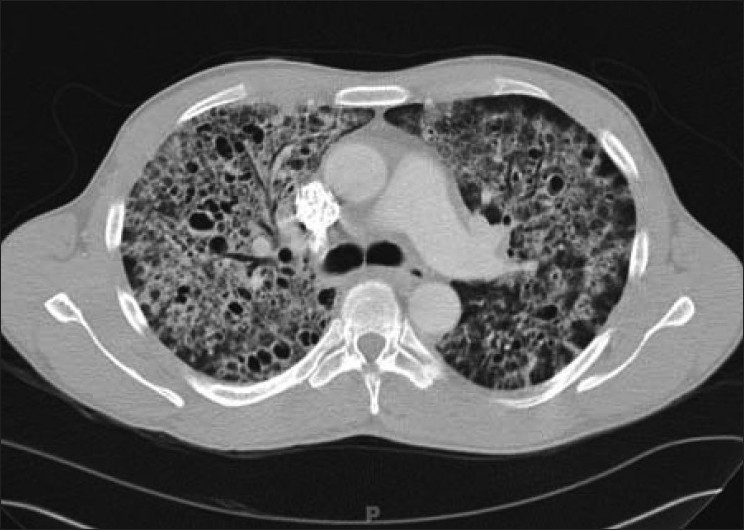
TC de tórax que muestra el sello distintivo de la neumonía por Pneumocystis en un entorno clínico de compromiso inmunitario:
Tenga en cuenta la atenuación en vidrio esmerilado con una distribución geográfica o de mosaico.
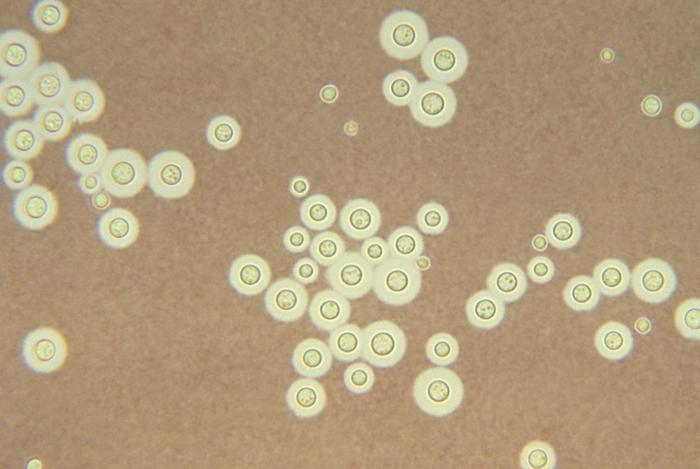
Montaje de tinta india de Cryptococcus:
Tenga en cuenta la cápsula que rodea la levadura en ciernes.
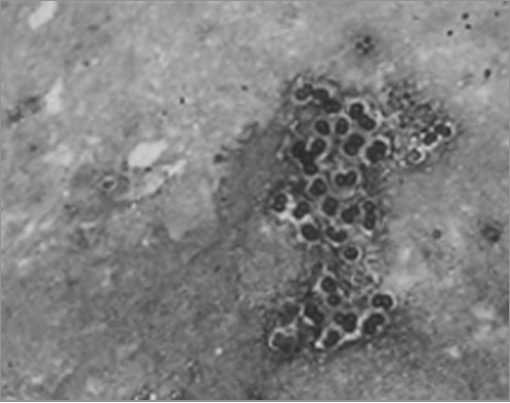
P. jiroveci:
Tinción de plata con metenamina que demuestra grupos de quistes de P. jiroveci en el esputo
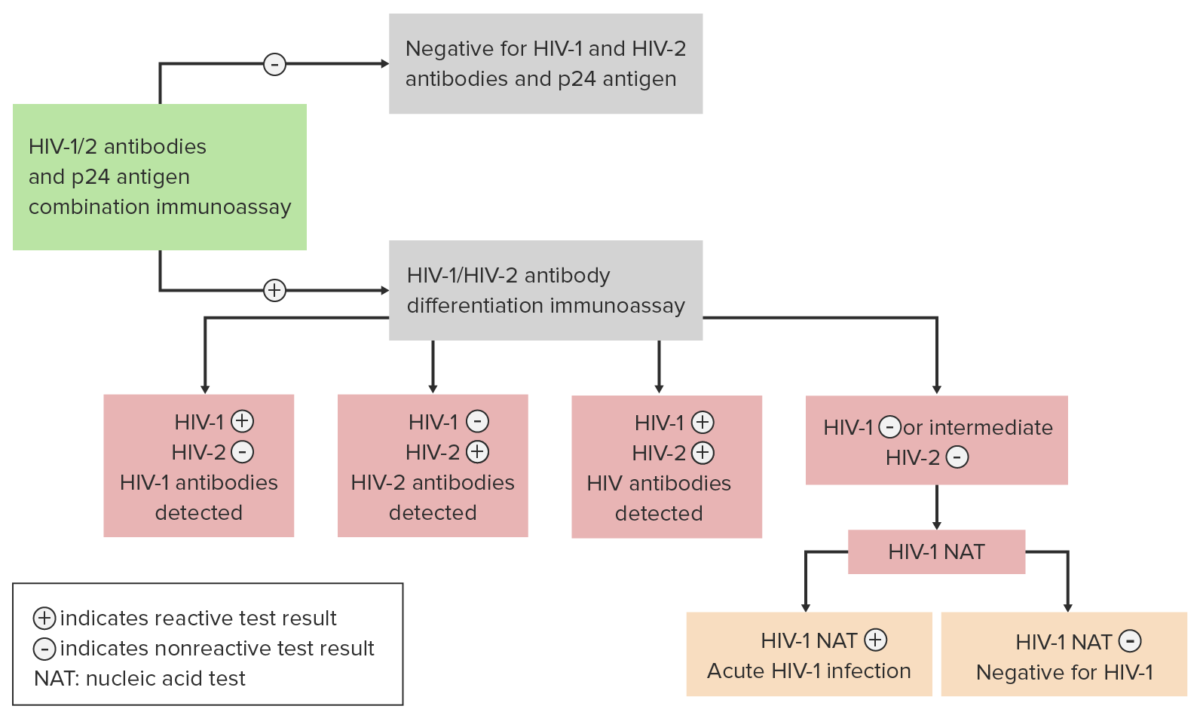
Algoritmo para el diagnóstico y diferenciación entre una infección por VIH producida por el subtipo VIH-1 y el subtipo VIH-2
Imagen por Lecturio.| Etapa | < 1 año | 1–5 años | ≥ 6 años |
|---|---|---|---|
| 0 | N / A | N / A | N / A |
| 1 | ≥ 1500 células/µL | ≥ 1000 células/µL | ≥ 500 células/µL |
| 2 | 750–1499 células/µL | 500–999 células/µL | 200–499 células/µL |
| 3 (SIDA) | < 750 células/µL | < 500 células/µL | < 200 células/µL |