As estatinas são inibidores competitivos da HMG-CoA redutase no fígado. A HMG-CoA redutase é a etapa limitante no processo da síntese do colesterol. A inibição provoca diminuição da formação de colesterol intra-hepatocitário, resultando na regulação positiva dos recetores de LDL e, consequentemente, na redução dos níveis séricos de LDL e triglicerídeos. As estatinas podem diminuir o LDL em 20%–60% (dependendo da sua potência) e apresentam benefícios independentes do colesterol (e.g., diminuição da inflamação vascular e estabilização da placa aterosclerótica). As indicações para o uso de estatinas incluem a prevenção de doença cardiovascular primária ou secundária em pacientes com dislipidemia. Os principais efeitos adversos incluem o aumento das transaminases Transaminases A subclass of enzymes of the transferase class that catalyze the transfer of an amino group from a donor (generally an amino acid) to an acceptor (generally a 2-keto acid). Most of these enzymes are pyridoxyl phosphate proteins. Autoimmune Hepatitis e a toxicidade muscular.
Last updated: Dec 15, 2025
As estatinas são inibidores competitivos da enzima HMG-CoA redutase, que é a etapa limitante na biossíntese do colesterol no fígado.
As estatinas são análogos estruturais da HMG-CoA.
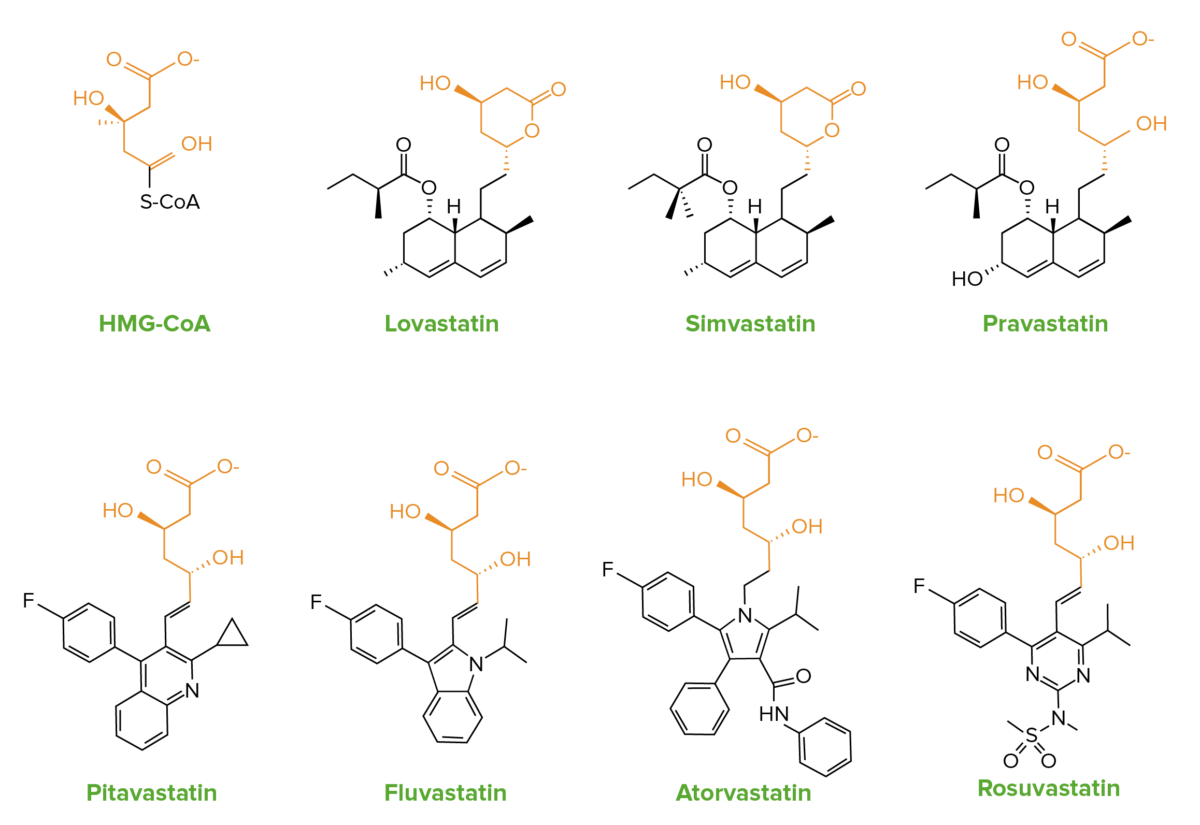
As semelhanças na estrutura química das estatinas com a HMG-CoA:
A lovastatina e a sinvastatina contêm um anel de lactona inativo, que é hidrolisado no organismo para a forma ativa.
Fisiologia normal:
Estatinas:
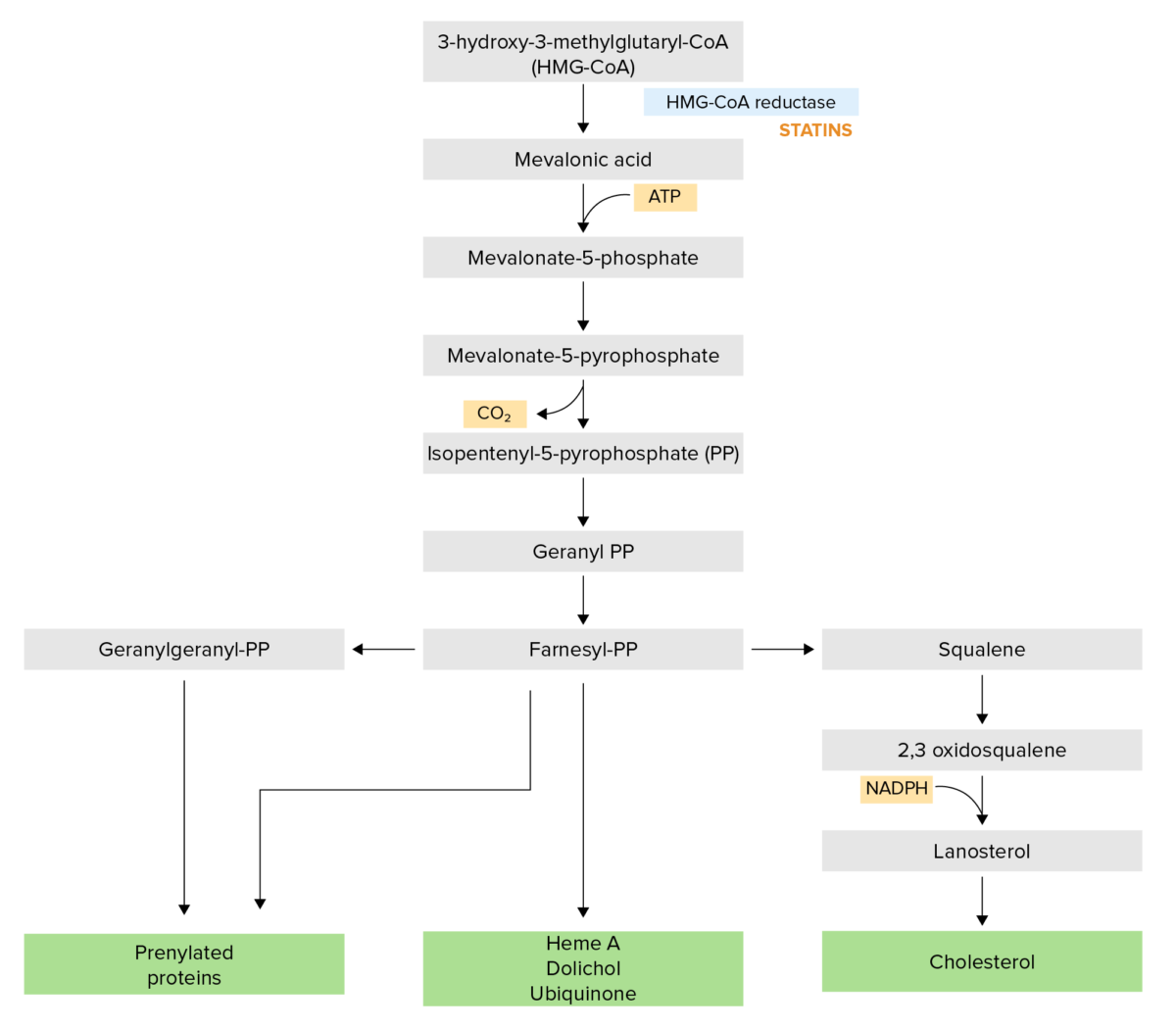
A via da síntese do colesterol:
As estatinas inibem competitivamente a HMG-CoA redutase, que é uma etapa limitante na síntese do colesterol.
NADPH: fosfato de dinucleótido de nicotinamida e adenina
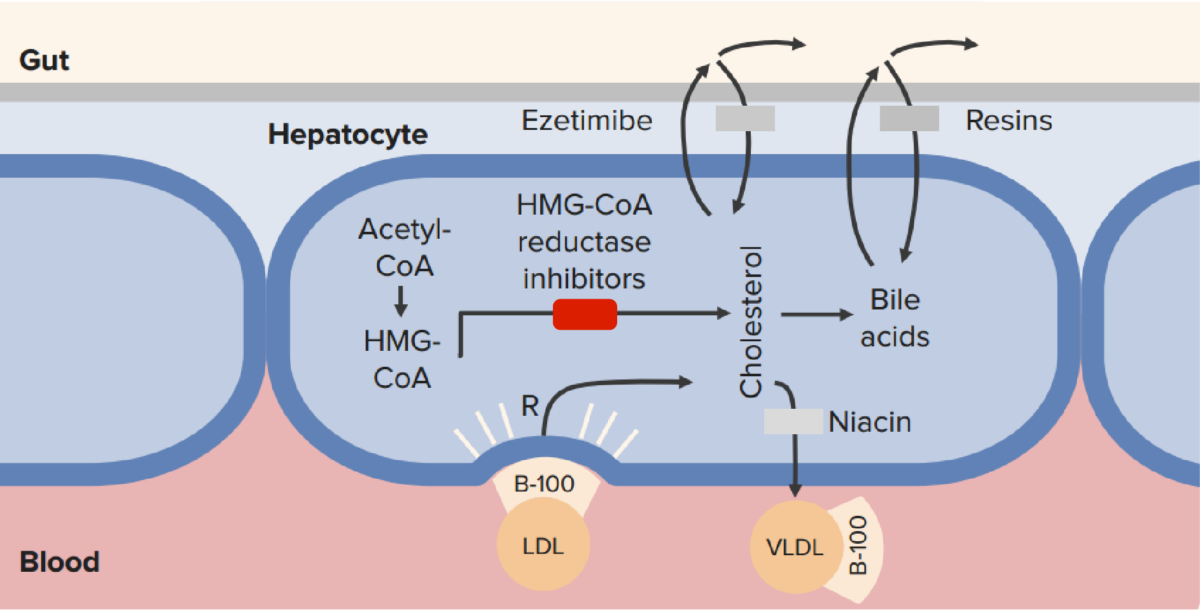
O mecanismo de ação das estatinas (inibidores da HMG-CoA redutase) em comparação com outros tratamentos hipolipemiantes:
As estatinas bloqueiam a síntese intra-hepatocitária de colesterol, resultando na regulação positiva dos recetores de LDL e na redução do LDL sérico.
CoA: coenzima A
As estatinas são classificadas com base na sua percentagem de redução de LDL e dose:
As estatinas estão indicadas no tratamento de dislipidemias com o objetivo de reduzir eventos cardiovasculares major adversos:
A tabela seguinte compara e contrasta os fármacos da classe das estatinas. Estes estão listados por ordem decrescente de potência.
| Estatina | Solubilidade | Metabolismo | Semi-vida no plasma Plasma The residual portion of blood that is left after removal of blood cells by centrifugation without prior blood coagulation. Transfusion Products | Tempo de administração ideal |
|---|---|---|---|---|
| Pitavastatina | Lipofílica | CYP2C9 CYP2C9 A cytochrome p-450 subtype that has specificity for acidic xenobiotics. It oxidizes a broad range of important clinical drugs that fall under the categories of nonsteroidal anti-inflammatory agents; hypoglycemic agents; anticoagulants; and diuretics. Anticoagulants | 12 horas | A qualquer momento |
| Rosuvastatina | Hidrofílica | CYP2C9 CYP2C9 A cytochrome p-450 subtype that has specificity for acidic xenobiotics. It oxidizes a broad range of important clinical drugs that fall under the categories of nonsteroidal anti-inflammatory agents; hypoglycemic agents; anticoagulants; and diuretics. Anticoagulants | 19 horas | A qualquer momento |
| Atorvastatina | Lipofílica | CYP3A4 CYP3A4 Class 3 Antiarrhythmic Drugs (Potassium Channel Blockers) | 14 horas | A qualquer momento |
| Lovastatina | Lipofílica | CYP3A4 CYP3A4 Class 3 Antiarrhythmic Drugs (Potassium Channel Blockers) | 2 a 3 horas | Noite |
| Sinvastatina | Lipofílica | CYP3A4 CYP3A4 Class 3 Antiarrhythmic Drugs (Potassium Channel Blockers) | 2 a 3 horas | Noite |
| Pravastatina | Hidrofílica | Sulfatação | 1 a 3 horas | A qualquer momento |
| Fluvastatina | Lipofílica | CYP2C9 CYP2C9 A cytochrome p-450 subtype that has specificity for acidic xenobiotics. It oxidizes a broad range of important clinical drugs that fall under the categories of nonsteroidal anti-inflammatory agents; hypoglycemic agents; anticoagulants; and diuretics. Anticoagulants | 1 a 3 horas | Noite |