A distrofia muscular de Becker (BMD) é uma doença genética recessiva ligado ao cromossoma X, causado por uma mutação no gene DMD. É produzida uma proteína da distrofina muscular anormal, parcialmente funcional, que leva à fraqueza muscular progressiva e à perda eventual de capacidade da marcha. A evolução clínica é altamente variável, mas os sintomas geralmente aparecem na adolescência. O diagnóstico é estabelecido com base nos valores de enzimas musculares, testes genéticos e biópsia muscular (se necessária). O tratamento da BMD é de suporte e visa retardar a progressão da doença assim como das suas complicações. A miocardiopatia dilatada é a principal causa de morte.
Última atualização: Feb 25, 2025
A distrofia muscular de Becker (BMD) é a 2ª forma mais comum de distrofia muscular.
A distrofia muscular de Becker é causada por uma mutação de deleção ou duplicação non-frameshift do gene DMD no braço curto do cromossoma X.
Fisiologia normal:
Fisiopatologia na BMD:
A distrofia muscular de Becker tem uma apresentação altamente variável.
A distrofia muscular de Becker cursa com fraqueza muscular lentamente progressiva, num padrão de proximal para distal.
Sintomas:
Achados do exame objetivo:
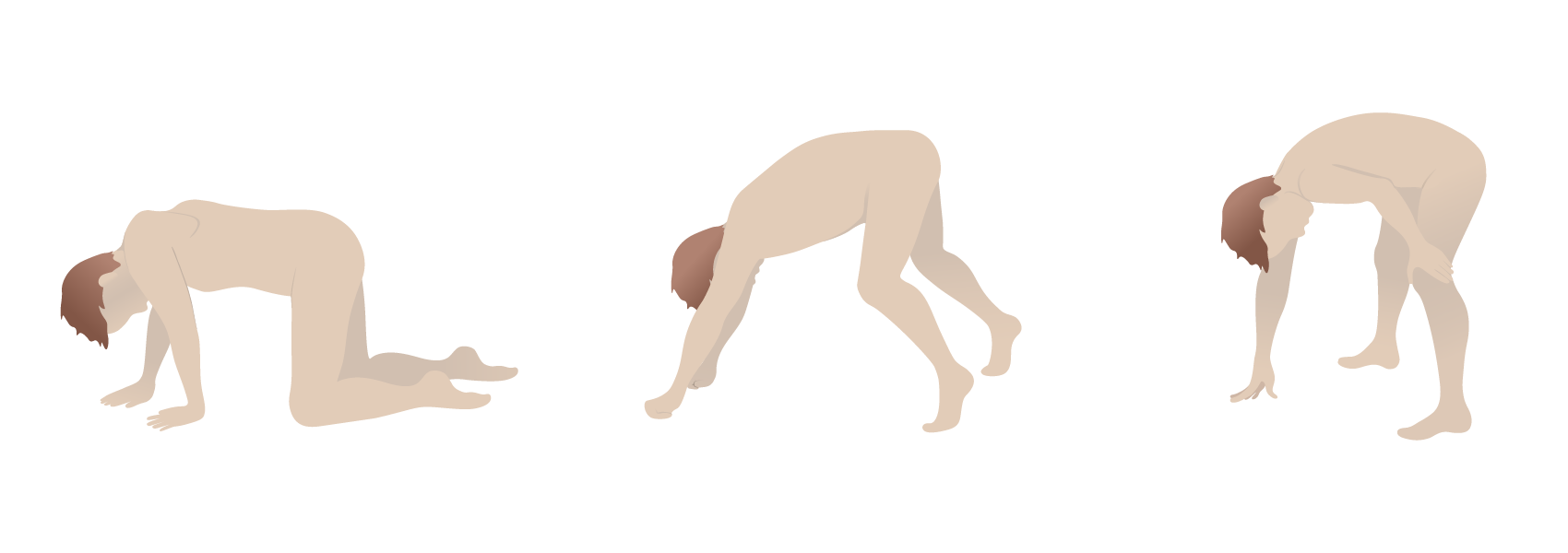
Sinal de Gower: devido à fraqueza muscular proximal, recorre-se ao uso dos braços e mãos como apoio para posicionamento em pé
Imagem por Lecturio.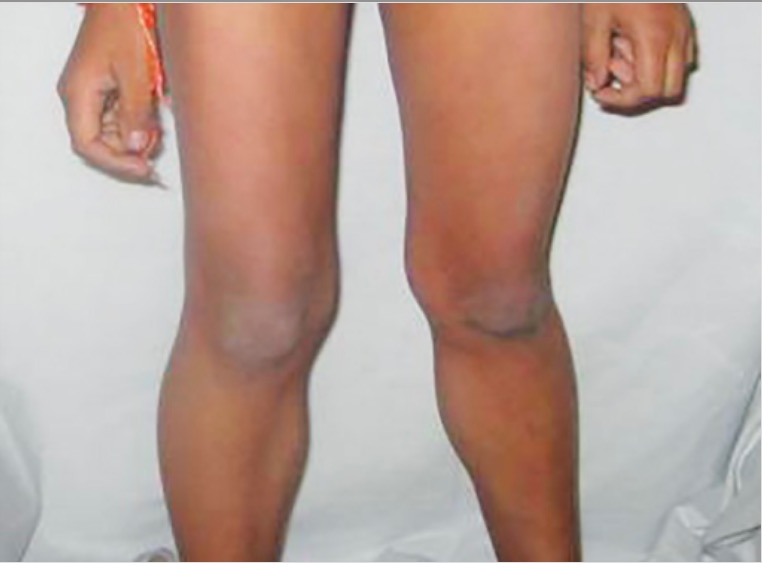
Pseudopertrofia dos músculos gastrocnémios devido à distrofia muscular: músculos grandes e fracos devido à substituição por gordura e tecido fibroso
Imagem: “Calf hypertrophy” por Professor, Departamento de Pedodontia e Odontologia Preventiva, Faculdade Dentária BJS, Ludhiana, Punjab, India. Licença: CC BY 3.0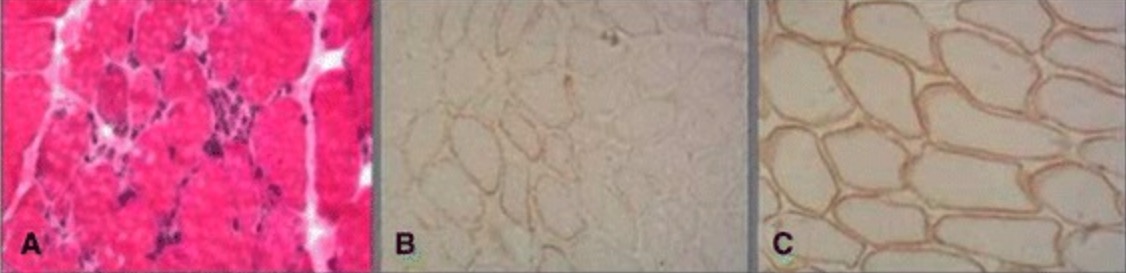
Biópsia muscular na distrofia muscular de Becker:
O exame histopatológico mostra fibras musculares necróticas com substituição por tecido fibroso e adiposo (A). A técnica de immunostaining mostra positividade parcial para a distrofina na distrofia muscular de Becker (B) em comparação com o músculo normal (C).
Não existe tratamento curativo para a BMD. O tratamento é dirigido a medidas de suporte e cuidados paliativos.