Os agentes antiplaquetários são fármacos que inibem a agregação plaquetária, um passo crítico na formação do tampão plaquetário inicial. A agregação anormal, ou inadequada, das plaquetas é um passo fundamental na fisiopatologia de eventos isquémicos arteriais. As principais categorias de agentes antiplaquetários incluem aspirina, inibidores de ADP, inibidores da absorção de fosfodiesterase/adenosina e inibidores da glicoproteína IIb/IIIa. As indicações comuns dos agentes antiplaquetários incluem o tratamento e prevenção de doenças cardíacas e AVC isquémicos, doença arterial periférica e outras patologias associadas a um alto risco de trombose arterial.
Last updated: Dec 15, 2025
Os agentes antiplaquetários são fármacos que inibem a agregação plaquetária, um passo crítico na formação do tampão plaquetário inicial.
Os antiplaquetários são utilizados no tratamento e/ou prevenção de trombose arterial. Indicações comuns incluem:
Existem várias classes primárias de agentes antiplaquetários:
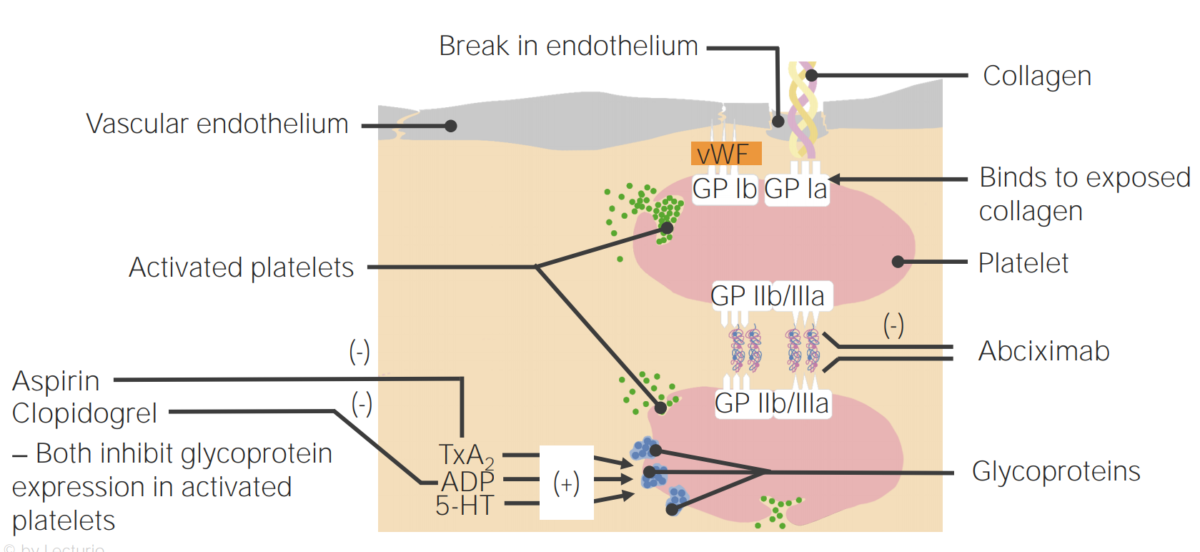
Mecanismos de ação dos agentes antiplaquetários
5-HT: 5-hidroxitriptamina
TxA2: tromboxano A2
VWF: fator von Willebrand
Após ocorrer uma lesão endotelial, a exposição do sangue aos componentes subendoteliais desencadeia a formação do tampão plaquetário. Este processo é conhecido como hemostasia primária. (A formação do coágulo de fibrina através da cascata de coagulação é uma hemostasia secundária).
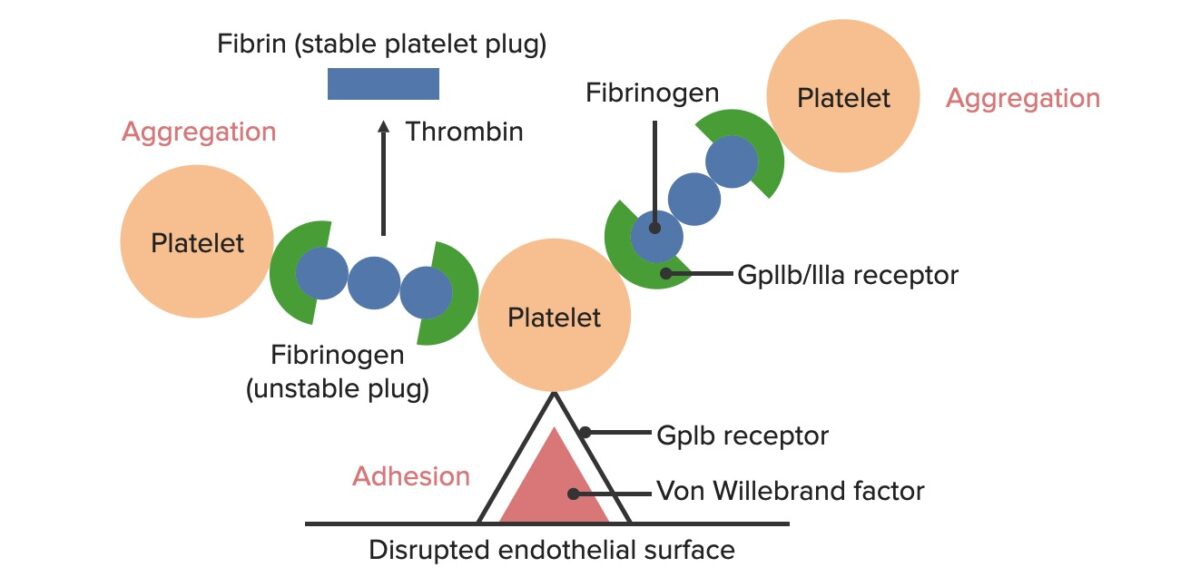
Formação do tampão hemostático temporário:
A superfície endotelial rompida expõe o VWF ao sangue que passa. As plaquetas ligam-se ao VWF através dos seus recetores GpIb, sendo ativadas. A ativação das plaquetas leva-as a secretar ADP, o que estimula a expressão dos recetores GpIIb/IIIa nas plaquetas. Os recetores GpIIb/IIIa ligam-se ao fibrinogénio, que é capaz de ligar uma plaqueta em cada extremidade, o que leva a que as plaquetas se agreguem. À medida que mais plaquetas se ligam umas às outras, gera-se o tampão plaquetário. À medida que a cascata de coagulação é ativada, a trombina converte o fibrinogénio mais fraco em fibrinogénio mais forte, o que cria um coágulo muito mais estável.
A exposição do sangue a componentes subendoteliais no local da lesão faz com que as plaquetas adiram a esse local.
As plaquetas ativadas aumentam a adesão e agregação plaquetária e estimulam a secreção dos grânulos plaquetários.
As plaquetas contêm grânulos, cada um dos quais liberta uma série de substâncias diferentes quando as plaquetas são ativadas. As funções das substâncias secretadas incluem:
| Mecanismo de Ação |
|
|---|---|
| Efeitos fisiológicos |
|
| Absorção |
|
| Distribuição |
|
| Metabolismo |
|
| Eliminação |
|
| Indicações específicas |
|
| Contraindicações específicas | Crianças <16 anos de idade (risco de síndrome de Reye se a criança desenvolver uma infeção viral) |
| Complicações/efeitos adversos |
|
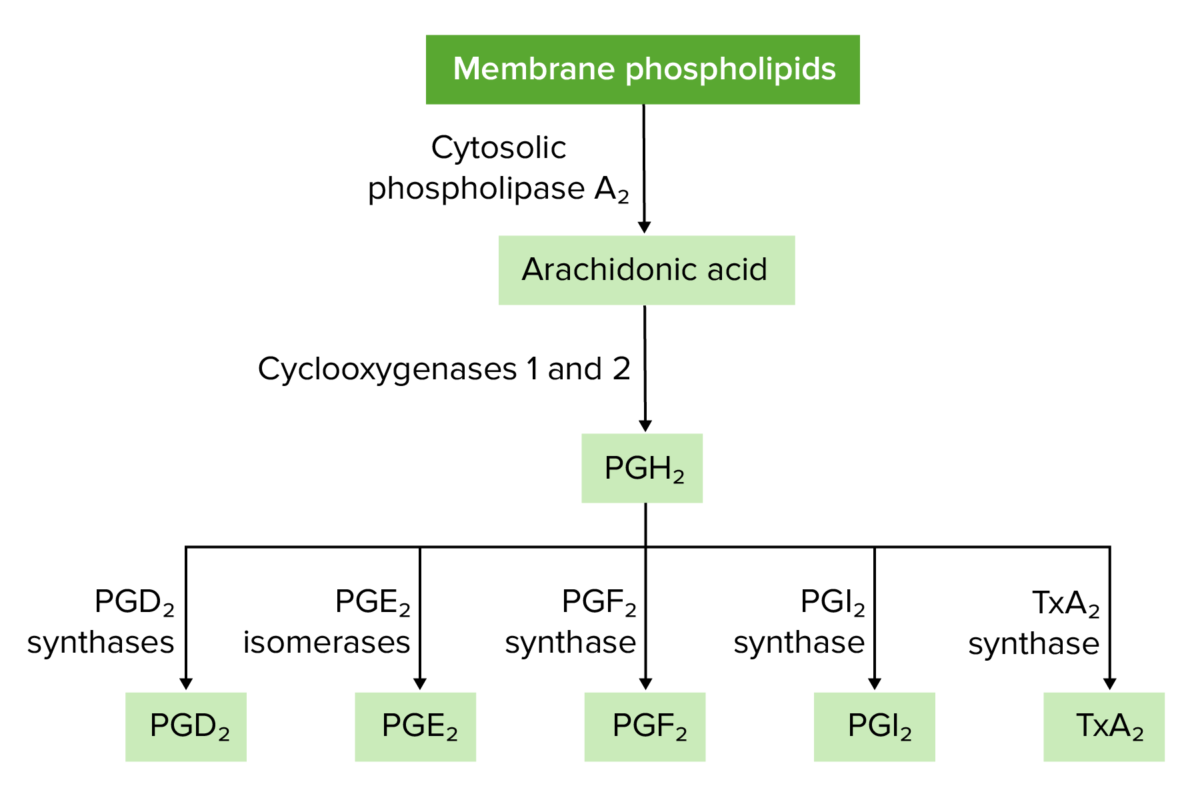
Visão geral da síntese de prostaglandinas e tromboxanos
PG: prostaglandina
| Agentes |
|
|---|---|
| Mecanismo de Ação |
|
| Efeitos fisiológicos |
|
| Indicações específicas |
|
| Contraindicações específicas | Prasugrel Prasugrel A piperazine derivative and platelet aggregation inhibitor that is used to prevent thrombosis in patients with acute coronary syndrome; unstable angina and myocardial infarction, as well as in those undergoing percutaneous coronary interventions. Antiplatelet Drugs: historial de um AVC isquémico ou TIA TIA Transient ischemic attack (TIA) is a temporary episode of neurologic dysfunction caused by ischemia without infarction that resolves completely when blood supply is restored. Transient ischemic attack is a neurologic emergency that warrants urgent medical attention. Transient Ischemic Attack (TIA) |
| Complicações |
|
| Fármaco | Clopidogrel Clopidogrel A ticlopidine analog and platelet purinergic p2y receptor antagonist that inhibits adenosine diphosphate-mediated platelet aggregation. It is used to prevent thromboembolism in patients with arterial occlusive diseases; myocardial infarction; stroke; or atrial fibrillation. Antiplatelet Drugs ( Plavix Plavix A ticlopidine analog and platelet purinergic p2y receptor antagonist that inhibits adenosine diphosphate-mediated platelet aggregation. It is used to prevent thromboembolism in patients with arterial occlusive diseases; myocardial infarction; stroke; or atrial fibrillation. Antiplatelet Drugs®) | Prasugrel Prasugrel A piperazine derivative and platelet aggregation inhibitor that is used to prevent thrombosis in patients with acute coronary syndrome; unstable angina and myocardial infarction, as well as in those undergoing percutaneous coronary interventions. Antiplatelet Drugs ( Effient Effient An adenosine triphosphate analogue and reversible p2y12 purinoceptor antagonist that inhibits adp-mediated platelet aggregation. It is used for the prevention of thromboembolism by patients with acute coronary syndrome or a history of myocardial infarction. Antiplatelet Drugs®) | Ticagrelor Ticagrelor An adenosine triphosphate analogue and reversible p2y12 purinoceptor antagonist that inhibits adp-mediated platelet aggregation. It is used for the prevention of thromboembolism by patients with acute coronary syndrome or a history of myocardial infarction. Antiplatelet Drugs |
|---|---|---|---|
| Absorção |
|
|
|
| Distribuição | Altamente ligado a proteínas (98%) |
|
|
| Metabolismo |
Metabolizado no fígado por:
|
Hidrolisado nos intestinos e no soro a um intermediário tiolactona inativo, sendo então convertido para um metabolito ativo por oxidação pelos CYP3A4 CYP3A4 Class 3 Antiarrhythmic Drugs (Potassium Channel Blockers) e CYP2B6 | Metabolizado pelo fígado a um metabolito ativo pelo CYP3A4 CYP3A4 Class 3 Antiarrhythmic Drugs (Potassium Channel Blockers) |
| Eliminação |
|
|
|
| Agentes | Dipiridamol (Persantine®) | Cilostazol Cilostazol A quinoline and tetrazole derivative that acts as a phosphodiesterase type 3 inhibitor, with anti-platelet and vasodilating activity. It is used in the treatment of peripheral vascular diseases; ischemic heart disease; and in the prevention of stroke. Phosphodiesterase Inhibitors |
|---|---|---|
| Mecanismo de Ação |
Mecanismos de ação duplos:
|
|
| Efeitos fisiológicos |
|
|
| Absorção |
|
|
| Distribuição |
|
Ligação a proteínas: 95% |
| Metabolismo |
|
|
| Eliminação |
|
|
| Indicações específicas |
|
Claudicação intermitente |
| Contraindicações específicas |
|
Insuficiência cardíaca |
| Complicações |
|
Pode induzir taquicardia, taquiarritmias e/ou hipotensão |
| Efeitos adversos |
|
|
Os 2 inibidores primários de GPIIb/IIIa são o eptifibatide Eptifibatide Cyclic peptide that acts as a platelet glycoprotein iib-iiia antagonist, reversibly inhibiting the binding of fibrinogen; von Willebrand factor; and other adhesive molecules to the gpiib-iiia receptors of platelets. It is used in the management of unstable angina and in patients undergoing coronary angioplasty and stenting procedures. Antiplatelet Drugs ( Integrilin Integrilin Cyclic peptide that acts as a platelet glycoprotein iib-iiia antagonist, reversibly inhibiting the binding of fibrinogen; von Willebrand factor; and other adhesive molecules to the gpiib-iiia receptors of platelets. It is used in the management of unstable angina and in patients undergoing coronary angioplasty and stenting procedures. Antiplatelet Drugs®) e o tirofibano ( Aggrastat Aggrastat Tyrosine analog and platelet glycoprotein gpiib-iiia complex antagonist that inhibits platelet aggregation and is used in the treatment of acute coronary syndrome. Antiplatelet Drugs®). O abciximab é um anticorpo monoclonal que também se encontra nesta categoria; no entanto, já não está disponível nos Estados Unidos.
| Agentes | Eptifibatide Eptifibatide Cyclic peptide that acts as a platelet glycoprotein iib-iiia antagonist, reversibly inhibiting the binding of fibrinogen; von Willebrand factor; and other adhesive molecules to the gpiib-iiia receptors of platelets. It is used in the management of unstable angina and in patients undergoing coronary angioplasty and stenting procedures. Antiplatelet Drugs ( Integrilin Integrilin Cyclic peptide that acts as a platelet glycoprotein iib-iiia antagonist, reversibly inhibiting the binding of fibrinogen; von Willebrand factor; and other adhesive molecules to the gpiib-iiia receptors of platelets. It is used in the management of unstable angina and in patients undergoing coronary angioplasty and stenting procedures. Antiplatelet Drugs®) | Tirofibano ( Aggrastat Aggrastat Tyrosine analog and platelet glycoprotein gpiib-iiia complex antagonist that inhibits platelet aggregation and is used in the treatment of acute coronary syndrome. Antiplatelet Drugs®) |
|---|---|---|
| Mecanismo de Ação | Liga-se e inibe o recetor de GPIIb/IIIa | |
| Efeitos fisiológicos | Evita que os recetores GPIIb/IIIa liguem o fibrinogénio e, assim, impede a agregação plaquetária | |
| Absorção |
|
|
| Distribuição |
|
|
| Metabolismo | Negligenciável | |
| Eliminação |
|
|
| Indicações específicas |
|
|
| Contraindicações específicas | Trombocitopenia grave | |
| Complicações |
|
|
Alguns dos usos terapêuticos mais MAIS Androgen Insensitivity Syndrome comuns dos agentes antiplaquetários incluem: