Los agentes antiplaquetarios son medicamentos que inhiben la agregación plaquetaria, un paso crítico en la formación del tapón plaquetario inicial. La agregación plaquetaria anormal o inapropiada es un paso clave en la fisiopatología de los eventos isquémicos arteriales. Las categorías principales de agentes antiplaquetarios incluyen aspirina, inhibidores de difosfato de adenosina, inhibidores de la captación de fosfodiesterasa/adenosina e inhibidores de la glucoproteína IIb/IIIa. Las indicaciones comunes para los agentes antiplaquetarios incluyen el tratamiento y la prevención de la cardiopatía isquémica y el accidente cerebrovascular, la enfermedad arterial periférica y otras afecciones asociadas con un alto riesgo de trombosis arterial.
Última actualización: Jun 27, 2025
Los medicamentos antiplaquetarios son medicamentos que inhiben la agregación plaquetaria, un paso crítico en la formación del tapón plaquetario inicial.
Los antiplaquetarios se utilizan en el tratamiento y/o prevención de la trombosis arterial. Las indicaciones comunes incluyen:
Existen varias clases principales de agentes antiplaquetarios:
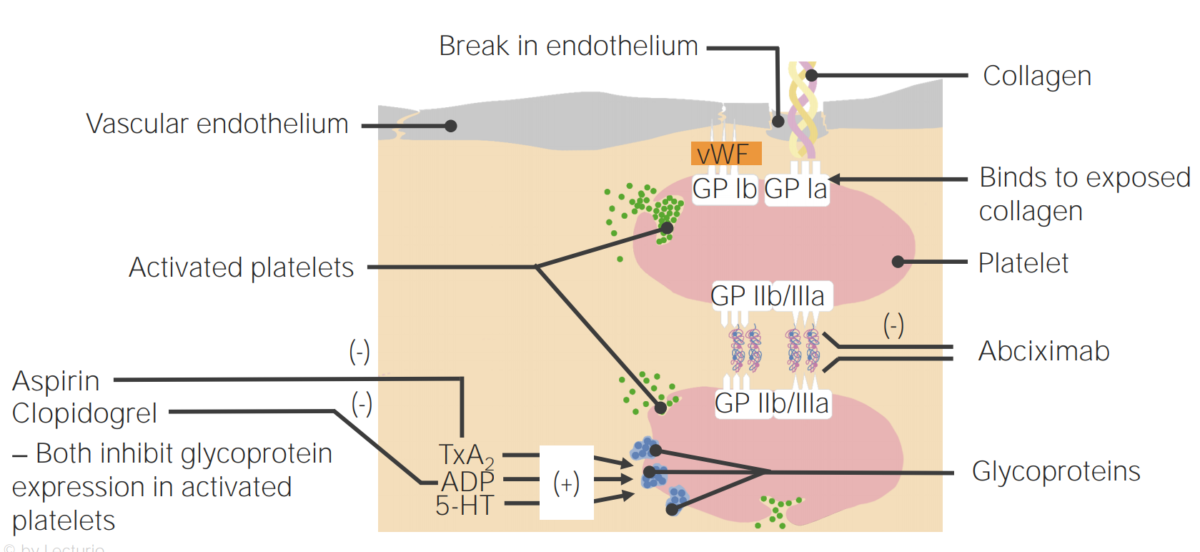
Mecanismos de acción de los agentes antiplaquetarios
5-HT: 5-hidroxitriptamina
TxA 2 : tromboxano A 2
vWF: factor de von Willebrand
Después de que ocurre la lesión endotelial, la exposición de la sangre a los componentes subendoteliales desencadena la formación del tapón plaquetario. Este proceso se conoce como hemostasia primaria. (La formación del coágulo de fibrina a través de la cascada de coagulación es la hemostasia secundaria).
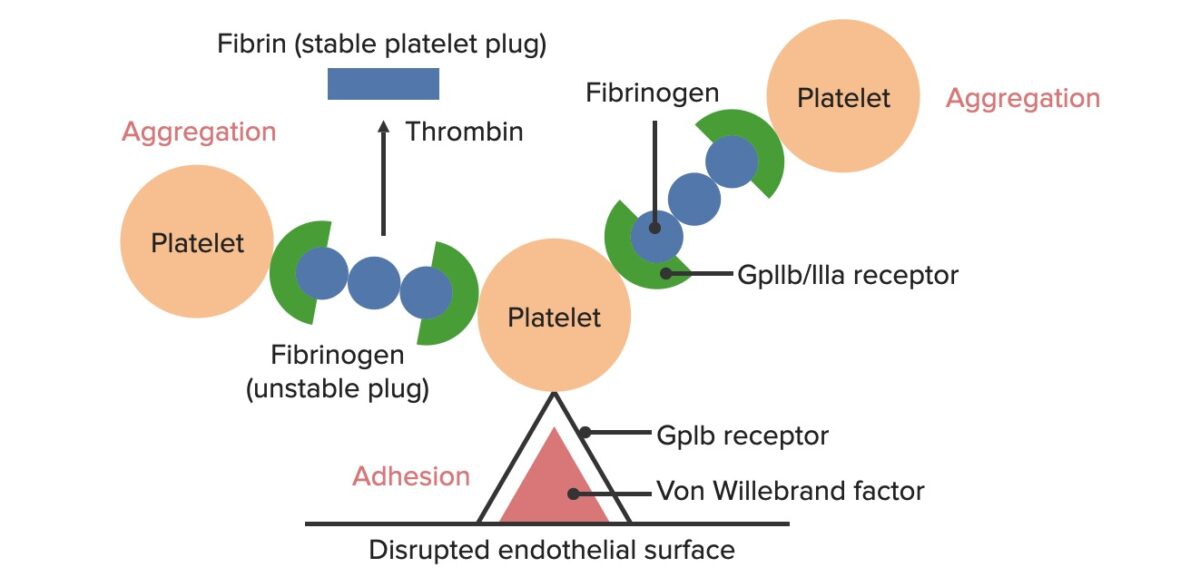
Formación del tapón hemostático temporal:
La superficie endotelial rota expone el factor de von Willebrand a la sangre. Las plaquetas se unen al factor de von Willebrand a través de sus receptores GpIb y se activan. La activación de las plaquetas hace que segreguen difosfato de adenosina, lo que estimula la expresión de los receptores GpIIb/IIIa en las plaquetas. Los receptores GpIIb/IIIa se unen al fibrinógeno, que puede unirse a una plaqueta en cada extremo, lo que hace que las plaquetas se agreguen. A medida que se unen más plaquetas entre sí, se genera el tapón plaquetario. Mientras que se activa la cascada de coagulación, la trombina convierte el fibrinógeno, el cual es débil, en fibrina que es más fuerte, creando así un coágulo mucho más estable.
La exposición de la sangre a los componentes subendoteliales en el sitio de la lesión hace que las plaquetas se adhieran a ese sitio.
Las plaquetas activadas mejoran aún más la adhesión y agregación plaquetaria y estimulan la secreción de los gránulos plaquetarios.
Las plaquetas contienen gránulos, cada uno de los cuales libera una serie de sustancias diferentes cuando se activan las plaquetas. Las funciones de las sustancias secretadas incluyen:
| Mecanismo de acción |
|
|---|---|
| Efectos fisiológicos |
|
| Absorción |
|
| Distribución |
|
| Metabolismo |
|
| Eliminación |
|
| Indicaciones específicas |
|
| Contraindicaciones específicas | Niños menores de 16 años (riesgo de síndrome de Reye si el niño desarrolla una infección viral) |
| Complicaciones / efectos secundarios |
|
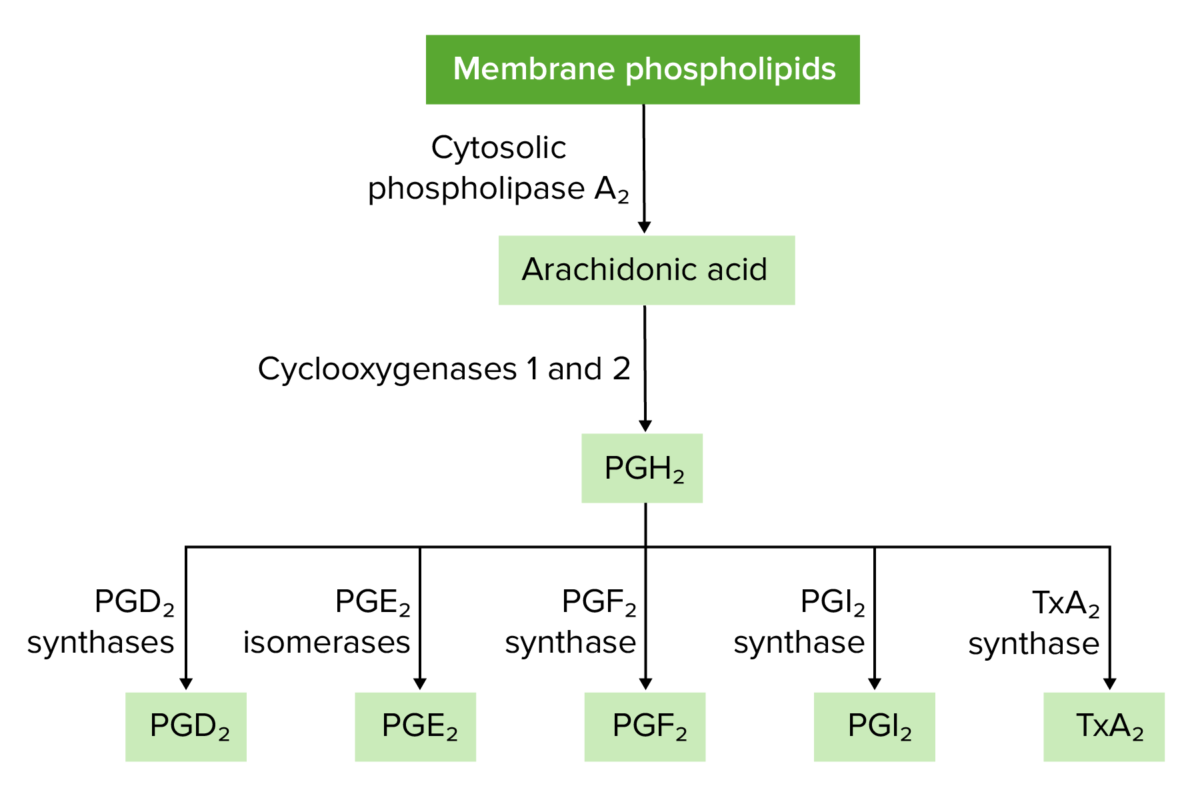
Descripción general de la síntesis de prostaglandinas y tromboxanos
PG: prostaglandina
| Medicamentos |
|
|---|---|
| Mecanismo de acción |
|
| Efectos fisiológicos |
|
| Indicaciones específicas |
|
| Contraindicaciones específicas | Prasugrel: antecedentes de ictus isquémico o AIT |
| Complicaciones |
|
| Medicamento | Clopidogrel (Plavix®) | Prasugrel (Effient®) | Ticagrelor |
|---|---|---|---|
| Absorción |
|
|
|
| Distribución | Altamente unido a proteínas (98%) |
|
|
| Metabolismo |
Metabolismo hepático a través de:
|
Se hidroliza en los intestinos y en el suero a un intermediario inactivo de tiolactona, que luego es convertido en un metabolito activo a través de la oxidación del CYP3A4 y CYP2B6 | Metabolismo hepático a un metabolito activo a través del CYP3A4 |
| Eliminación |
|
|
|
| Medicamentos | Dipiridamol (Persantine®) | Cilostazol |
|---|---|---|
| Mecanismo de acción |
Mecanismo de acción doble:
|
|
| Efectos fisiológicos |
|
|
| Absorción |
|
|
| Distribución |
|
Unión a proteínas: 95% |
| Metabolismo |
|
|
| Eliminación |
|
|
| Indicaciones específicas |
|
Claudicación intermitente |
| Contraindicaciones específicas |
|
Insuficiencia cardiaca |
| Complicaciones |
|
Puede inducir taquicardia, taquiarritmias y/o hipotensión |
| Efectos secundarios |
|
|
Los 2 inhibidores primarios de la GPIIb/IIIa son el eptifibatide (Integrilin®) y tirofibán (Aggrastat®). El abciximab es un anticuerpo monoclonal que también se encuentra en esta categoría; sin embargo, ya no está disponible en los Estados Unidos.
| Medicamentos | Eptifibatida (Integrilin®) | Tirofibán (Aggrastat®) |
|---|---|---|
| Mecanismo de acción | Se unen e inhiben reversiblemente el receptor GPIIb/IIIa | |
| Efectos fisiológicos | Evitan que los receptores GPIIb/IIIa se unan al fibrinógeno y, por lo tanto, evitan la agregación plaquetaria. | |
| Absorción |
|
|
| Distribución |
|
|
| Metabolismo | Insignificante | |
| Eliminación |
|
|
| Indicaciones específicas |
|
|
| Contraindicaciones específicas | Trombocitopenia grave | |
| Complicaciones |
|
|
Algunos de los usos terapéuticos más comunes de los agentes antiplaquetarios incluyen: