O raquitismo hipofosfatémico ligado ao X (RHLX) é o mais comum dos vários distúrbios hereditários caracterizados pela excreção de fosfato renal e que leva a ossos frágeis ou moles. Anteriormente conhecido como "raquitismo resistente a vitamina D", o RHLX não é atualmente considerada uma verdadeira resistência à vitamina D (relacionada com defeitos hereditários na via metabólica da vitamina D ou no recetor de calcitriol). A apresentação clínica típica inicia-se durante a infância e manifesta-se como baixa estatura, joelhos em valgo ou em varo, dor óssea e odontalgia. O diagnóstico é feito através de estudos laboratoriais e confirmado pela identificação da mutação no gene PHEX. O tratamento inclui burosumab a administração de elevadas doses de vitamina D (calcitriol) e fosfato. Para garantir o crescimento adequado, é fulcral o acompanhamento destes pacientes por uma equipa multidisciplinar.
Última atualização: Jul 8, 2022
O raquitismo hipofosfatémico ligado ao X (RHLX) é uma doença genética rara que causa hipofosfatémia e consequente raquitismo clínico.
A apresentação clínica dos RHLX pode variar de assintomática a gravemente sintomática. O raquitismo hipofosfatémico ligado ao X é geralmente confundido com o raquitismo nutricional nos bebés, e os sintomas incluem:
Antecedentes familiares:
Testes de laboratório:
Testes genéticos:
Imagiologia:
Deve ser realizada a avaliação radiológica para excluir a curvatura fisiológica e a displasia óssea. Potenciais achados no raio-X podem incluir:
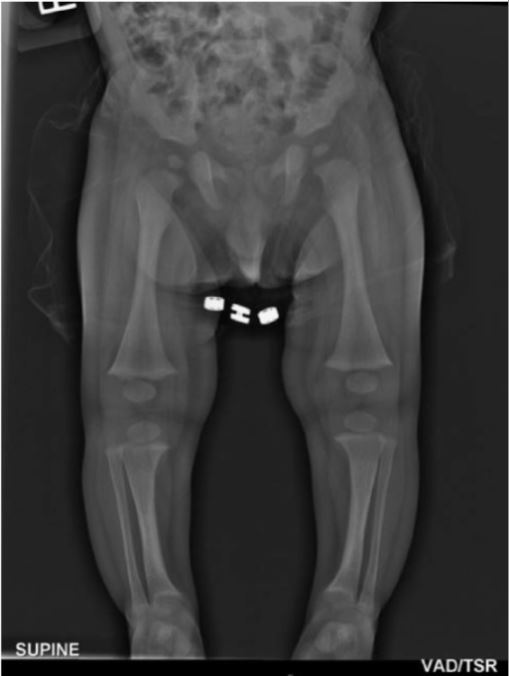
Uma criança de 7 meses com raquitismo hipofosfatémico ligado ao X:
Os ossos longos dos membros inferiores demonstram alargamento das metáfises com desgaste, mas sem alargamento da epífise. Existe também uma ligeira curvatura da tíbia.
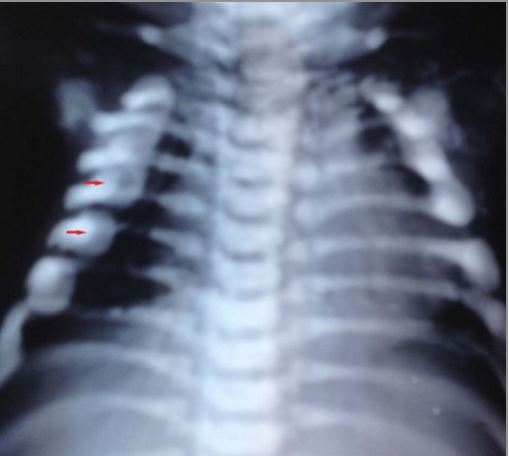
Radiografia que mostra rosário raquítico: poeminências tipo conta nas articulações costocondrais
Imagem: “Malignant infantile osteopetrosis: Case report with review of literature” por Essabar L, Meskini T, Ettair S, Erreimi N, Mouane N. License: CC BY 2.0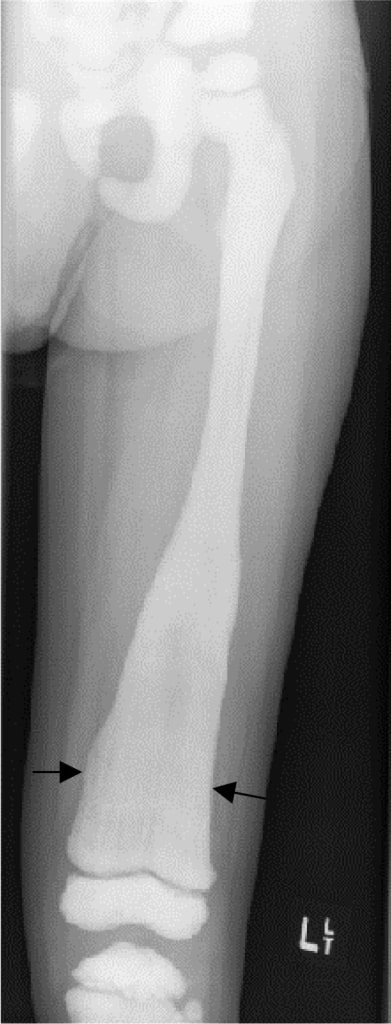
Um raio-X de uma criança de 4 anos com deformidade em frasco de Erlenmeyer do fémur distal, que mostra o reforço da metáfise no raquitismo hipofosfatémico ligado ao X
Imagem: “Osteopetrosis” por Stark Z, Savarirayan R. Licença: CC BY 2.0Os objetivos do tratamento são melhorar a osteomalácia e as deformidades esqueléticas, melhorar o crescimento dos bebés, a atividade física das crianças e diminuir a dor.
Alguns adultos com RHLX podem ter problemas médicos ligeiros, enquanto outros podem apresentar dor persistente ou complicações. É imperativa a monitorização do tratamento para potenciais complicações do hiperparatiroidismo e nefrocalcinose.