A hiperplasia endometrial (HE) diz respeito ao crescimento anormal do endométrio uterino. Este crescimento anormal pode ser devido à estimulação de estrogénio ou mutações genéticas que levam à proliferação descontrolada. O carcinoma endometrial (CE) é a neoplasia ginecológica mais MAIS Androgen Insensitivity Syndrome comum em países desenvolvidos e inclui vários tipos histológicos. O carcinoma endometrioide (conhecido como CE tipo 1) geralmente desenvolve-se a partir de hiperplasia endometrial atípica, é hormonalmente responsivo e apresenta um prognóstico favorável. Outros tipos histológicos são conhecidos como CE tipo 2; tendem a apresentar-se em estadios mais MAIS Androgen Insensitivity Syndrome avançados, não respondem a hormonas e têm um prognóstico muito pior. Mulheres com HE e CE tendem a apresentar hemorragia menstrual irregular ou pós-menopausa. O diagnóstico é histológico. O tratamento geralmente envolve terapia com progesterona, cirurgia e radioterapia adjuvante (para doença avançada).
Last updated: Dec 15, 2025
A hiperplasia endometrial (HE) é um estado de proliferação excessiva de células endometriais, que resulta num aumento do rácio glândula-estroma.
O carcinoma endometrial (CE) refere-se à proliferação excessiva de células endometriais que são capazes de invadir os tecidos circundantes e metastatizar para locais à distância.
Existem 2 sistemas de classificação primária para hiperplasia endometrial:
| Terminologia do sistema da WHO | Terminologia do sistema EIN EIN Atypical hyperplasia Endometrial Hyperplasia and Endometrial Cancer | Características |
|---|---|---|
| Endométrio normal | Endométrio normal |
|
| Hiperplasia sem atipia | Hiperplasia benigna do endométrio |
|
| Hiperplasia atípica | EIN EIN Atypical hyperplasia Endometrial Hyperplasia and Endometrial Cancer |
|
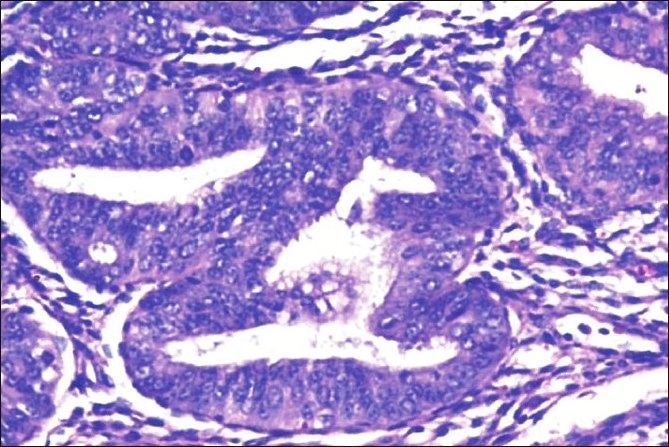
Histopatologia da neoplasia intraepitelial endometrial/hiperplasia atípica:
A imagem mostra glândulas endometriais compactas com estroma intermediário escassso e estratificação do epitélio de revestimento
As células epiteliais mostram atipia citológica com alto rácio nucleocitoplasmático, aglomeração irregular de cromatina nuclear e figuras mitóticas (coloração de hematoxilina & eosina, × 200)
A classificação do CE é de acordo com o seu subtipo histológico. O adenocarcinoma endometrioide de baixo grau é conhecido como tipo 1 e todos os outros são do tipo 2.
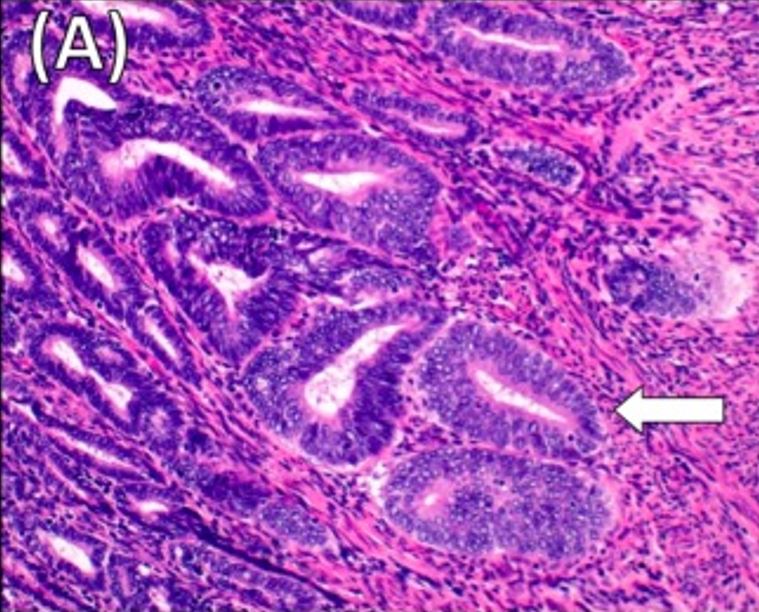
Histologia do adenocarcinoma endometrioide grau 2 moderadamente diferenciado:
Observe a invasão miometrial superficial do tumor (seta). Coloração H&E x20
O grau descreve a quantidade de crescimento glandular sólido. O cancro endometrial é classificado em 1 de 3 graus.
| Grau | Definição | Histologia |
|---|---|---|
| I | Bem diferenciado | ≤ 5% do tecido exibe um padrão de crescimento sólido |
| II | Moderadamente diferenciado | 6%–50% do tecido exibe um padrão de crescimento sólido |
| III | Pouco diferenciado | > 50% do tecido exibe um padrão de crescimento sólido |
O estadio descreve a extensão da disseminação do tumor Tumor Inflammation. O estadiamento tem em consideração o tamanho do tumor Tumor Inflammation, extensão da invasão local, envolvimento gnaglionar e metástases. Existem 4 estádios principais no CE. A doença é estadiada com base nos achados de maior grau “highest findings”. Por exemplo, um tumor Tumor Inflammation confinado ao colo do útero, mas com gânglios linfáticos positivos, é classificado como estadio III. Da mesma forma, a invasão direta do tumor Tumor Inflammation na mucosa da bexiga é estádio IV, independentemente do envolvimento dos gânglios linfáticos.
| Estádio | Extensão da invasão do tumor Tumor Inflammation no tecido circundante | Metastização |
|---|---|---|
| I | O tumor Tumor Inflammation está confinado ao corpo uterino. | Nenhuma |
| II | O tumor Tumor Inflammation invade o estroma do colo do útero, mas não se estende além do útero. | Nenhuma |
| III | Tumor Tumor Inflammation invade anexos, vagina Vagina The vagina is the female genital canal, extending from the vulva externally to the cervix uteri internally. The structures have sexual, reproductive, and urinary functions and a rich blood supply, mainly arising from the internal iliac artery. Vagina, Vulva, and Pelvic Floor: Anatomy ou paramétrio. | Metástases para gânglios linfáticos regionais: gânglios linfáticos pélvicos ou para-aórticos |
| IV | Invasão direta do tumor Tumor Inflammation na mucosa da bexiga ou reto |
|
A maioria dos fatores de risco para HE e CE inclui qualquer fator que aumente a exposição ao estrogénio sem oposição.
Os seguintes fatores diminuem o risco de HE/CE:
Cerca de ¾ das mulheres diagnosticadas com CE estão na pós-menopausa. A apresentação clássica é uma mulher obesa de 60 e poucos anos com hemorragia pós-menopausa.
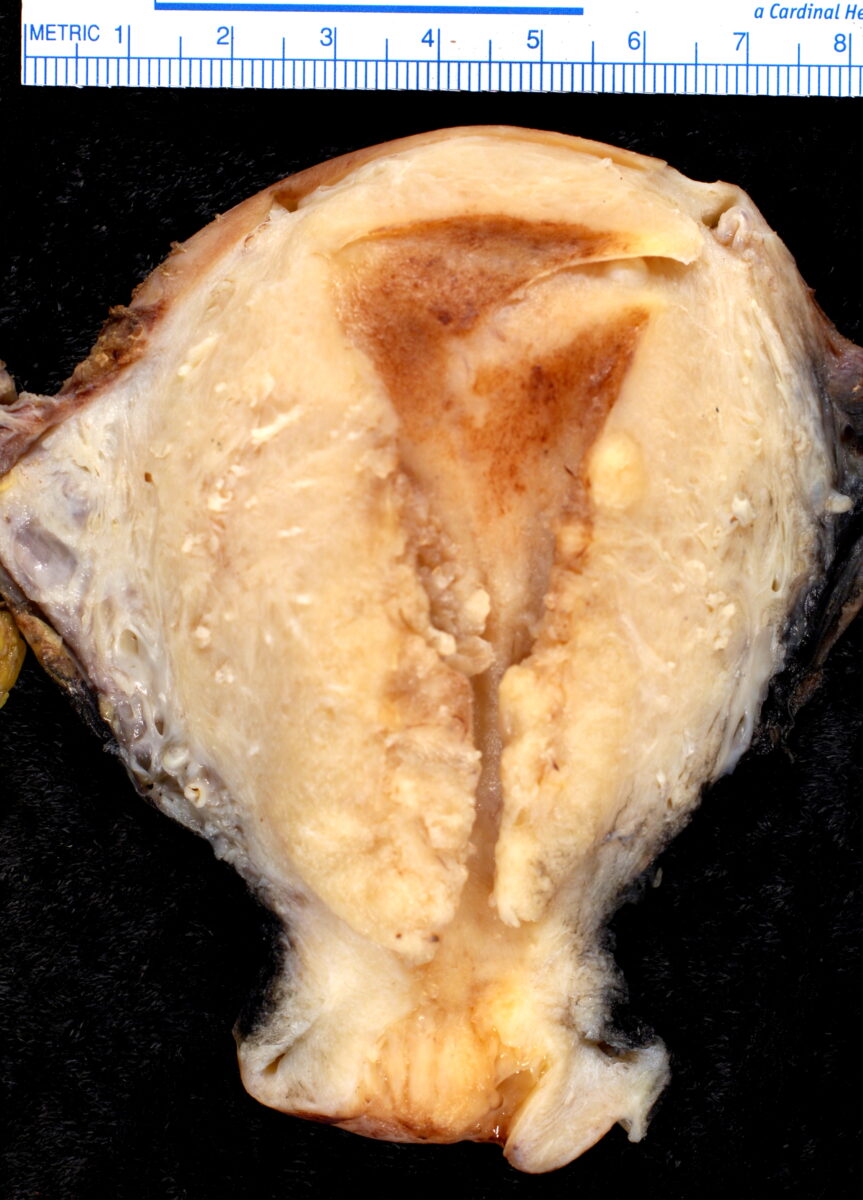
Adenocarcinoma endometrioide, amostra macroscópica:
Observar o tumor principalmente na metade inferior da amostra, que invade o miométrio circundante.
A biópsia é necessária para o diagnóstico definitivo de HE e CE. O exame pélvico geralmente é normal. Todas as mulheres que apresentem hemorragia anormal (especialmente hemorragia pós-menopausa) devem ser avaliadas com ecografia pélvica e/ou biópsia.
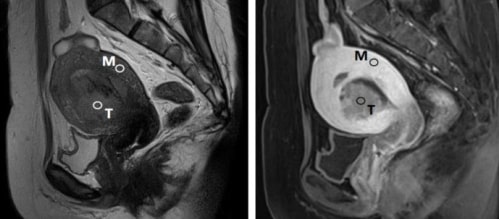
Cancro do endométrio em corte sagital
Esquerda: RM ponderada em T2
Direita: RM ponderada em T1 com contraste
T: tumor
M: miométrio
O tratamento é principalmente cirúrgico, com potencial para radioterapia adjuvante. O tratamento da doença avançada é altamente individualizado.