La hiperplasia endometrial (HE) es el crecimiento anormal del endometrio uterino. Este crecimiento anormal puede deberse a estimulación estrogénica o a mutaciones genéticas que conducen a una proliferación descontrolada. El carcinoma endometrial (CE) es la neoplasia maligna ginecológica más común en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum países desarrollados y tiene varios tipos histológicos. El carcinoma endometrioide (conocido como CE tipo 1) generalmente se desarrolla a partir de una hiperplasia endometrial atípica, es sensible a hormonas y conlleva un pronóstico favorable. Otros tipos histológicos se conocen como CE tipo 2; tienden a presentarse en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum etapas más avanzadas, no responden a hormonas y tienen un pronóstico mucho peor. Las mujeres con HE y CE tienden a presentar sangrado menstrual posmenopáusico o irregular. El diagnóstico es histológico. El tratamiento suele incluir terapia con progestinas, cirugía y radioterapia adyuvante (para enfermedad avanzada).
Last updated: Dec 15, 2025
La hiperplasia endometrial (HE) es un estado de proliferación excesiva de células endometriales, lo que resulta en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum un aumento de la relación glándula-estroma.
El carcinoma endometrial (CE) se refiere a la proliferación excesiva de células endometriales que son capaces de invadir los LOS Neisseria tejidos circundantes y metastatizar a sitios distantes.
Existen 2 sistemas de clasificación principales para la hiperplasia endometrial:
| Terminología del sistema de la OMS | Terminología del sistema NIE | Características |
|---|---|---|
| Endometrio normal | Endometrio normal |
|
| Hiperplasia sin atipia | Hiperplasia endometrial benigna |
|
| Hiperplasia atípica | NIE |
|
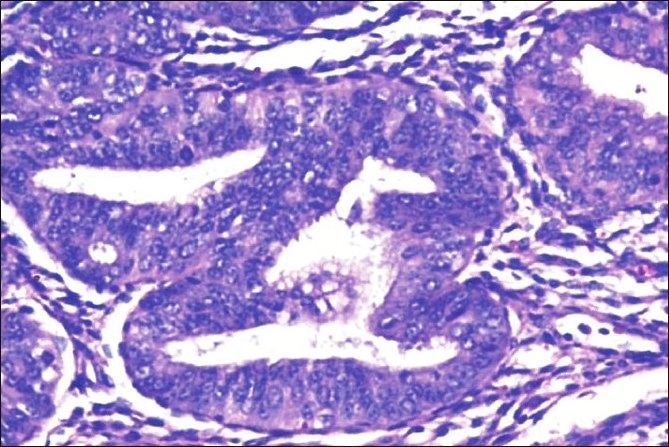
Histopatología de la neoplasia intraepitelial endometrial/hiperplasia atípica:
La imagen muestra glándulas endometriales estrechamente empaquetadas con escaso estroma intermedio y estratificación del epitelio de revestimiento.
Las células epiteliales muestran atipia citológica con una proporción nucleocitoplasmática alta, aglutinación irregular de la cromatina nuclear y figuras mitóticas (tinción con hematoxilina y eosina, ×200)
Clasificación de CE según su subtipo histológico. El adenocarcinoma endometrioide de bajo grado se conoce como tipo 1 y todos los LOS Neisseria demás son tipo 2.
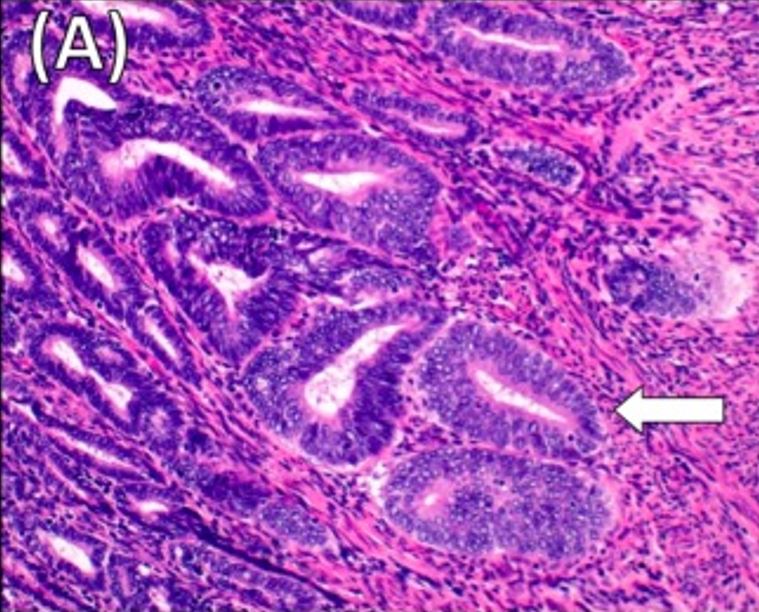
Histología del adenocarcinoma endometrioide de grado 2 moderadamente diferenciado:
Obsérvese la invasión miometrial superficial del tumor (flecha). Tinción H&E x20
El grado describe la cantidad de crecimiento glandular sólido. El cáncer endometrial se clasifica en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 1 de 3 grados.
| Grado | Definición | Histología |
|---|---|---|
| I | Bien diferenciado | ≤ 5% del tejido exhibe un patrón de crecimiento sólido |
| II | Moderadamente diferenciado | 6%–50% del tejido exhibe un patrón de crecimiento sólido |
| III | Pobremente diferenciado | > 50% del tejido exhibe un patrón de crecimiento sólido |
El estadio describe la extensión de la diseminación del tumor. La estadificación tiene en cuenta el tamaño del tumor, la extensión de la invasión local, la afectación de los ganglios linfáticos y la metástasis. Hay 4 estadios principales en el CE. La enfermedad se estadifica según los hallazgos “más elevados”. Por ejemplo, un tumor Tumor Inflammation limitado al AL Amyloidosis cuello uterino, pero con ganglios linfáticos positivos, se clasifica como estadio III. De manera similar, la invasión tumoral directa a la mucosa de la vejiga se encuentra en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum el estadio IV, independientemente de la afectación de los LOS Neisseria ganglios linfáticos.
| Estadio | Extensión de la invasión del tumor Tumor Inflammation en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum el tejido circundante | Metástasis |
|---|---|---|
| I | El tumor Tumor Inflammation está confinado al AL Amyloidosis cuerpo uterino. | Ninguna |
| II | El tumor Tumor Inflammation invade el estroma del cuello uterino, pero no se extiende más allá del útero. | Ninguna |
| III | El tumor Tumor Inflammation invade los LOS Neisseria anexos, la vagina Vagina The vagina is the female genital canal, extending from the vulva externally to the cervix uteri internally. The structures have sexual, reproductive, and urinary functions and a rich blood supply, mainly arising from the internal iliac artery. Vagina, Vulva, and Pelvic Floor: Anatomy o el parametrio. | Metástasis a ganglios linfáticos regionales: ganglios pélvicos o paraaórticos |
| IV | Invasión tumoral directa en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum la mucosa de la vejiga o el recto |
La mayoría de los LOS Neisseria factores de riesgo tanto para la HE como para el CE incluyen cualquier cosa que aumente la exposición a estrógenos sin oposición.
Los LOS Neisseria siguientes factores disminuyen el riesgo de HE/CE:
Alrededor de ¾ de las mujeres diagnosticadas con CE son posmenopáusicas. La presentación clásica es una mujer obesa de 60 y tantos años con sangrado posmenopáusico.
Se requiere biopsia para el diagnóstico definitivo de HE y CE. El examen pélvico suele ser normal. Todas las mujeres que presenten sangrado anormal (especialmente sangrado posmenopáusico) deben ser evaluadas con ultrasonido pélvico y/o biopsia.
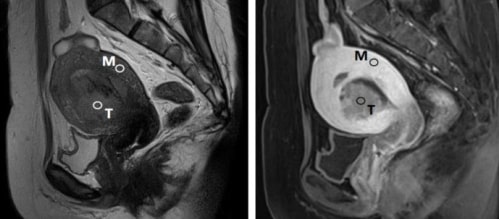
Cáncer de endometrio visto en una vista sagital
Izquierda: RM ponderada en T2
Derecha: RM ponderada en T1 con contraste
T: tumor
M: miometrio
El tratamiento es principalmente quirúrgico, con posibilidad de radioterapia adyuvante. El manejo de la enfermedad avanzada es altamente individualizado.