A hemorragia subdural (HSD) é o sangramento no espaço entre as camadas meníngeas da dura e da aracnoide, ao redor do cérebro. O mecanismo mais MAIS Androgen Insensitivity Syndrome comum que desencadeia o evento de sangramento é o trauma (e.g., traumatismo cranioencefálico contuso) causando uma lesão de estiramento das veias que comunicam com a circulação extracerebral, mas a rutura de pequenas artérias neste espaço ou a hipotensão intracraniana também podem ser possíveis etiologias. A HSD aguda apresenta-se imediatamente após um traumatismo cranioencefálico, com alteração do nível de consciência que pode ir desde uma perda momentânea de consciência até ao coma Coma Coma is defined as a deep state of unarousable unresponsiveness, characterized by a score of 3 points on the GCS. A comatose state can be caused by a multitude of conditions, making the precise epidemiology and prognosis of coma difficult to determine. Coma, o que a torna uma condição potencialmente fatal. HSD crónica também pode ocorrer, apresentando uma deterioração neurológica mais MAIS Androgen Insensitivity Syndrome gradual. O diagnóstico é baseado na suspeita clínica após traumatismo cranioencefálico e confirmado com neuroimagem (e.g., TAC de crânio sem contraste). O tratamento inclui estabilização, interrupção (possivelmente reversão) de todos os anticoagulantes, monitorização numa UCI neurológica e intervenção neurocirúrgica.
Last updated: Dec 15, 2025
O hematoma Hematoma A collection of blood outside the blood vessels. Hematoma can be localized in an organ, space, or tissue. Intussusception subdural (HSD) é o sangramento, geralmente causado por traumatismo craniano, no espaço entre as camadas meníngeas da dura e da aracnoide, que envolvem o cérebro, criando um espaço denominado espaço subdural.
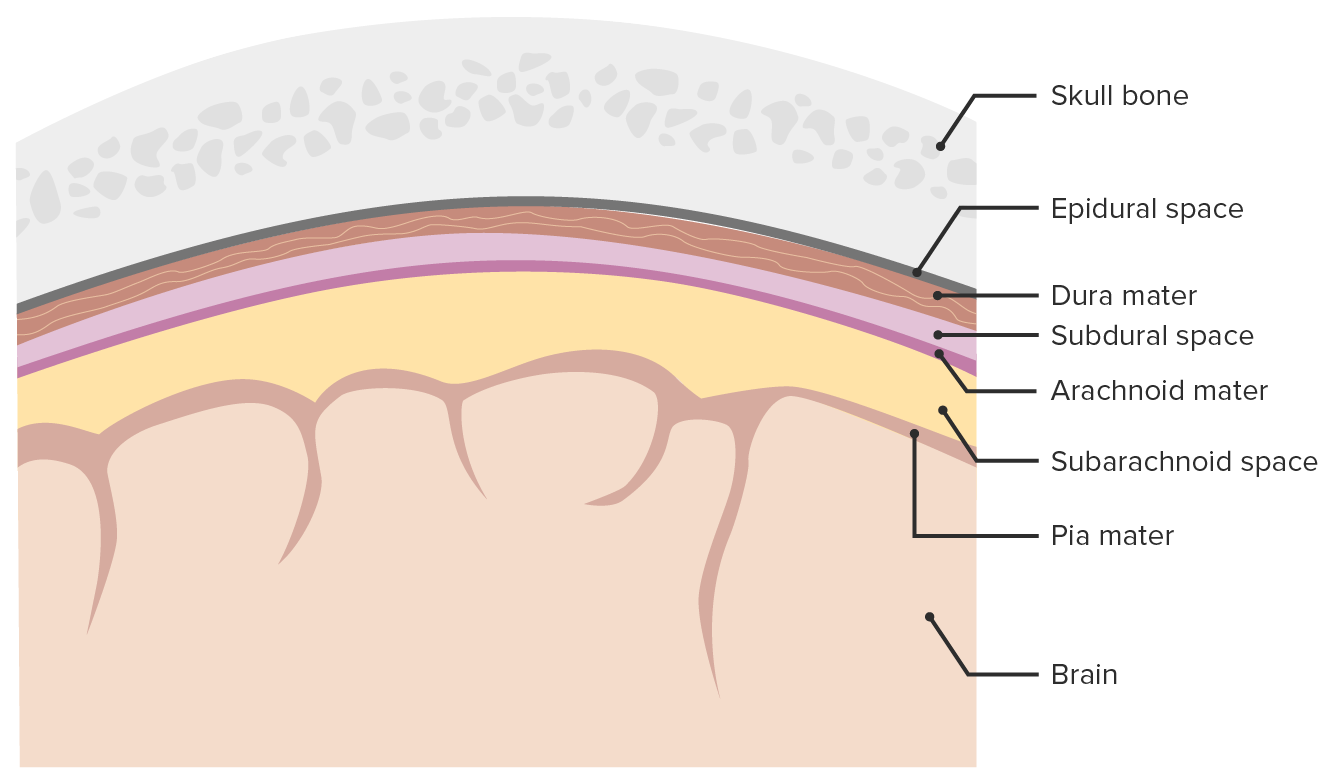
Meninges e espaços meníngeos:
Imagem que descreve as 3 camadas (dura-máter, aracnoide, pia-máter) em redor do cérebro e da medula espinhal. As meninges servem de proteção mecânica do SNC, sustentam os vasos sanguíneos cerebrais e espinhais e permitem a passagem do LCR. Só o espaço subaracnoide é um verdadeiro espaço presente em condições fisiológicas, enquanto que os espaços epidural e subdural se formam apenas durante processos patológicos. O espaço epidural pode abrir como resultado de traumatismo cranioencefálico ou, raramente, devido a outros processos patológicos.
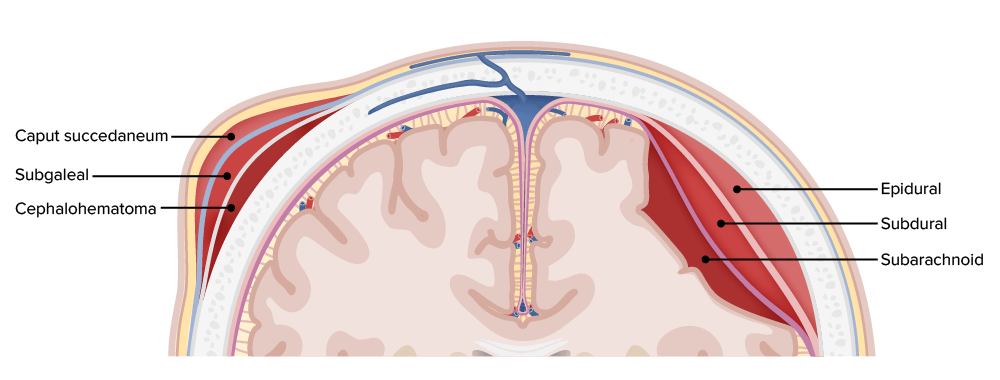
Hemorragias por localização dentro das diferentes camadas das meninges e do escalpe
Imagem por Lecturio.Trauma cranioencefálico:
Anticoagulação ou coagulopatia:
Atrofia cerebral:
Hemorragia intracerebral:
Rotura de aneurisma da vasculatura cerebral:
Malformações da vasculatura cerebral:
Tumor Tumor Inflammation cerebral:
Hipotensão intracraniana:
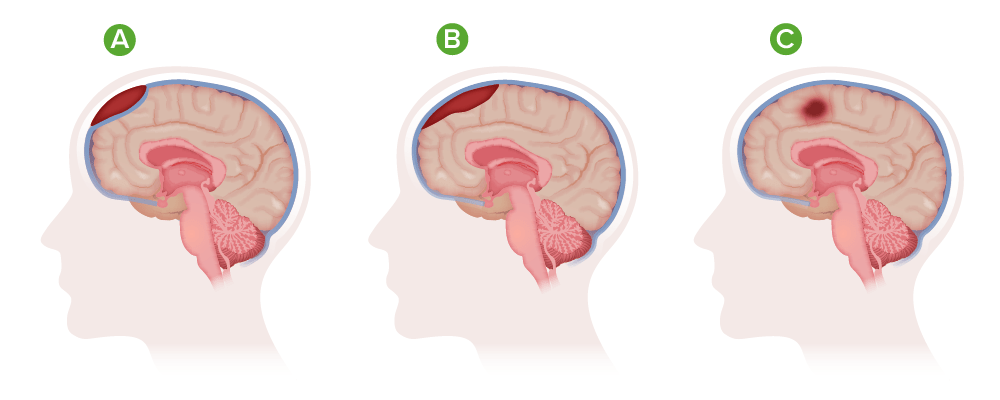
Tipos de hematoma
A) Hematoma epidural;
B) Hematoma subdural;
C) Hematoma intracraniano
O traumatismo cranioencefálico é a etiologia mais MAIS Androgen Insensitivity Syndrome comum de HSD, na maioria das vezes traumas leves (e.g., queda ao nível do solo) num indivíduo idoso.
O diagnóstico de HSD deve ser suspeitado em qualquer pessoa idosa que apresente traumatismo cranioencefálico, estado mental alterado, diminuição do nível de consciência ou sinais/sintomas neurológicos. A TAC cerebral deve ser realizada de emergência se suspeita de HSD aguda.
TAC cerebral sem contraste:
RM cerebral:
Angiografia:
Punção lombar:
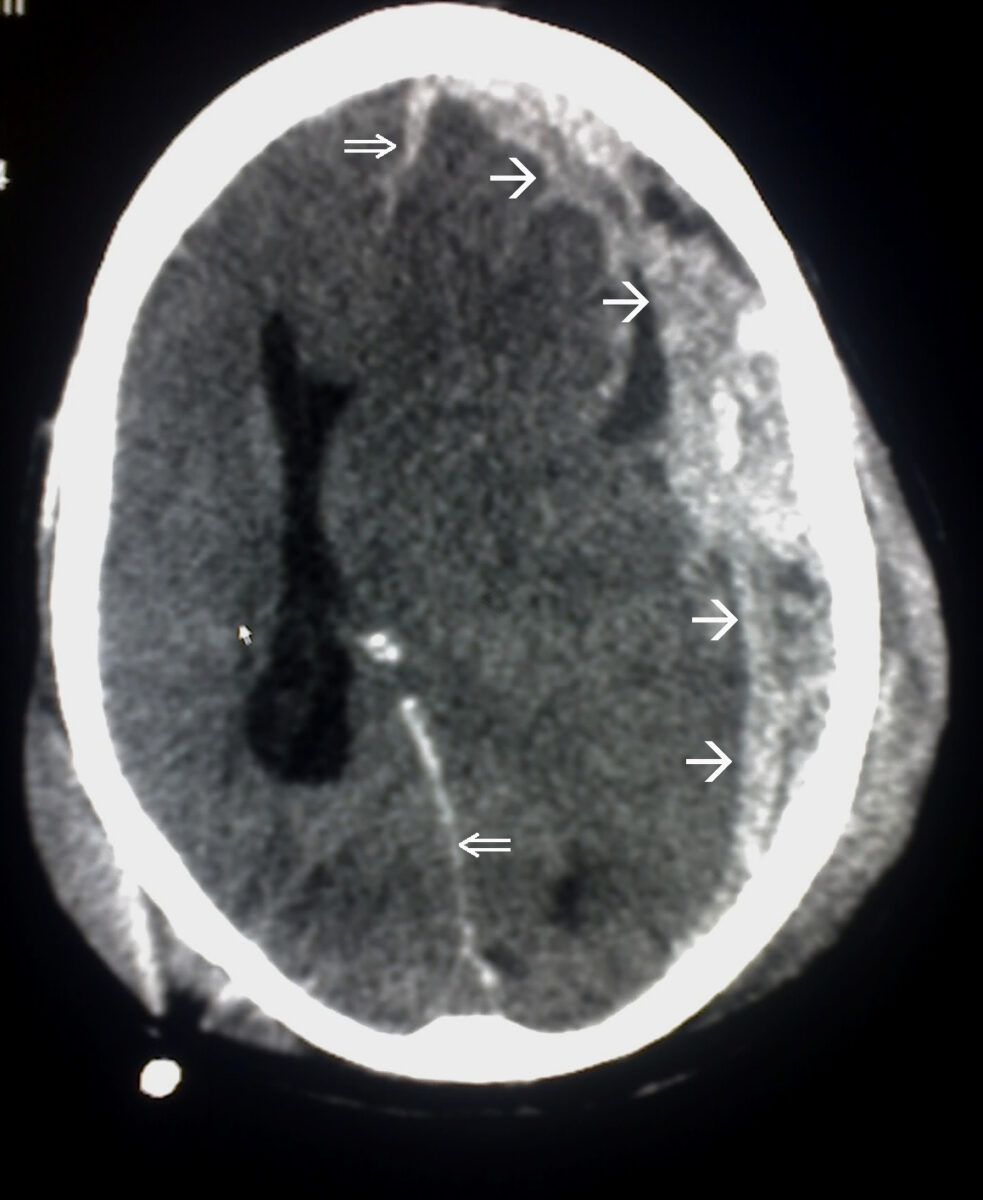
Hemorragia subdural:
Observar a convexidade do hematoma e o desvio da linha média associado (com distorção da anatomia cerebral e obliteração do ventrículo lateral).
A HSD aguda, especialmente aquela que se apresenta com comprometimento neurológico ou coma Coma Coma is defined as a deep state of unarousable unresponsiveness, characterized by a score of 3 points on the GCS. A comatose state can be caused by a multitude of conditions, making the precise epidemiology and prognosis of coma difficult to determine. Coma, é uma situação neurológica emergente que frequentemente requer intervenção cirúrgica. A falha em estabilizar, diagnosticar, avaliar e intervir prontamente pode resultar em expansão hemorrágica, lesão cerebral do parênquima, PIC elevada, herniação cerebral e morte.
As ferramentas de decisão clínica usadas para determinar entre o tratamento cirúrgico ou não cirúrgico incluem: