A terapêutica antirretroviral (TARV) tem como alvo o ciclo de replicação do vírus da imunodeficiência humana (VIH), sendo classificada com base na enzima ou mecanismo viral que é inibido. O objetivo do tratamento é suprimir a replicação viral de forma a alcançar o resultado de carga viral não detetada. Atualmente, são usados inibidores da transcriptase reversa, protease Protease Enzyme of the human immunodeficiency virus that is required for post-translational cleavage of gag and gag-pol precursor polyproteins into functional products needed for viral assembly. HIV protease is an aspartic protease encoded by the amino terminus of the pol gene. HIV Infection and AIDS, integrase Integrase Enzyme of the human immunodeficiency virus that is required to integrate viral DNA into cellular DNA in the nucleus of a host cell. HIV integrase is a DNA nucleotidyltransferase encoded by the pol gene. HIV Infection and AIDS e inibidores de entrada em regimes combinados de TARV (cTARV). A terapêutica combinada (esquema de 3 fármacos) é utilizada para prevenir a resistência farmacológica e a resistência cruzada, que se desenvolvem através de mutações genéticas.
Last updated: Dec 15, 2025
Contents
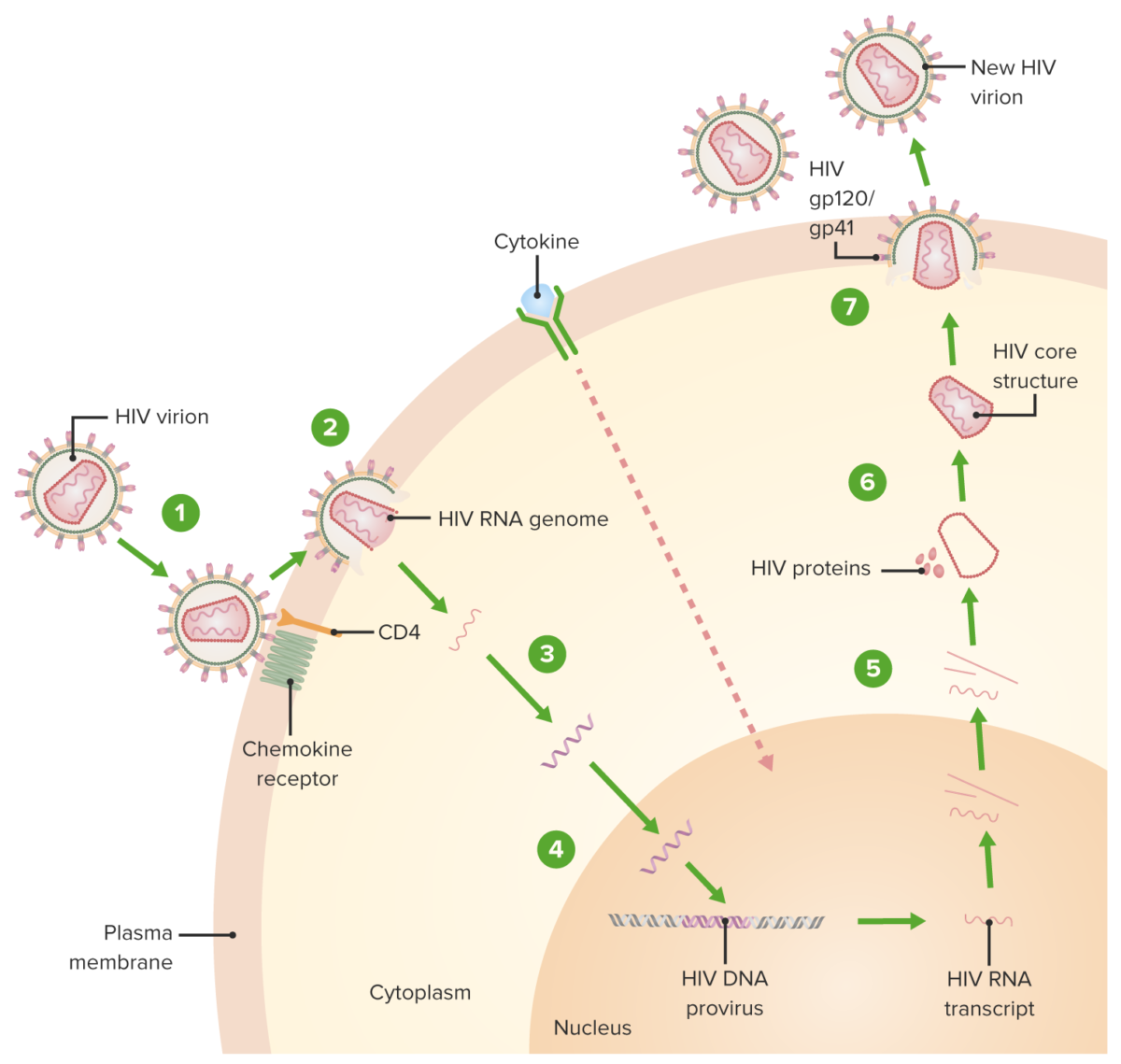
Ciclo de replicação do VIH:
1. O virião liga-se a um recetor CD4 e de quimiocina, sofrendo uma mudança conformacional que facilita a sua fusão e da célula hospedeira.
2. O virião vai perdendo o invólucro de proteína da cápside (que envolve o RNA viral e proteínas) à medida que atravessa o citoplasma.
3. Ocorre a síntese de DNA pró-viral mediada por transcriptase reversa.
4. O DNA viral é transportado através do núcleo e integrado no DNA do hospedeiro, sendo o processo facilitado pela integrase.
5. O DNA viral é transcrito, originando múltiplas cópias do novo RNA do VIH que são transportadas para o citoplasma. O novo RNA do VIH torna-se o genoma de um novo vírus. Ocorre ainda a ativação de citocinas da célula.
6. O novo RNA viral + proteínas + enzimas movem-se para a superfície celular e formam uma partícula não infeciosa.
7. A partícula (RNA viral + proteínas) abandona a célula hospedeira com o VIH imaturo. A proteína protease viral (enzima) cliva as poliproteínas recém-sintetizadas produzindo um VIH maduro.
| Tipo de fármaco | Mecanismo de ação |
|---|---|
Inibidores da transcriptase reversa
|
|
| Inibidores da transferência de cadeia da integrase Integrase Enzyme of the human immunodeficiency virus that is required to integrate viral DNA into cellular DNA in the nucleus of a host cell. HIV integrase is a DNA nucleotidyltransferase encoded by the pol gene. HIV Infection and AIDS (INSTIs, pela sigla em inglês) |
|
| Inibidores da protease Protease Enzyme of the human immunodeficiency virus that is required for post-translational cleavage of gag and gag-pol precursor polyproteins into functional products needed for viral assembly. HIV protease is an aspartic protease encoded by the amino terminus of the pol gene. HIV Infection and AIDS (IPs, pela sigla em inglês) |
|
Inibidores de entrada:
|
|
| Inibidor pós-fixação | Liga-se à molécula CD4, bloqueando a entrada viral, mas não a ligação |
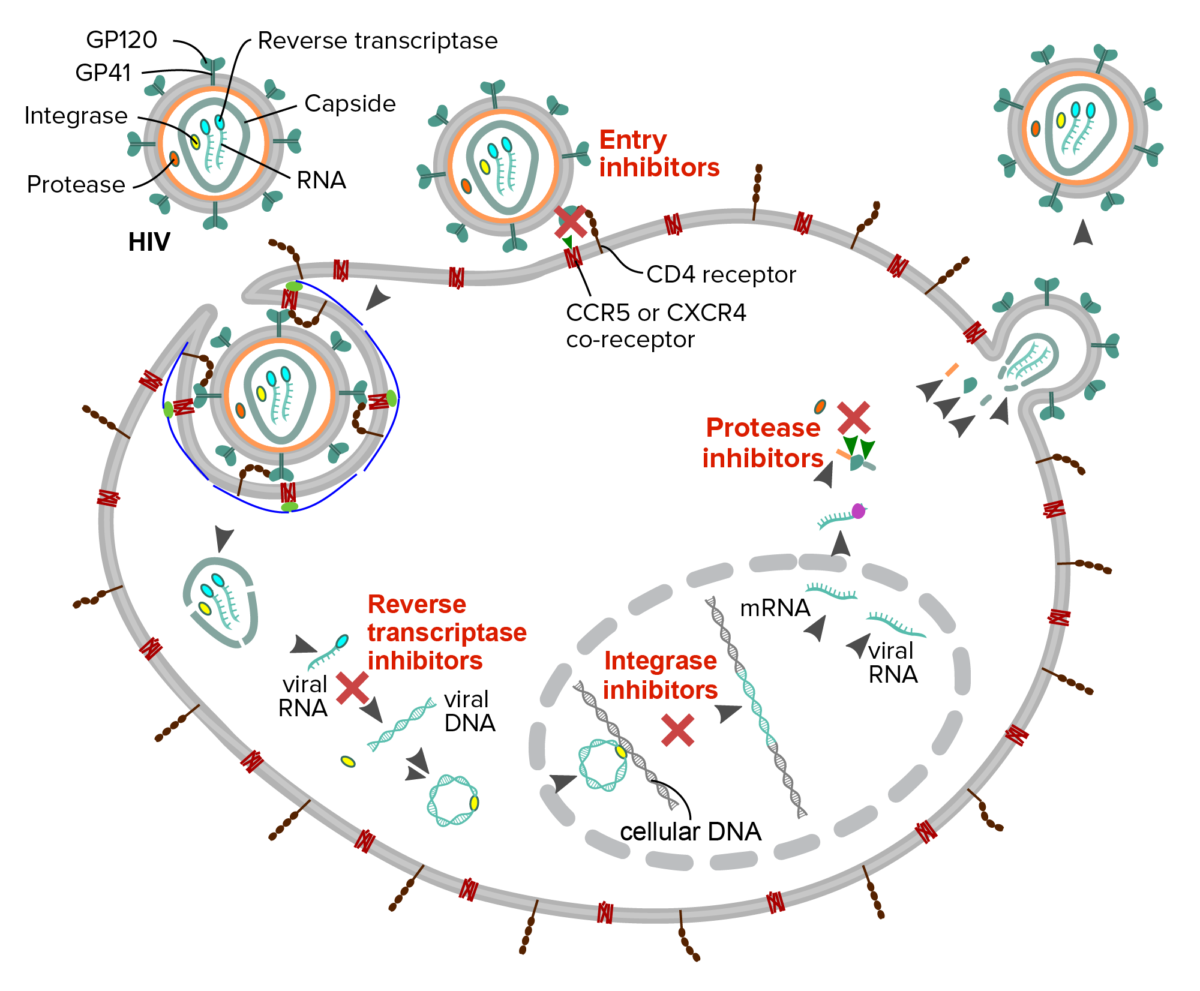
Descrição esquemática do mecanismo das 4 classes de fármacos antirretrovirais contra o VIH:
Inibidores de fusão ou entrada: interferem na ligação, fusão ou entrada do vírus VIH
Inibidores da transcriptase reversa: interferem na tradução do RNA viral em DNA
Inibidores da integrase: impedem a inserção do genoma viral no DNA do hospedeiro
Inibidores da protease: bloqueiam a clivagem dos precursores proteicos necessários para a produção de partículas virais infeciosas
| Fármaco | Efeitos adversos | Interações/contra-indicações |
|---|---|---|
Zidovudina (AZT):
|
|
|
| Emtricitabina: estruturalmente semelhante à lamivudina |
|
Não associar lamivudina (os fármacos competem com a fosforilação intracelular). |
| Lamivudina: ativo contra o vírus da hepatite B |
|
Não associar emtricitabina (os fármacos competem com a fosforilação intracelular). |
| Abacavir Abacavir Anti-HIV Drugs | Reação de hipersensibilidade (potencialmente fatal): febre, erupção cutânea, dor abdominal, vómitos, dispneia |
|
| Tenofovir Tenofovir An adenine analog reverse transcriptase inhibitor with antiviral activity against HIV-1 and hepatitis b. It is used to treat HIV infections and chronic hepatitis b, in combination with other antiviral agents, due to the emergence of antiviral drug resistance when it is used alone. Anti-HIV Drugs (NtRTI): TAF e TDF (TAF: ativo contra o vírus da hepatite B) |
|
|
Inibidores não competitivos da transcriptase reversa:
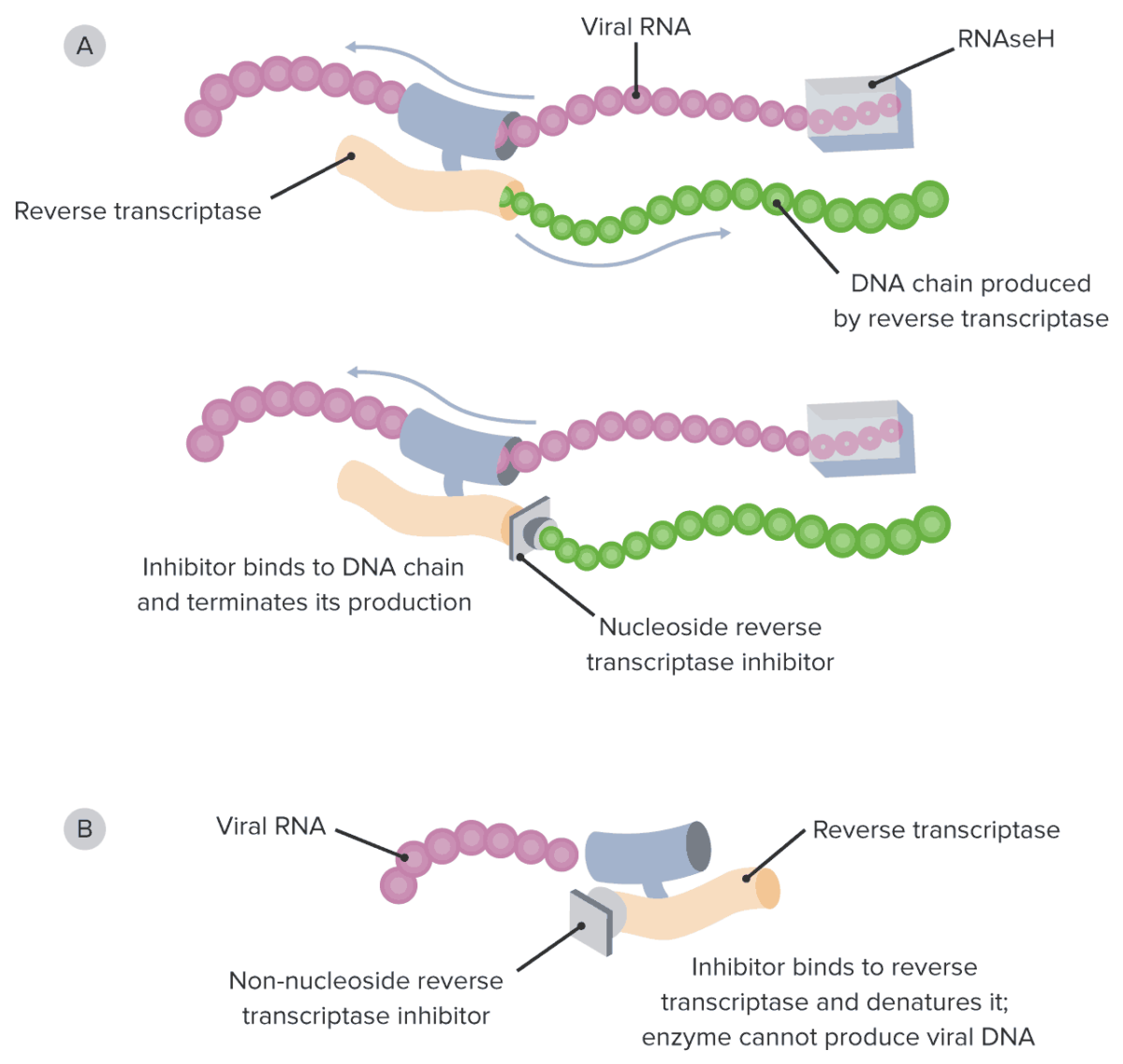
Diagrama do mecanismo de ação dos NRTIs e NNRTIs:
R: Os NRTIs bloqueiam o genoma do DNA viral em crescimento e substituem os nucleótidos naturais, atuando como terminadores de cadeia.
B: Por outro lado, os NNRTIs ligam-se diretamente à enzima transcriptase reversa, impedindo diretamente a síntese de DNA viral.
NRTI: inibidor nucleótido da transcriptase reversa
NNRTI: inibidor não nucleótido da transcriptase reversa
RNAseH: ribonuclease H
| Fármaco | Efeitos adversos | Interações/contra-indicações |
|---|---|---|
| Etravirina: NNRTI mais MAIS Androgen Insensitivity Syndrome usado em casos de VIH resistentes |
|
Pode interagir com outros antirretrovirais (por exemplo, a dose de maraviroc Maraviroc A cyclohexane and triazole derivative that acts as an antagonist of the ccr5 receptor. It prevents infection by HIV-1 virus strains which use ccr5 as a co-receptor for membrane fusion and cellular entry. Anti-HIV Drugs deve ser dobrada se usado em combinação) |
| Efavirenz Efavirenz Anti-HIV Drugs |
|
Evitar nos casos com síndrome do QT longo, doença hepática, doença psiquiátrica |
| Doravirina | Efeitos no SNC/psiquiátricos semelhantes ao efavirenz Efavirenz Anti-HIV Drugs (mas muito menos comuns) | O uso concomitante com rifampicina está contraindicado (↓ exposição à doravirina) |
| Rilpivirina |
|
|
| Nevirapina: não está indicada no tratamento inicial (↑ toxicidade) |
|
|
| Fármaco | Efeitos adversos | Interações/contra-indicações |
|---|---|---|
| Atazanavir Atazanavir Anti-HIV Drugs |
|
|
| Darunavir |
|
|
| Ritonavir Ritonavir An HIV protease inhibitor that works by interfering with the reproductive cycle of HIV. It also inhibits cytochrome p-450 cyp3a. Anti-HIV Drugs: reforço |
|
Um dos inibidores mais MAIS Androgen Insensitivity Syndrome potentes do CYP3A4 CYP3A4 Class 3 Antiarrhythmic Drugs (Potassium Channel Blockers); evitar tomar fármacos com índice terapêutico estreito. |
| Lopinavir Lopinavir An HIV protease inhibitor used in a fixed-dose combination with ritonavir. It is also an inhibitor of cytochrome p-450 cyp3a. Anti-HIV Drugs: coformulado com ritonavir Ritonavir An HIV protease inhibitor that works by interfering with the reproductive cycle of HIV. It also inhibits cytochrome p-450 cyp3a. Anti-HIV Drugs |
|
Não está indicado no tratamento inicial (devido à sua potência e toxicidade) |
| Fármaco | Efeitos adversos | Interações/contra-indicações |
|---|---|---|
| Raltegravir Raltegravir Anti-HIV Drugs |
|
Os indutores enzimáticos (por exemplo, a rifampicina) aumentam o seu metabolismo, induzindo a UDP-glucuronosiltransferase. |
| Dolutegravir Dolutegravir Anti-HIV Drugs | Aumento ligeiro e reversível da creatinina (inibe o transportador renal, OCT2) |
|
| Elvitegravir Elvitegravir Anti-HIV Drugs: administrado com cobicistate ou ritonavir Ritonavir An HIV protease inhibitor that works by interfering with the reproductive cycle of HIV. It also inhibits cytochrome p-450 cyp3a. Anti-HIV Drugs | Sintomas gastrointestinais | Atualmente disponível apenas numa combinação de dose fixa com tenofovir Tenofovir An adenine analog reverse transcriptase inhibitor with antiviral activity against HIV-1 and hepatitis b. It is used to treat HIV infections and chronic hepatitis b, in combination with other antiviral agents, due to the emergence of antiviral drug resistance when it is used alone. Anti-HIV Drugs, emtricitabina e cobicistate (que ↑ interações medicamentosas) |
| Bictegravir Bictegravir Anti-HIV Drugs: coformulado com emtricitabina e TAF |
|
A ingestão com rifampicina ou dofetilida está contraindicada |

Diagrama esquemático da entrada viral e etapas inibidas por enfuvirtida e maraviroc:
A subunidade trimérica gp120 do complexo de glicoproteínas do envelope viral liga-se ao CD4 na superfície da célula alvo, desencadeando uma mudança conformacional que promove interações com recetores de quimiocinas (neste caso, CCR5). A subunidade transmembranar trimérica gp41 é ativada para mediar a fusão da membrana, de forma a que o conteúdo viral possa entrar na célula. O maraviroc bloqueia o correcetor CCR5. A enfuvirtida liga-se à gp41, impedindo a fusão.