A deficiência de mieloperoxidase (MPO) é uma doença hereditária ou adquirida causada por mutações no gene MPO no cromossoma 17, o que leva a uma deficiência de MPO em neutrófilos e monócitos. Esta deficiência prejudica particularmente a destruição de patógenos nos fagolisossomos. Embora a maioria dos doentes esteja assintomática e não sofra de uma frequência aumentada de infeções, uma minoria (particularmente doentes diabéticos) pode desenvolver infeções fúngicas graves. A coloração histoquímica de neutrófilos para MPO pode fornecer o diagnóstico. Não há tratamento específico para a deficiência de MPO e não são indicados antibióticos profiláticos.
Última atualização: Jan 5, 2025
Mutação genética:
Deficiência primária de MPO:
Deficiência adquirida (secundária) de MPO:
Os neutrófilos são a primeira linha de defesa contra patogénios:
Neutrófilos deficientes em MPO:
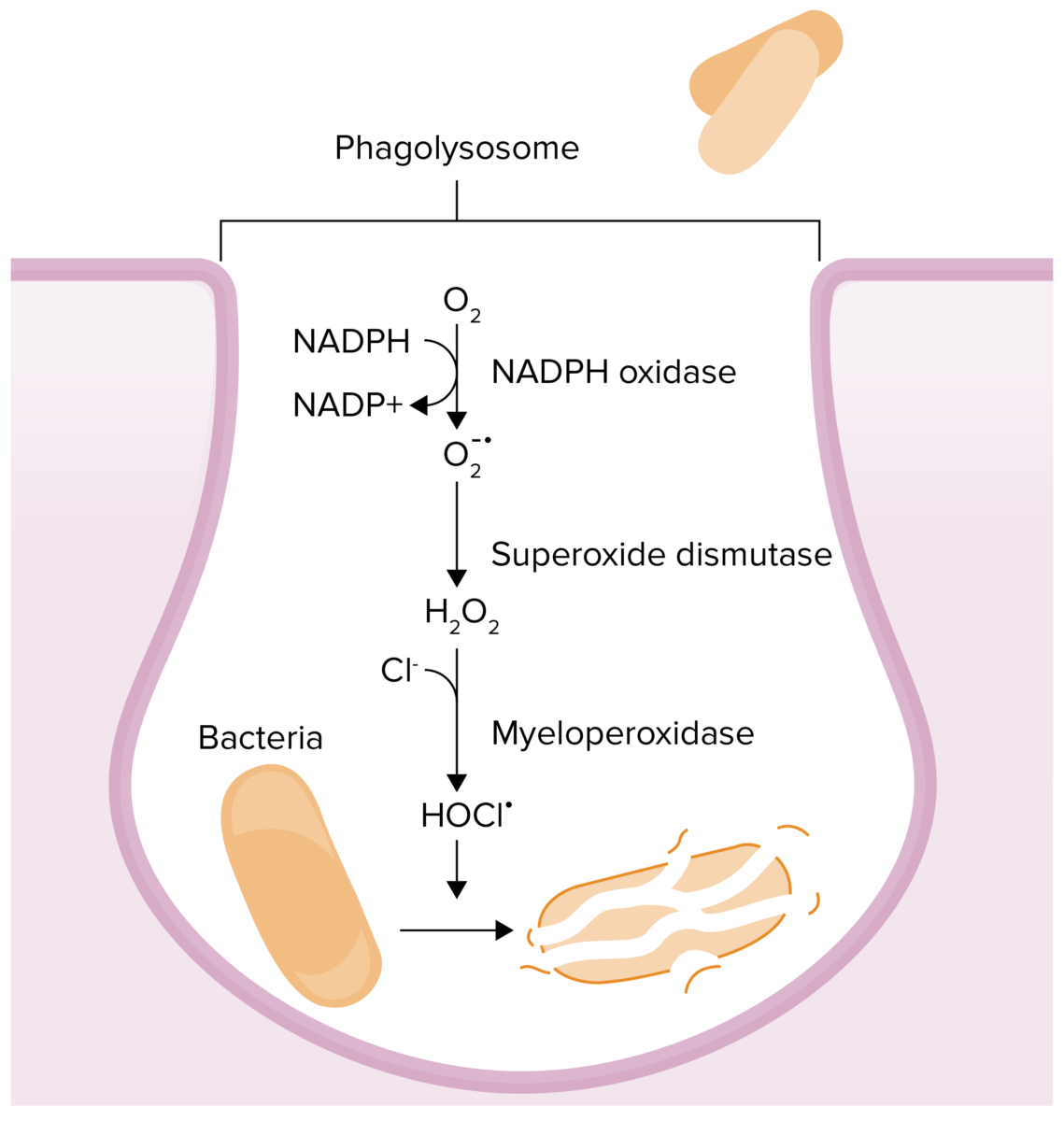
Reações químicas que ocorrem em fagolisossomas num esforço para matar um patogénio:
A deficiência de mieloperoxidase resulta na incapacidade de converter o peróxido de hidrogénio em ácido hipocloroso.
Como a maioria dos doentes é assintomática, não é necessário nenhum tratamento específico para a deficiência de MPO.