A via das pentoses fosfato (também conhecida como hexose monofosfato (HMP) shunt)) é um importante processo fisiológico que pode ocorrer em 2 fases: oxidativa e não oxidativa. A fase oxidativa utiliza glicose-6-fosfato para produzir nicotinamida adenina dinucleotídeo fosfato ( NADPH NADPH Nicotinamide adenine dinucleotide phosphate. A coenzyme composed of ribosylnicotinamide 5'-phosphate (nmn) coupled by pyrophosphate linkage to the 5'-phosphate adenosine 2. Pentose Phosphate Pathway) e ribulose-5-fosfato (que pode ser convertida em ribose-5-fosfato). A fase não oxidativa é uma coleção de várias reações reversíveis nas quais os intermediários estão conectados a várias outras vias, incluindo síntese de nucleotídeos, síntese de aminoácidos aromáticos e glicólise.
Last updated: Apr 17, 2025
A via das pentoses fosfato origina, através de várias reações, moléculas de fosfato de dinucleotídeo de nicotinamida e adenina ( NADPH NADPH Nicotinamide adenine dinucleotide phosphate. A coenzyme composed of ribosylnicotinamide 5′-phosphate (nmn) coupled by pyrophosphate linkage to the 5′-phosphate adenosine 2. Pentose Phosphate Pathway, pela sigla em inglês) e ribose-5-fosfato. Esta via ocorre paralelamente à glicólise.
A via das pentoses fosfato ocorre no citoplasma das células.
A via das pentoses fosfato origina intermediários, que são utilizados para variados fins:
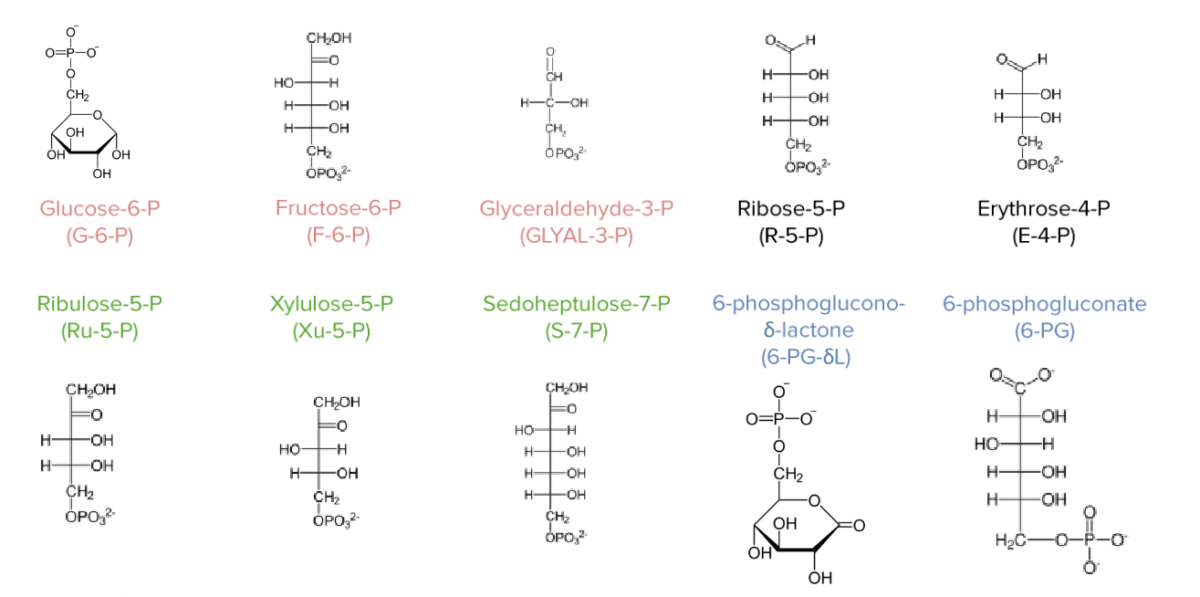
Intermediários da via das pentoses fosfato:
A glicose-6-fosfato (G-6-P), frutose-6-fosfato (F-6-P) e gliceraldeído-3-fosfato (GLYAL-3-P) são intermediários da glicólise. A ribose-5-fosfato (R-5-P) é utilizada na síntese de nucleotídeos, enquanto a eritrose-4-fosfato (E-4-P) é utilizada na síntese de aminoácidos aromáticos. Na linha inferior encontram-se representados os açúcares que raramente, ou nunca, são encontrados fora da via das pentoses fosfato.
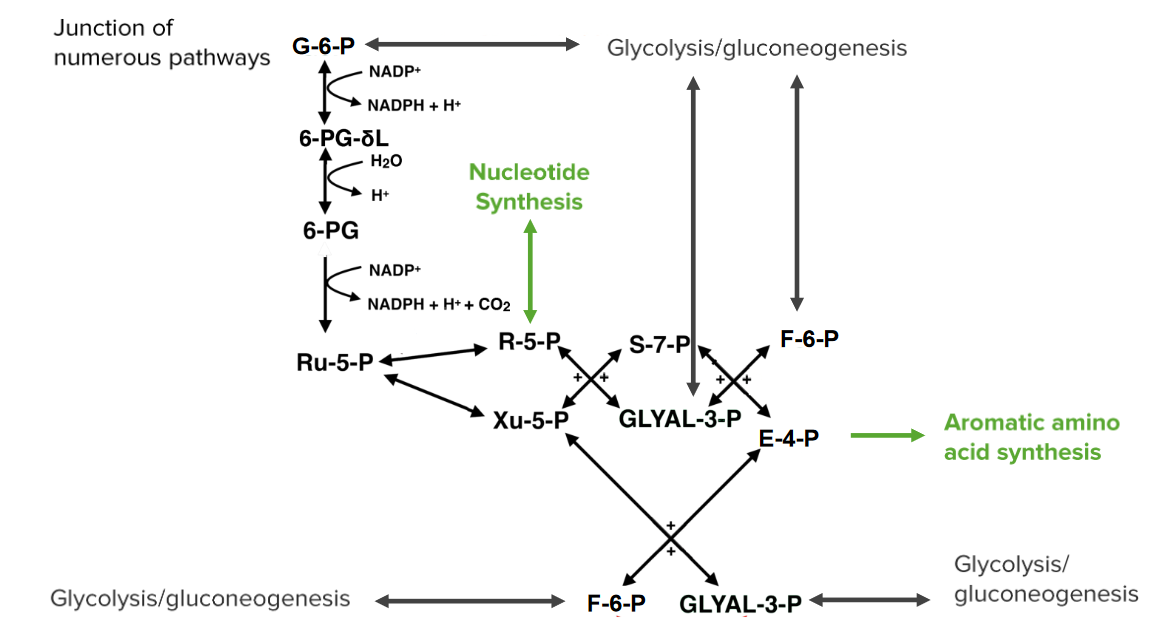
A via das pentoses fosfato funciona como um ponto de combinação entre várias vias.
A imagem apresentada mostra os múltiplos pontos de entrada e saída de metabólitos, incluindo a síntese de nucleotídeos, síntese de aminoácidos aromáticos, glicólise e gliconeogênese
NADPH: fosfato dinucleotídeo de nicotinamida e adenina
P: Fosfato
G: Glicose
PG: Fosfogluconato
L: Lactona
Ru: Ribulose
R: Ribose
Xu: xilulose
S: Sedoheptulose
GLIAL: gliceraldeído
A via das pentoses fostato é dividida em 2 fases principais:
A fase oxidativa consiste numa fase irreversível composta por 3 etapas.
Substratos iniciais:
Reações:
Produtos finais:
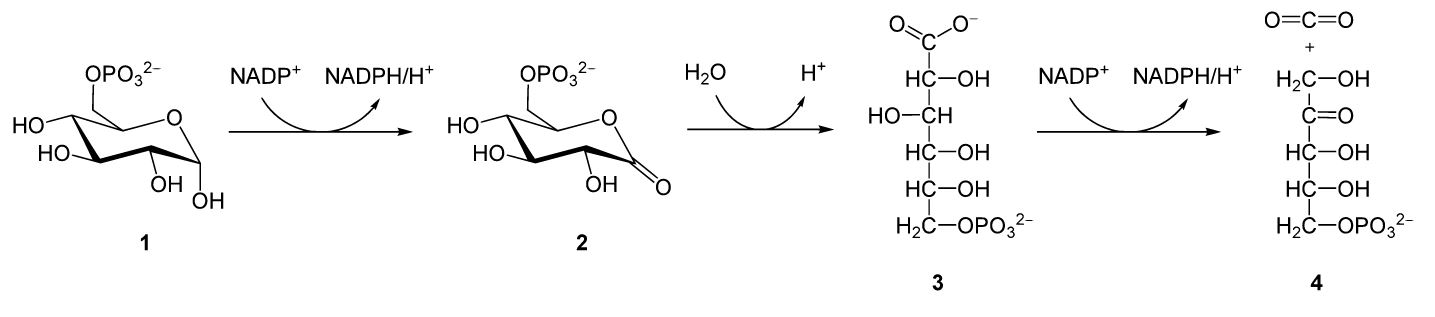
Na fase oxidativa ocorre a conversão da glicose-6-fosfato (1) em ribulose-5-fosfato (4), dando origem a 2 moléculas de NADPH.
NADPH: Fosfato dinucleotídeo de nicotinamida e adenina
A fase não oxidativa é reversível e utiliza as isomerases Isomerases A class of enzymes that catalyze geometric or structural changes within a molecule to form a single product. The reactions do not involve a net change in the concentrations of compounds other than the substrate and the product. Basics of Enzymes para formar os intermediários dos açúcares, que são utilizados na glicólise e na biossíntese de nucleotídeos.
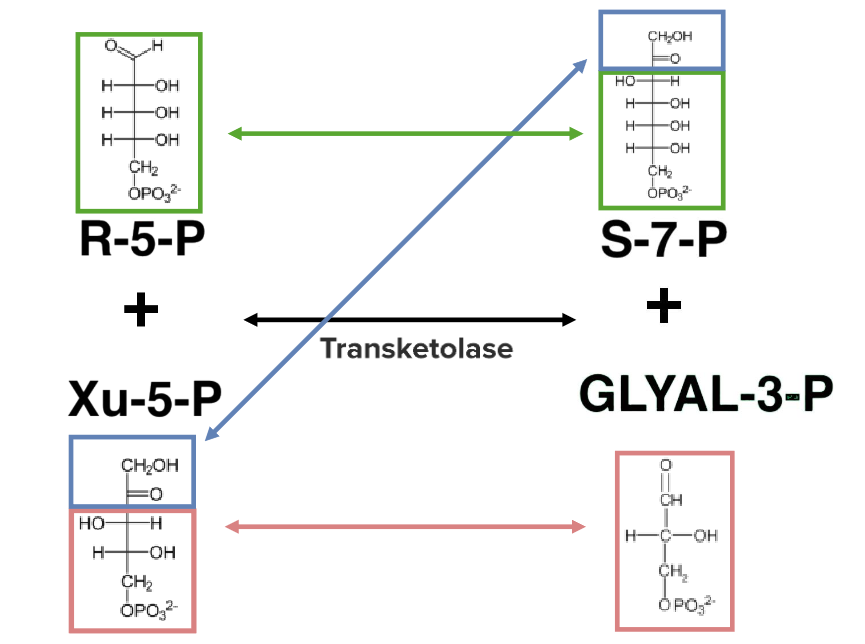
Rearranjo dentro da fase não oxidativa da via das pentose fosfato:
A transcetolase transfere 2 carbonos de xilulose-5-fosfato (Xu-5-P) para ribose-5-fosfato (R-5-P) para produzir sedo-heptulose-7-fosfato (S-7-P) e gliceraldeído-3-fosfato (GLICAL-3-P).
Rearranjo na fase não oxidativa da via das pentoses fosfato:
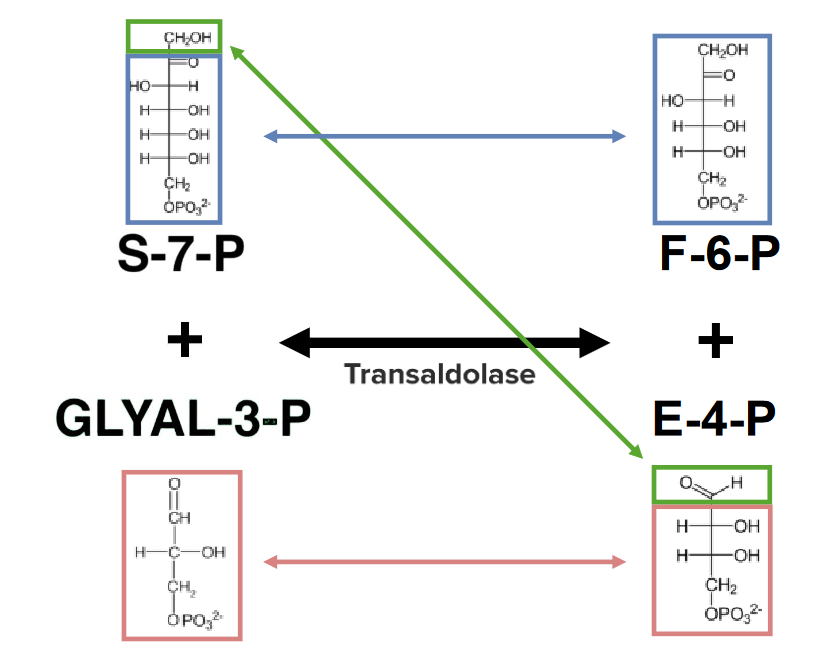
A transaldolase transfere um carbono de sedoheptulose-7-fosfato (S-7-P) para gliceraldeído-3-fosfato (GLYCAL-3-P) para produzir eritrose-4-fosfato (E-4-P) e frutose-6-fosfato (F-6-P).
Rearranjo na fase não oxidativa da via das pentoses fosfato:
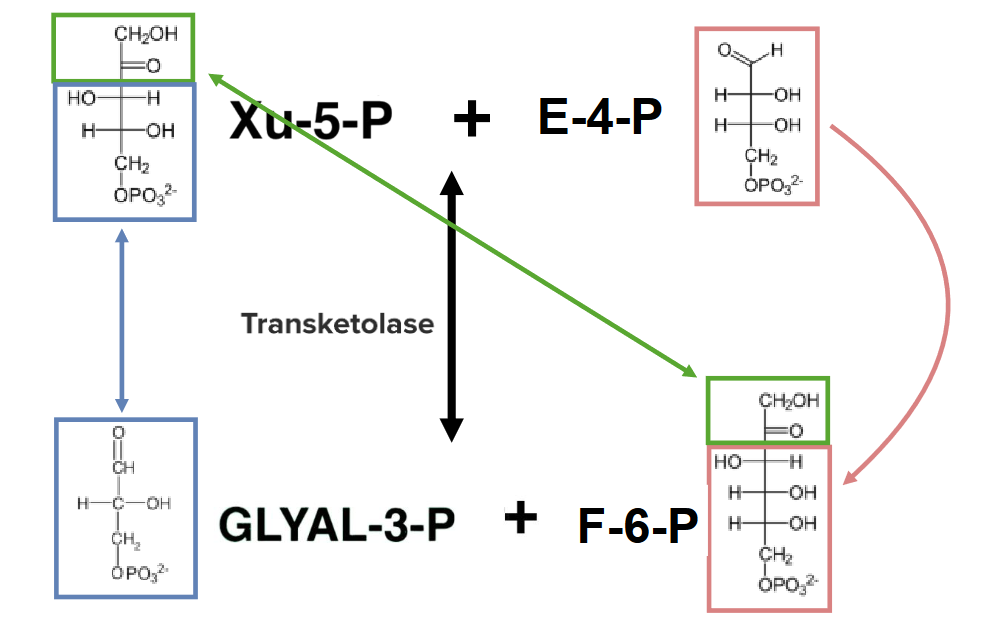
A transcetolase transfere 2 carbonos de xilulose-5-fosfato (Xu-5-P) para eritrose-4-fosfato (E-4-P) para produzir a frutose-6-fosfato (F-6-P) e o gliceraldeído-3-fosfato (GLIAL-3-P).