El virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology de Lassa, parte de la familia Arenaviridae Arenaviridae A family of RNA viruses naturally infecting rodents and consisting of one genus (arenavirus) with two groups: old world arenaviruses and new world arenaviruses. Infection in rodents is persistent and silent. Vertical transmission is through milk-, saliva-, or urine-borne routes. Horizontal transmission to humans, monkeys, and other animals is important. Lassa Virus, es un virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology de ARN monocatenario que causa la fiebre de Lassa, un tipo de enfermedad hemorrágica viral. El virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology es endémico de partes de África Occidental (Sierra Leona, Liberia, Guinea y Nigeria) y países vecinos. El reservorio es la rata multimamada ( Mastomys natalensis Mastomys natalensis Lassa Virus), y la transmisión es por inhalación o contacto con excreciones de roedores o el consumo de estos animales. También puede ocurrir la transmisión de persona a persona. La mayoría de los LOS Neisseria pacientes infectados son asintomáticos. Sin embargo, los LOS Neisseria pacientes sintomáticos presentan fiebre, malestar, cefalea, vómitos y dolor Dolor Inflammation torácico, estos síntomas pueden progresar a hemorragia, hipovolemia y shock Shock Shock is a life-threatening condition associated with impaired circulation that results in tissue hypoxia. The different types of shock are based on the underlying cause: distributive (↑ cardiac output (CO), ↓ systemic vascular resistance (SVR)), cardiogenic (↓ CO, ↑ SVR), hypovolemic (↓ CO, ↑ SVR), obstructive (↓ CO), and mixed. Types of Shock. El tratamiento es principalmente con ribavirina y terapia de soporte. No existe una vacuna eficaz, pero las medidas preventivas como evitar la exposición a los LOS Neisseria roedores y el uso de equipo de protección personal pueden reducir la transmisión. La ribavirina también se administra como profilaxis posterior a la exposición.
Last updated: Dec 15, 2025
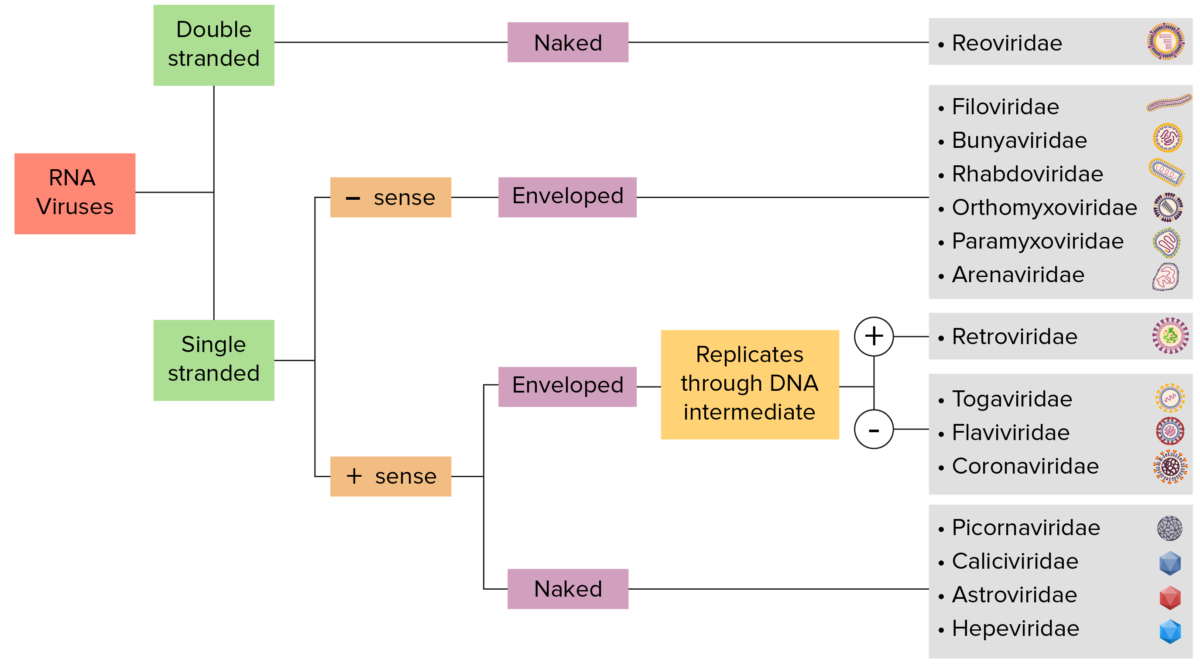
Identificación de los virus ARN:
Los virus pueden clasificarse de muchas maneras. Sin embargo, la mayoría de los virus tienen un genoma formado por ADN o ARN. Los virus con genoma ARN pueden caracterizarse además por tener ARN monocatenario o bicatenario. Los virus “envueltos” están cubiertos por una fina capa de membrana celular (normalmente tomada de la célula huésped). Si la envoltura está ausente, los virus se denominan “desnudos”. Los virus con genomas monocatenarios son positivos si el genoma se emplea directamente como ARN mensajero (ARNm), que se traduce en proteínas. Los virus monocatenarios negativos emplean la ARN polimerasa, una enzima viral, para transcribir su genoma en ARN mensajero.
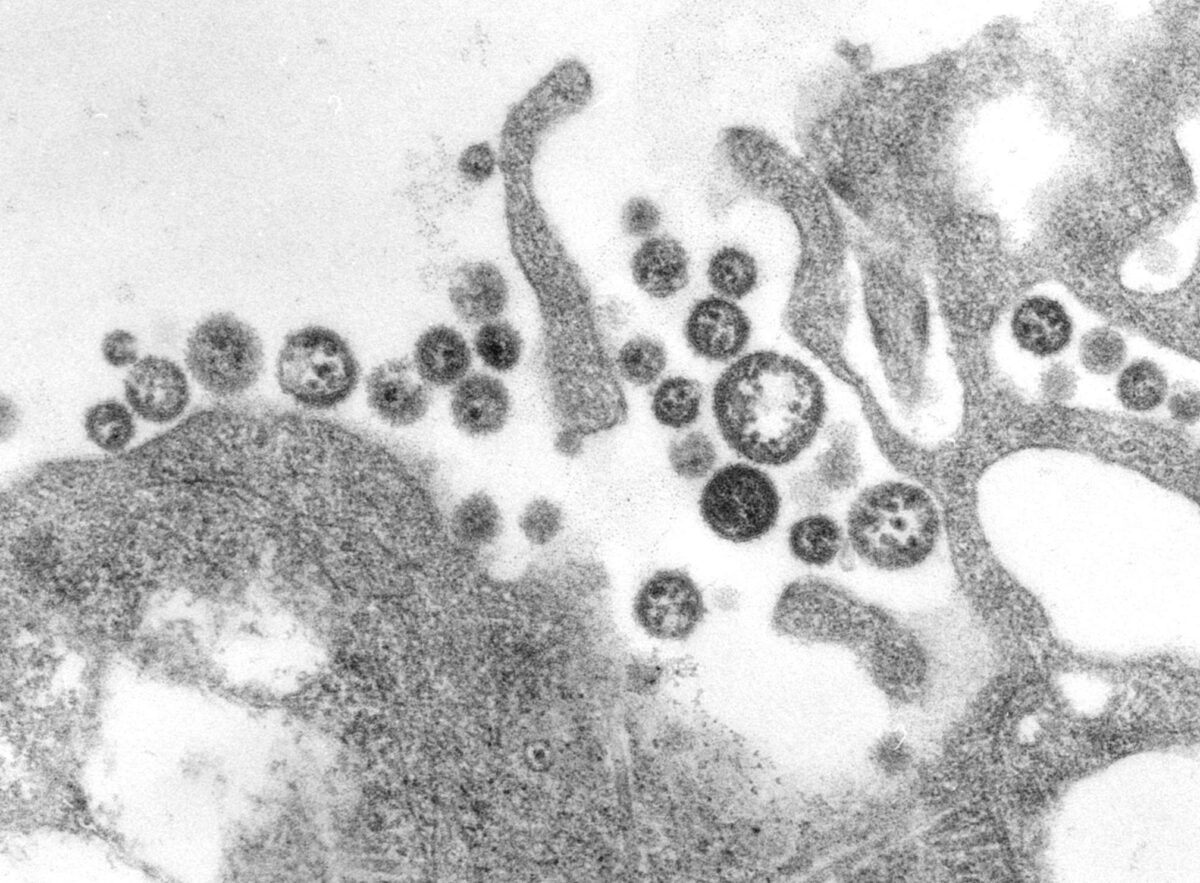
An electron micrograph of Lassa virus virions
Image: “A transmission electron micrograph (TEM) of a number of Lassa virus virions adjacent to some cell debris” by CDC/C. S. Goldsmith. License: Public Domain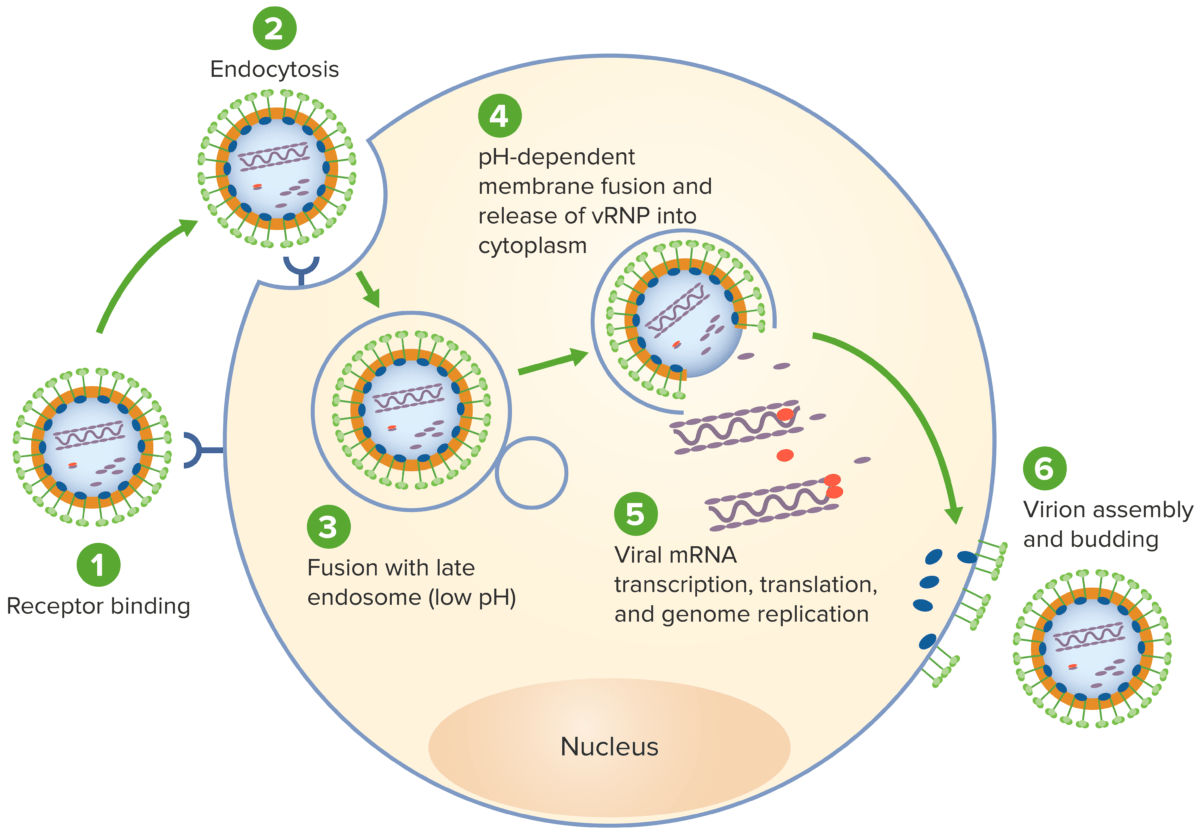
El ciclo de vida del virus Lassa:
El virus se une a los receptores del huésped a través de las glicoproteínas de la envoltura.
El virus es posteriormente endocitado, consiguiendo así la entrada en la célula.
A continuación se produce la fusión del virus con un endosoma.
El virus se fusiona con la membrana del endosoma, lo que permite la liberación de la ribonucleocápside viral en el citoplasma.
La ARN polimerasa dependiente de ARN (RdRP) media la replicación y transcripción del gen viral en el citoplasma del huésped.
Se ensamblan nuevos viriones y se produce la gemación, liberando el virión para infectar otras células.
vRNP: ribonucleoproteína viral
Los LOS Neisseria arenavirus pueden causar fiebres hemorrágicas ( virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology de Lassa) y/o enfermedad neurológica ( virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology de la coriomeningitis linfocítica).
| Organismo | LCMV LCMV Lymphocytic choriomeningitis virus (LCMV) is a single-stranded RNA virus transmitted to humans via rodents, the primary reservoir. Viral infections can occur through direct contact (such as through a break in the skin) with rodent urine, saliva, or droppings or via inhalation of aerosolized virus. The disease typically results in a self-limited, febrile, biphasic disease. Lymphocytic Choriomeningitis Virus | Virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology de Lassa |
|---|---|---|
| Familia | Arenaviridae Arenaviridae A family of RNA viruses naturally infecting rodents and consisting of one genus (arenavirus) with two groups: old world arenaviruses and new world arenaviruses. Infection in rodents is persistent and silent. Vertical transmission is through milk-, saliva-, or urine-borne routes. Horizontal transmission to humans, monkeys, and other animals is important. Lassa Virus | Arenaviridae Arenaviridae A family of RNA viruses naturally infecting rodents and consisting of one genus (arenavirus) with two groups: old world arenaviruses and new world arenaviruses. Infection in rodents is persistent and silent. Vertical transmission is through milk-, saliva-, or urine-borne routes. Horizontal transmission to humans, monkeys, and other animals is important. Lassa Virus |
| Género | Mammarenavirus Mammarenavirus Lassa Virus | Mammarenavirus Mammarenavirus Lassa Virus |
| Características |
|
|
| Reservorio | Roedores | Roedores |
| Transmisión |
|
|
| Progresión Clínica | Bifásico:
|
|
| Diagnóstico |
|
|
| Tratamiento |
|
|
| Prevención |
|
|
Otras fiebres hemorrágicas virales:
Condiciones causadas por otros patógenos no virales: