El virus de la coriomeningitis linfocítica es un virus de ARN monocatenario que se transmite a humanos a través de roedores, su reservorio principal. Las infecciones virales pueden ocurrir por contacto directo (como una herida en la piel) con orina, saliva o excrementos de roedores, o por inhalación de virus en aerosoles. La transmisión vertical y, en raras ocasiones, el trasplante de órganos también provoca infecciones. La enfermedad generalmente da como resultado una enfermedad bifásica febril autolimitada. En casos graves, los pacientes pueden presentar encefalitis, meningitis aséptica o meningoencefalitis. Las infecciones por el virus de la coriomeningitis linfocítica en mujeres embarazadas también se ha reconocido como un teratógeno importante que provoca la muerte fetal o defectos congénitos. El diagnóstico se realiza mediante serología o RT-PCR. El tratamiento es de soporte.
Última actualización: Jul 17, 2022
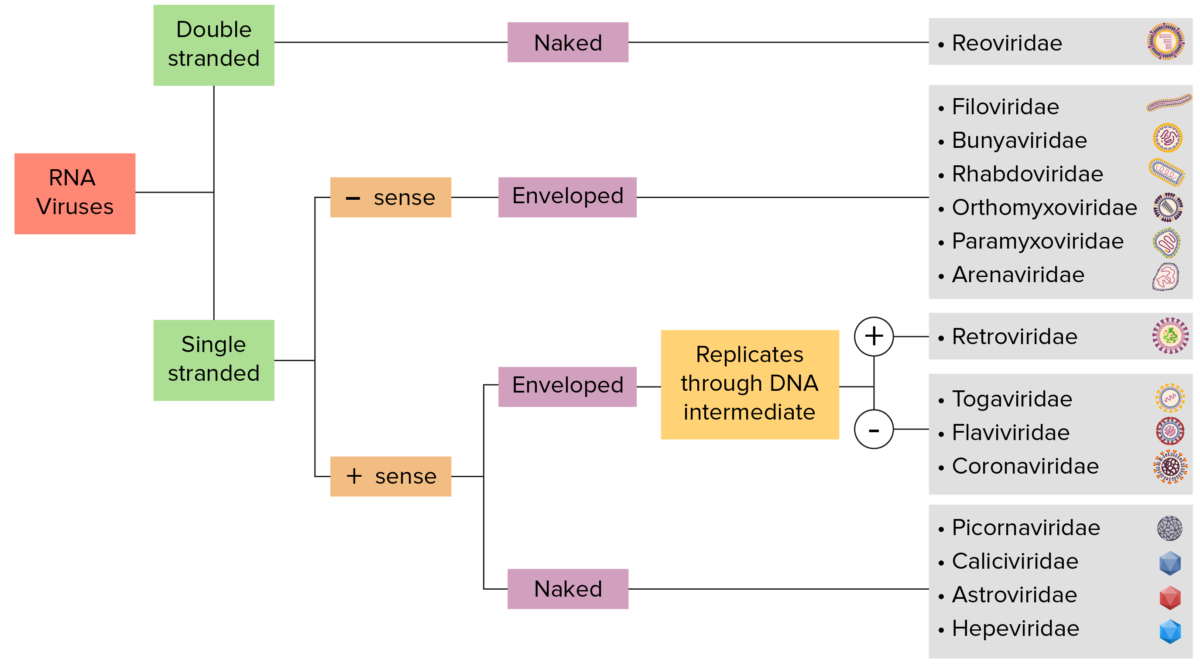
Identificación de los virus ARN:
Los virus pueden clasificarse de muchas maneras. Sin embargo, la mayoría de los virus tienen un genoma formado por ADN o ARN. Los virus con genoma ARN pueden caracterizarse además por tener ARN monocatenario o bicatenario. Los virus «envueltos» están cubiertos por una fina capa de membrana celular (normalmente tomada de la célula huésped). Si la envoltura está ausente, los virus se denominan «desnudos». Los virus con genomas monocatenarios son positivos si el genoma se emplea directamente como ARN mensajero (ARNm), que se traduce en proteínas. Los virus monocatenarios negativos emplean la ARN polimerasa, una enzima viral, para transcribir su genoma en ARN mensajero.
Taxonomía:
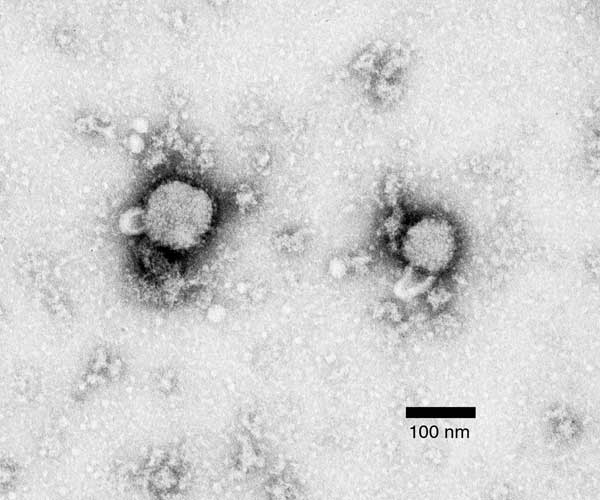
Micrografía electrónica del virus de la coriomeningitis linfocítica
Imagen: “Negative stain electron micrograph of an arenavirus from a mouse that tested positive for LCM” por CDC. Licencia: Dominio PúblicoArenavirus: provocan infecciones crónicas en roedores (ratón doméstico, Mus musculus)
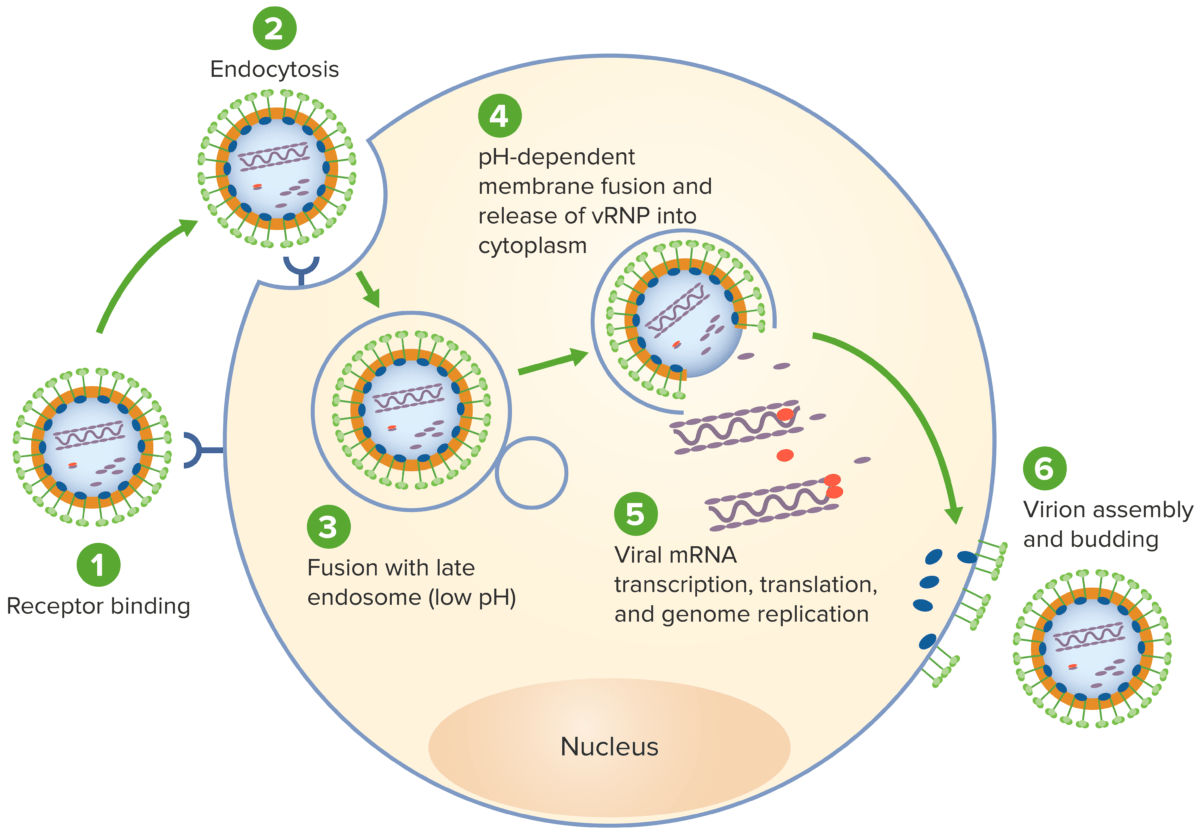
El ciclo vital del virus de la coriomeningitis linfocítica:
1. El virus se une a los receptores del huésped a través de las glicoproteínas de la envoltura.
2. El virus es posteriormente endocitado, consiguiendo así la entrada en la célula.
3. A continuación se produce la fusión del virus con un endosoma.
4. El virus se fusiona con la membrana del endosoma, lo que permite la liberación de la ribonucleocápside viral en el citoplasma.
5. La ARN polimerasa dependiente de ARN (RdRP) media la replicación y transcripción del gen viral en el citoplasma del huésped.
6. Se ensamblan nuevos viriones y se produce la gemación, liberando el virión para infectar otras células.
vRNP: ribonucleoproteína viral
LCMV no es citotóxico, si bien la respuesta inmune del huésped intenta eliminar el virus, esto puede desencadenar una enfermedad inmunomediada. La respuesta inmune produce las diferentes manifestaciones de la enfermedad.
La infección por el virus de la coriomeningitis linfocítica da como resultado una enfermedad bifásica.
Inicio de los síntomas:
Síntomas de la 1ra fase:
Síntomas de la 2da fase:
Después de unos días de recuperación, pueden comenzar los síntomas de la segunda fase, que incluyen síntomas neurológicos (típicos de meningitis y/o encefalitis).
Otros hallazgos menos frecuentes:
Las mujeres que se infectan con virus de la coriomeningitis linfocítica durante el embarazo pueden transmitir la infección al feto.
La inmunosupresión significativa en los receptores de trasplantes juega un papel en el desarrollo de la enfermedad:
Durante la primera fase de la enfermedad, las anomalías de laboratorio más comunes son
Los arenavirus pueden causar enfermedades neurológicas y/o fiebres hemorrágicas, para lo que una de las principales etiologías es el virus de Lassa.
| Organismo | Virus de la coriomeningitis linfocítica | Virus de Lassa |
|---|---|---|
| Familia | Arenaviridae | |
| Género | Mammarenavirus | |
| Características |
|
|
| Reservorio | Roedores | |
| Transmisión |
|
|
| Curso clínico | Bifásico:
|
|
| Diagnóstico |
|
|
| Tratamiento | De soporte |
|
| Prevención | Evite el contacto con roedores y sus fluidos corporales. |
|
Los siguientes virus de ARN seleccionados también pueden provocar una infección del SNC.