La trombocitopenia se presenta cuando el recuento de plaquetas es < 150 000 por microlitro. El rango normal de las plaquetas suele ser entre 150 000–450 000/µl de sangre total. La trombocitopenia puede ser el resultado de una disminución de la producción, un aumento de la destrucción o un secuestro esplénico de las plaquetas. Los pacientes suelen ser asintomáticos hasta que el recuento de plaquetas es < 50 000/µL. Las manifestaciones clínicas de la trombocitopenia incluyen la facilidad de aparición de hematomas o hemorragias, petequias, púrpura y, cuando son graves, hemorragias espontáneas de las mucosas y/o internas. El diagnóstico se realiza con un hemograma y un frotis de sangre; pueden ser necesarias pruebas adicionales para determinar la etiología subyacente si no es evidente en el escenario clínico. El tratamiento implica tratar la etiología subyacente y las transfusiones de plaquetas.
Última actualización: Ene 15, 2024
La trombocitopenia es una deficiencia de plaquetas, típicamente definida como < 150 000 plaquetas por microlitro de sangre total.
La trombocitopenia puede clasificarse como leve, moderada o grave en función del recuento de plaquetas:
La trombocitopenia puede estar causada por la disminución de la producción, el aumento de la destrucción o el secuestro de las plaquetas.
| Mecanismo | Ejemplos |
|---|---|
| Disminución de la producción | Fallo de la médula ósea:
|
Disminución de la trombopoyetina:
|
|
Nutricional:
|
|
Congénito:
|
|
| Aumento de la destrucción | Inmuno-mediado:
|
| Consumo en trombos |
|
| Secuestro en bazo |
|
| Mecanismos mixtos o poco claros | Trombocitopenia inducida por infección:
|
| Dilución |
|
| Pseudotrombocitopenia (un recuento de plaquetas falsamente bajo debido a la aglutinación) |
|
En condiciones fisiológicas normales, las plaquetas se producen a partir de la fragmentación de los megacariocitos en la médula ósea.
Las plaquetas son las principales células implicadas en la formación del tapón plaquetario inicial (i.e., la hemostasia primaria).
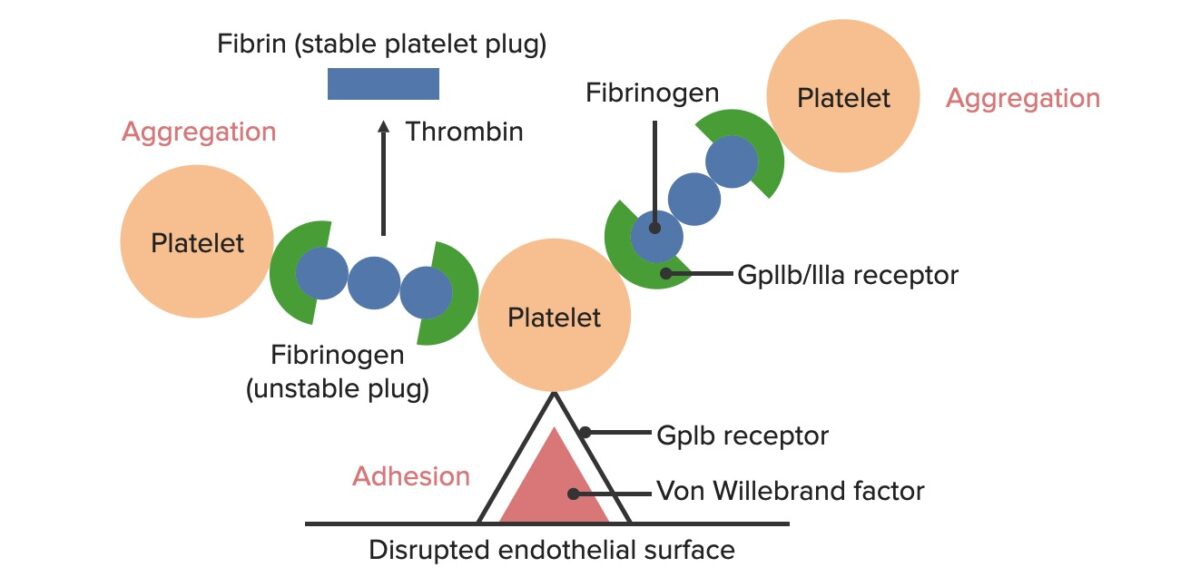
Formación del tapón hemostático temporal:
La superficie endotelial alterada expone el FVW al paso de la sangre. Las plaquetas se unen al FVW a través de sus receptores GpIb y se activan. La activación de las plaquetas las lleva a secretar ADP, que estimula la expresión de los receptores GpIIb/IIIa en las plaquetas. Los receptores GpIIb/IIIa se unen al fibrinógeno, que es capaz de unir una plaqueta en cada extremo, provocando la agregación de las plaquetas. A medida que se unen más plaquetas entre sí, se genera el tapón plaquetario. Al activarse la cascada de la coagulación, la trombina convierte el fibrinógeno más débil en fibrina más fuerte, creando un coágulo mucho más estable.
En la trombocitopenia, la deficiencia de plaquetas resulta en:
La trombocitopenia inducida por medicamentos puede deberse a efectos tóxicos directos sobre la médula ósea (e.g., la quimioterapia) o a anticuerpos dependientes del medicamento. Anticuerpos medicamento-dependientes:
A diferencia de la mayoría de las trombocitopenias inducidas por medicamentos, la TIH se asocia a un riesgo notablemente mayor de trombosis que de hemorragia.
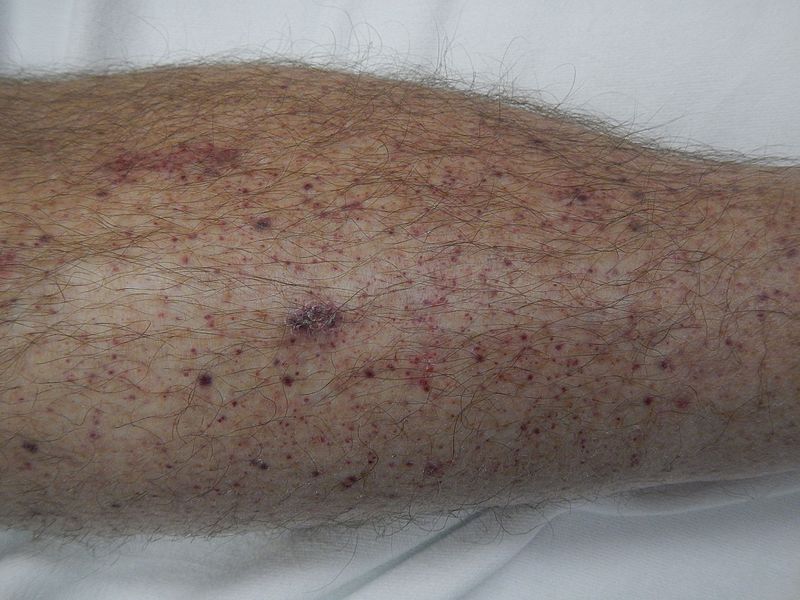
Petequias en la parte inferior de la pierna de un paciente con púrpura trombocitopénica inmune
Imagen: “Petechiae on lower leg” por James Heilman, MD.es Licencia: CC BY-SA 4.0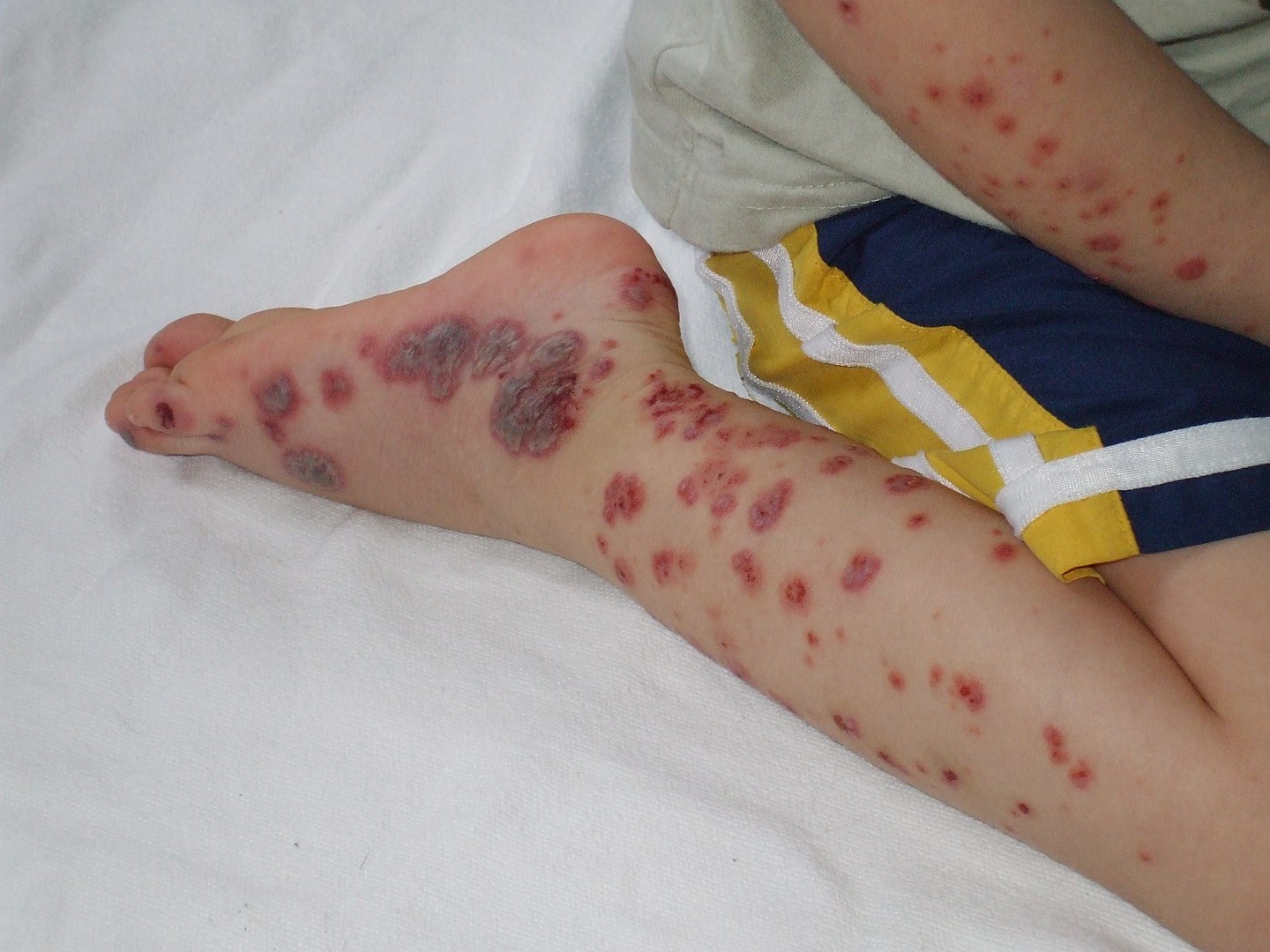
Púrpura evidente en las extremidades distales de un paciente pediátrico
Imagen: «Purpura2» por Okwikikim. Licencia: Dominio PúblicoEl diagnóstico de la trombocitopenia en sí se realiza con evaluaciones de laboratorio. A partir de los antecedentes y el examen se pueden obtener pistas sobre la etiología subyacente, y las pruebas de laboratorio adicionales pueden ayudar al diagnóstico.
Las siguientes pruebas deben solicitarse para todos los pacientes con trombocitopenia:
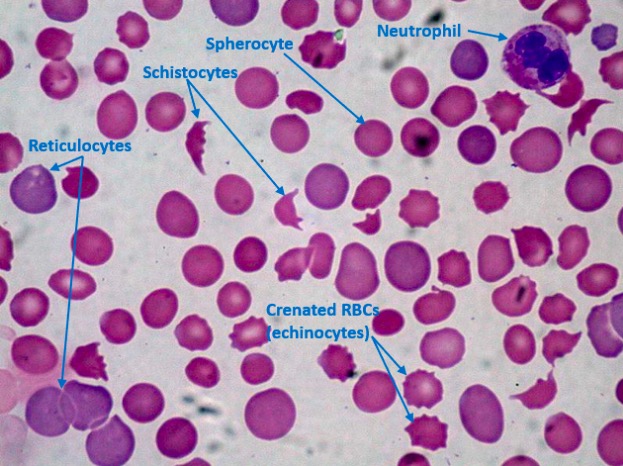
Lámina de sangre periférica de un paciente con CID que muestra trombocitopenia, esquistocitos y esferocitos:
Hay muchos reticulocitos (eritrocitos inmaduros), lo que indica una respuesta hematopoyética rápida de la médula ósea. Los recuentos de plaquetas se reducen (no se ve ninguna aquí) por el consumo debido a la CID. Normalmente, debe haber al menos 8 plaquetas en un solo campo de inmersión en aceite de 1 000×; 1 plaqueta indica aproximadamente 20 000 plaquetas/µL en la sangre periférica.
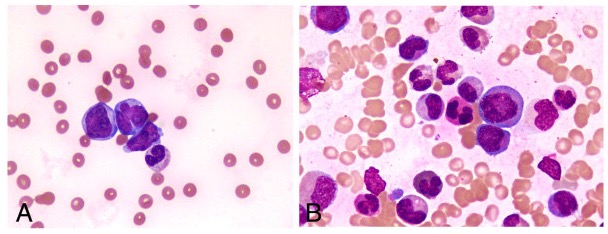
Los frotis periféricos muestran escasez de plaquetas
Imagen: “Peripheral blood smear and bone marrow aspirate” por Shabneez Hussain. Licencia: CC BY 2.0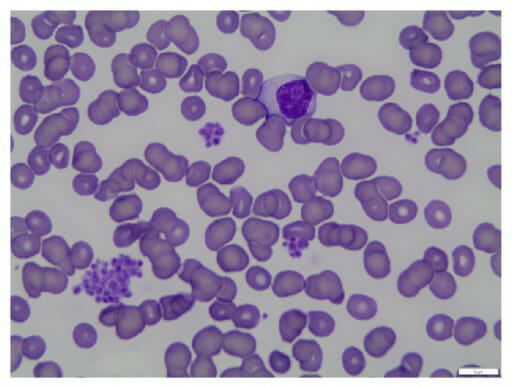
Frotis de sangre de pseudotrombocitopenia: La seudotrombocitopenia se debe a la aglutinación de las plaquetas in vitro debido a la aglutinación.
Imagen: “fig1: Peripheral blood smear (100x oil)” por Geok Chin Tan. Licencia: CC BY 4.0Las siguientes pruebas deben solicitarse solo cuando estén clínicamente indicadas para ayudar a identificar la etiología subyacente.
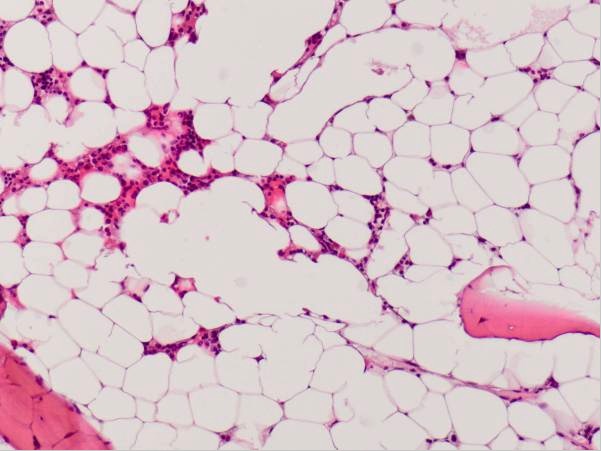
Médula ósea hipocelular en un paciente con anemia aplásica
Imagen: “Hypocellular bone marrow showing only little hematopoiesis” por Department of Obstetrics of Gynaecology, Erasmus University Medical Center, PO Box 2040, 3000 CA Rotterdam, The Netherlands. Licencia: CC BY 2.0El tratamiento de la trombocitopenia depende principalmente del manejo de la causa subyacente, del control del recuento de plaquetas y de la prevención/control de cualquier complicación hemorrágica.