El cáncer cervicouterino es el 3er cáncer ginecológico más común. Más del 90% de los LOS Neisseria casos de cáncer cervicouterino están asociados con los LOS Neisseria virus Virus Viruses are infectious, obligate intracellular parasites composed of a nucleic acid core surrounded by a protein capsid. Viruses can be either naked (non-enveloped) or enveloped. The classification of viruses is complex and based on many factors, including type and structure of the nucleoid and capsid, the presence of an envelope, the replication cycle, and the host range. Virology del papiloma humano (VPH) de alto riesgo, que se transmiten por contacto sexual. El cáncer cervicouterino se puede prevenir mediante la detección temprana y el tratamiento de las lesiones precancerosas causadas por el VPH de alto riesgo. Los LOS Neisseria métodos de detección son la citología cervical y la tipificación de VPH. Las guías varían en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum cuanto al AL Amyloidosis momento de iniciar el tamizaje; varias sociedades estadounidenses recomiendan que el tamizaje comience entre los LOS Neisseria 21 y los LOS Neisseria 25 años de edad, mientras que la Organización Mundial de la Salud (OMS) sugiere esperar hasta los LOS Neisseria 30 años, especialmente en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum entornos con recursos limitados. Las guías también varían en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum cuanto al AL Amyloidosis método preferido para realizar las pruebas, aunque universalmente se prefiere la prueba del VPH (con o sin citología) a partir de los LOS Neisseria 30 años. Desde que se inició el programa de tamizaje, la incidencia y la mortalidad por cáncer cervicouterino han disminuido en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum un 75%.
Last updated: Feb 13, 2023
Contents
Las estrategias de tamizaje se pueden realizar de forma independiente o simultánea (prueba conjunta).
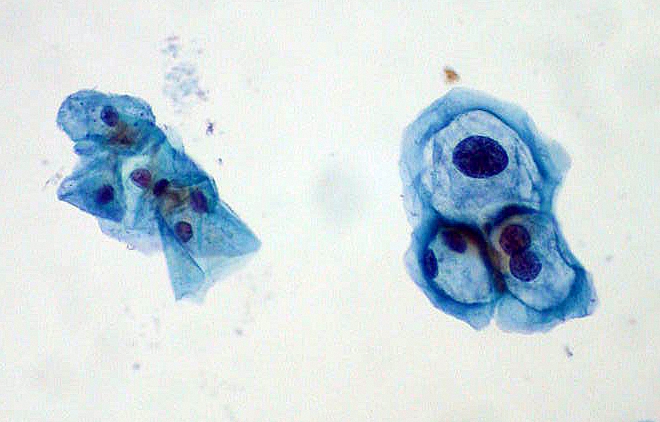
Imagen de un frotis de Papanicolaou para el tamziaje de cáncer cervicouterino: las células escamosas normales están a la izquierda; las células infectadas por VPH con displasia leve se encuentran a la derecha.
Imagen: “ThinPrep Pap frotis HPV” por Ed Uthman. Licencia: Dominio Público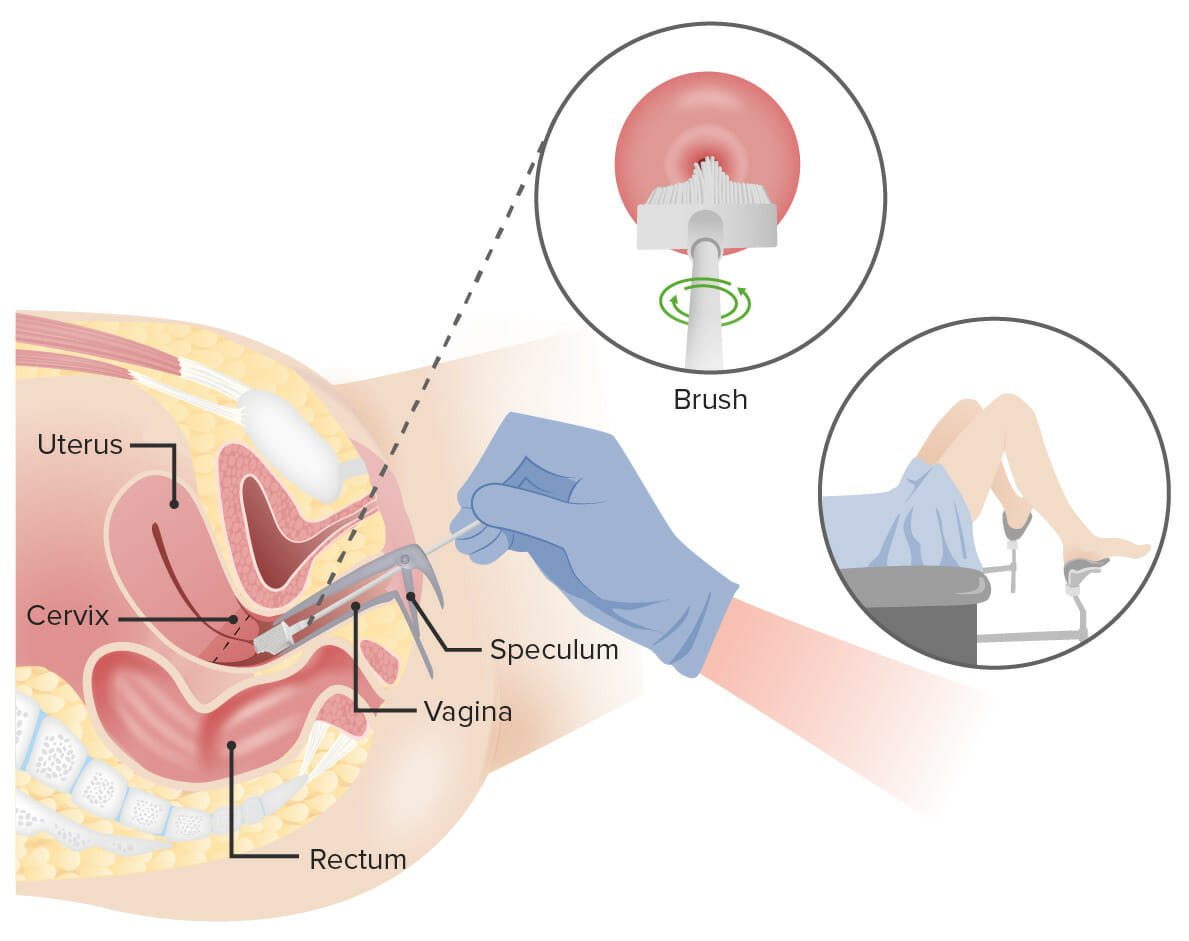
Prueba de Papanicolaou:
Se introduce un espéculo en la vagina para ensancharla. A continuación, se introduce una escoba (mostrada aquí) o un cepillo endocervical y una espátula en la vagina para recoger células del cuello uterino. Las células se examinan al microscopio para detectar signos de enfermedad. Imagen por Lecturio.
Las siguientes recomendaciones son para individuos de riesgo promedio. Este grupo incluye personas que completaron su esquema de vacunación contra el VPH.
Ciertas condiciones tienen un alto riesgo de cáncer cervicouterino, por lo que las pruebas de tamizaje deben ser individualizadas y más frecuentes:
El sistema Bethesda es un informe estandarizado de resultados, que incluye una muestra adecuada, la categorización general de los LOS Neisseria hallazgos y los LOS Neisseria resultados:
Tipos de anormalides de células epiteliales escamosas:
Anomalías de las células glandulares (clasificadas como endocervicales, endometriales o no especificadas):
Otros posibles hallazgos reportados en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum la citología cervical:
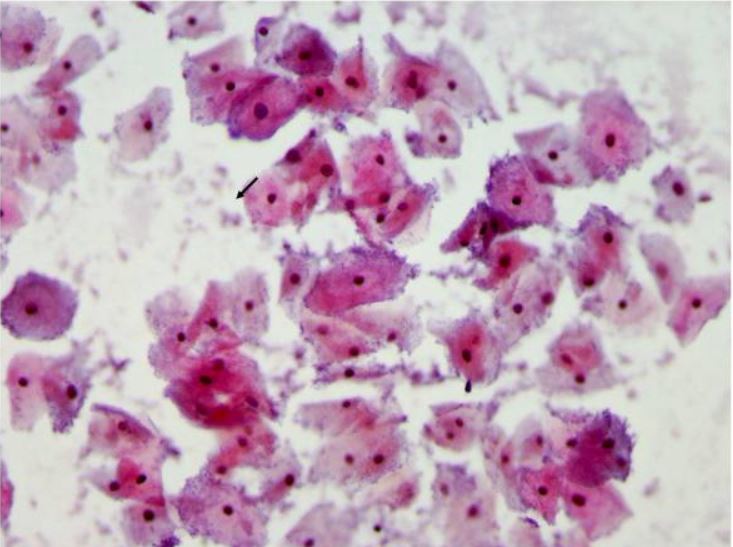
Frotis de Papanicolaou que muestra vaginosis bacteriana con muchas células guía
Las células guía son células epiteliales vaginales salpicadas de cocobacilos adherentes que se aprecian mejor en el borde de las células. Las bacterias se tiñen de azul- violeta con la tinción de Papanicolaou (flechas).
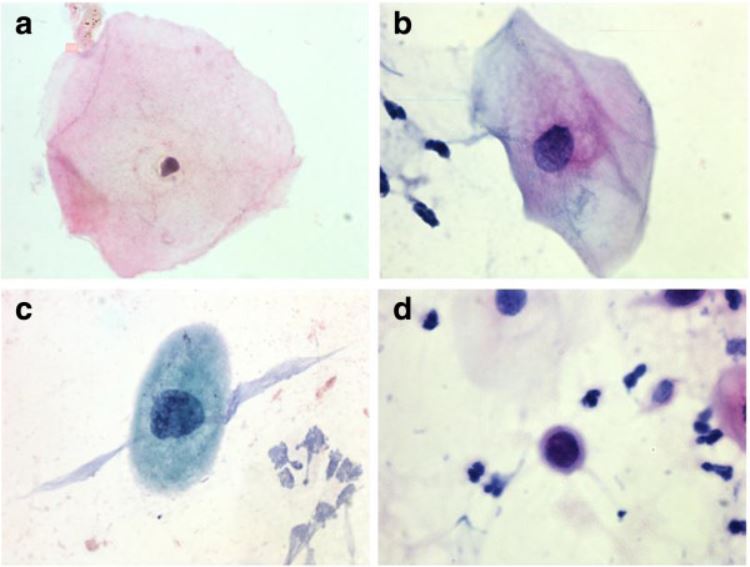
Ejemplos de hallazgos de células escamosas durante la detección del cáncer cervicouterino:
a. Célula normal
b. Células escamosas atípicas de significado incierto
c. Lesión intraepitelial escamosa de bajo grado
d. Lesión intraepitelial escamosa de alto grado
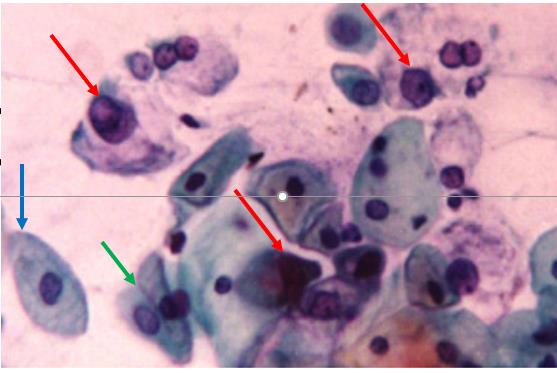
AGCUS favoreciendo un proceso neoplásico, tinción de Papanicolaou
Citología cervical que muestra células glandulares atípicas (flechas rojas), favoreciendo un proceso neoplásico. La flecha azul apunta a una célula epitelial escamosa benigna y la flecha verde apunta a 2 células endocervicales benignas.
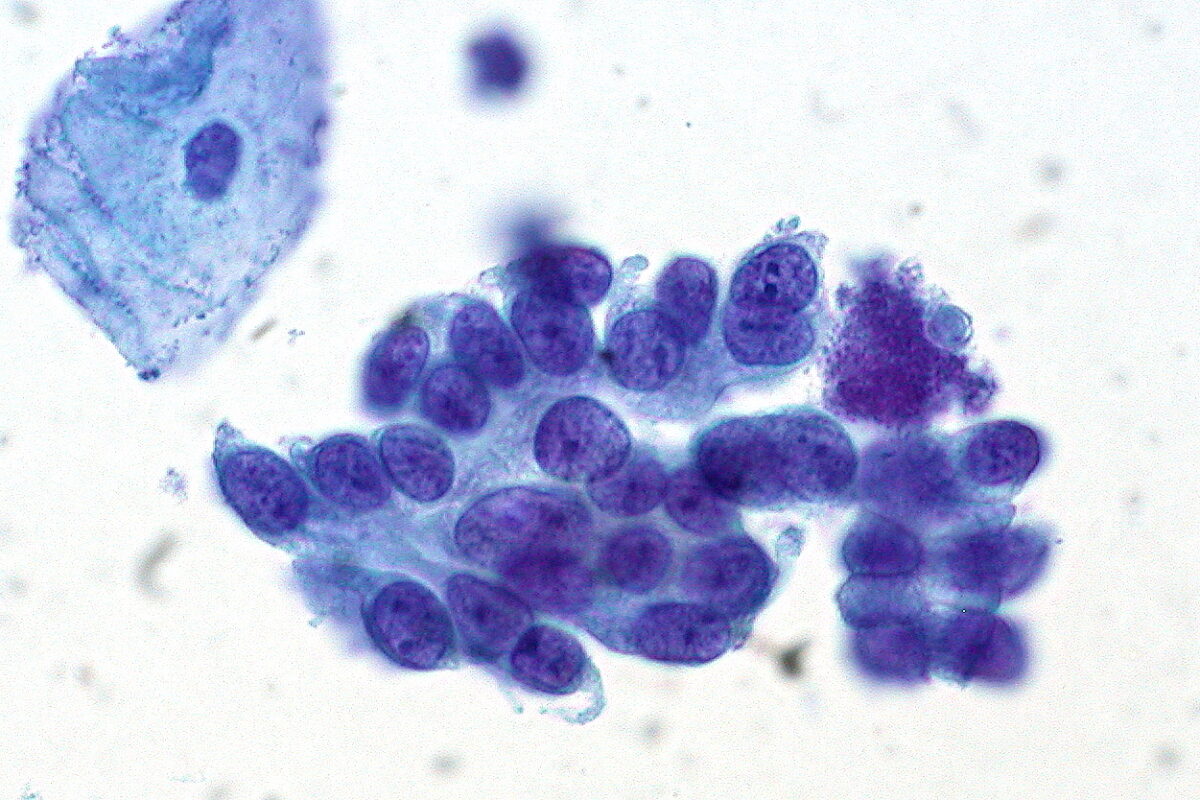
Citología cervical que muestra adenocarcinoma in situ del cuello uterino: observe la célula epitelial escamosa benigna en la parte superior izquierda.
Imagen: “Adenocarcinoma in Situ of the Cervix” por Ed Uthman. Licencia: CC BY 2.0El tratamiento de los LOS Neisseria resultados anormales del tamizaje se basa en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum el riesgo de la paciente de CIN CIN An increased tendency to acquire chromosome aberrations when various processes involved in chromosome replication, repair, or segregation are dysfunctional. Colorectal Cancer 3+ (expresado en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum porcentaje), tanto ahora como dentro de 5 años.in
| Riesgo | Tratamiento de preferencia |
|---|---|
| Riesgo de CIN CIN An increased tendency to acquire chromosome aberrations when various processes involved in chromosome replication, repair, or segregation are dysfunctional. Colorectal Cancer 3+ en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum los LOS Neisseria próximos 5 años (umbrales de actuación clínica) | |
| < 0.15 % | Retorno al AL Amyloidosis tamizaje de rutina a intervalos de 5 años. |
| 0.15 % a < 0.55 % | Reptir prueba (pruebas primarias de VPH, pruebas conjuntas) en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 3 años. |
| 0.55 % a < 4 % | Repetir prueba en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 1 año. |
| Riesgo inmediato de CIN CIN An increased tendency to acquire chromosome aberrations when various processes involved in chromosome replication, repair, or segregation are dysfunctional. Colorectal Cancer 3+ (umbral de intervención clínica) | |
| 4 % a < 25 % | Se recomienda colposcopia |
| 25 % a < 60 % | Tratamiento expedito o colposcopia es aceptable (para pacientes no embarazadas ≥ 25 años de edad). |
| ≥ 60 % | Tratamiento expedito de preferencia (para pacientes no embarazadas ≥ 25 años de edad) |
| Antecedentes | Resultado actual de VPH | Resultado actual de citología | Riesgo inmediato de CIN CIN An increased tendency to acquire chromosome aberrations when various processes involved in chromosome replication, repair, or segregation are dysfunctional. Colorectal Cancer 3+(%) | Riesgo a 5 años de CIN CIN An increased tendency to acquire chromosome aberrations when various processes involved in chromosome replication, repair, or segregation are dysfunctional. Colorectal Cancer 3+(%) | Tratamiento recomendado |
|---|---|---|---|---|---|
| Desconocido | VPH-negativo | NILM | 0.00 | 0.12 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 5 años |
| ASC-US | 0.04 | 0.40 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 3 años | ||
| LSIL | 1.1 | 2.0 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 1 año | ||
| ASC-H | 3.4 | 3.8 | Colposcopía | ||
| HSIL+ | 25 | 27 | Colposcopia o tratamiento expedito | ||
| VPH-positivo | NILM | 2.1 | 4.8 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 1 año | |
| ASC-US | 4.4 | 7.3 | Colposcopía | ||
| LSIL | 4.3 | 6.9 | Colposcopia | ||
| ASC-H | 26 | 33 | Colposcopia o tratamiento expedito | ||
| HSIL+ | 49 | 53 | Colposcopia o tratamiento expedito | ||
| VPH-negativo | VPH-negativo | NILM | 0.00 | 0.09 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 5 años |
| ASC-US | 0.01 | 0.36 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 3 años | ||
| LSIL | 0.44 | 0.79 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 1 año | ||
| ASC-H | 2.8 | 3.3 | Colposcopia | ||
| HSIL+ | 14 | 14 | Colposcopia | ||
| VPH-positivo | NILM | 0.74 | 2.3 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 1 año | |
| ASC-US | 2.0 | 3.8 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 1 año | ||
| LSIL | 2.1 | 3.8 | Seguimiento en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum 1 año | ||
| ASC-H | 14 | 18 | Colposcopia | ||
| HSIL+ | 32 | 34 | Colposcopia o tratamiento expedito |