Los inhibidores de los microtúbulos y las topoisomerasas se dirigen a estructuras y procesos celulares para inhibir la proliferación de células cancerosas. Los inhibidores de los microtúbulos actúan sobre el citoesqueleto, mientras que los inhibidores de la topoisomerasa actúan sobre una enzima que es importante en la replicación y transcripción del ADN. El sistema de microtúbulos, junto con los microfilamentos y los filamentos intermedios, forman el citoesqueleto celular. Estos componentes son esenciales para la división celular, el movimiento y la señalización. Los taxanos y los alcaloides de la vinca interfieren con la función de los microtúbulos y, por lo tanto, inhiben la mitosis. La topoisomerasa ayuda a la replicación del ADN mediante la creación de rupturas de cadena doble y simple para liberar el ADN superenrollado. La inhibición de la enzima provoca la terminación de la replicación del ADN y el daño del ADN. Existen múltiples medicamentos quimioterapéuticos en cada clase que comúnmente producen mielosupresión como efecto secundario.
Última actualización: Abr 13, 2025
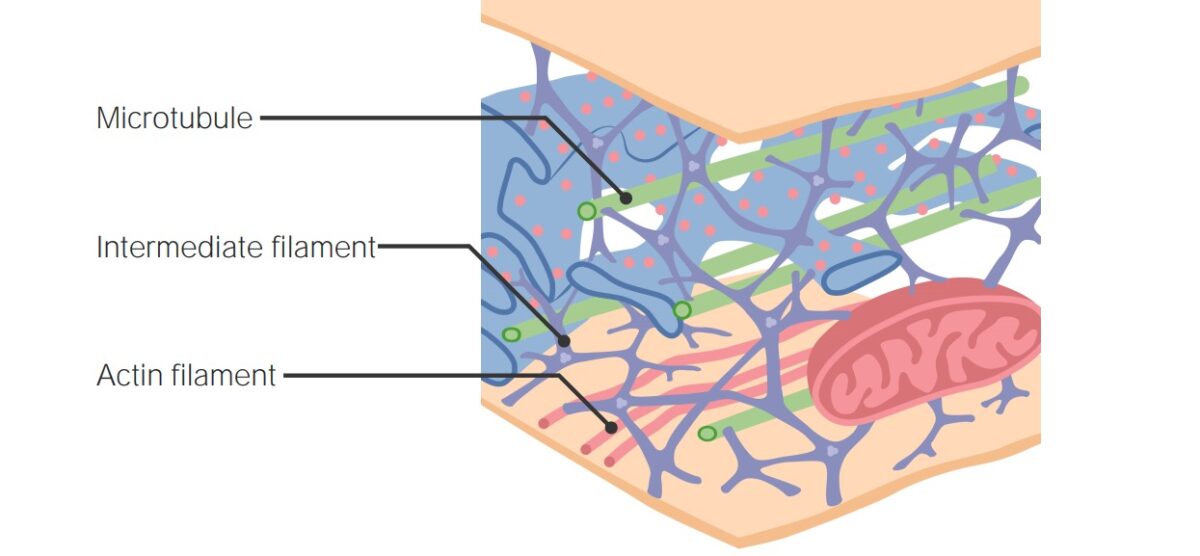
Filamentos del citoesqueleto
Imagen por Lecturio.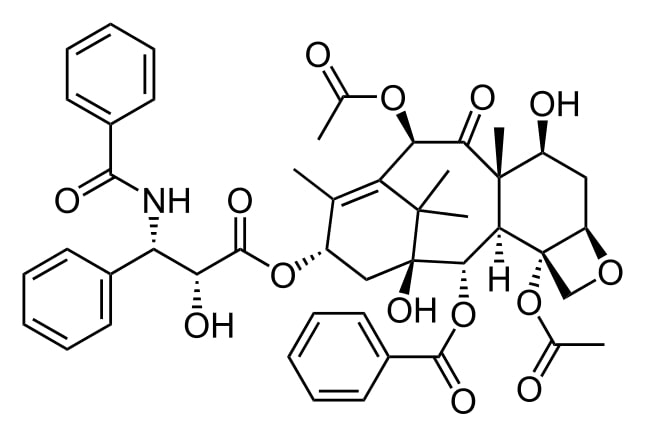
Estructura del paclitaxel
Imagen: “Taxol” por Calvero. Licencia: Dominio Público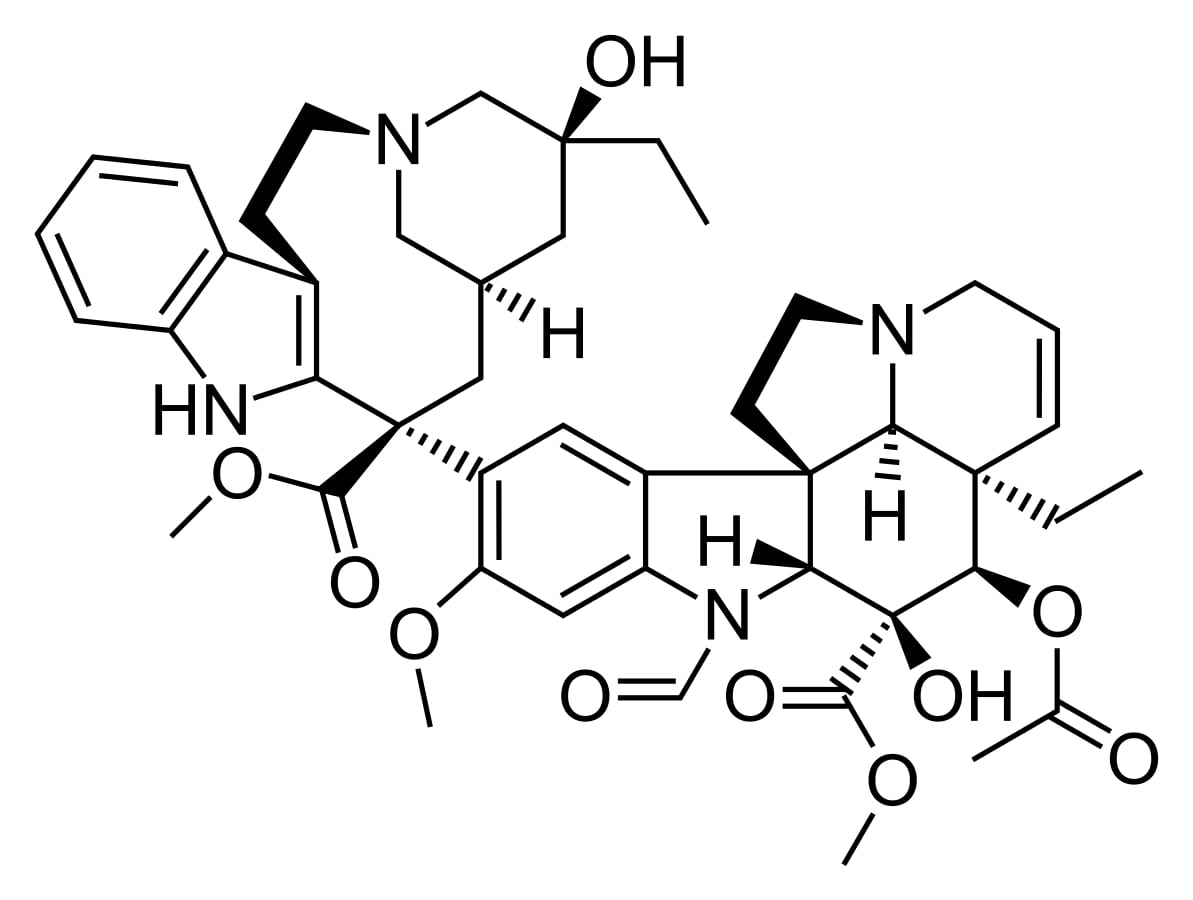
Estructura de la vincristina
Imagen: “Vincristine” por Fvasconcellos. Licencia: Dominio Público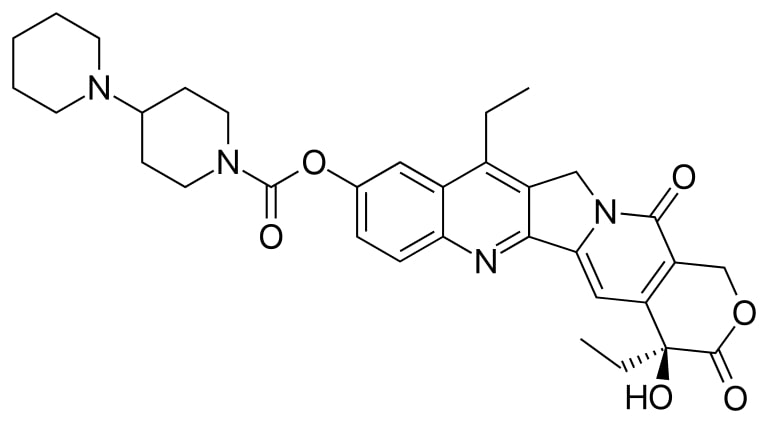
Estructura del irinotecán
Imagen: “Irinotecan” por Fvasconcellos. Licencia: Dominio Público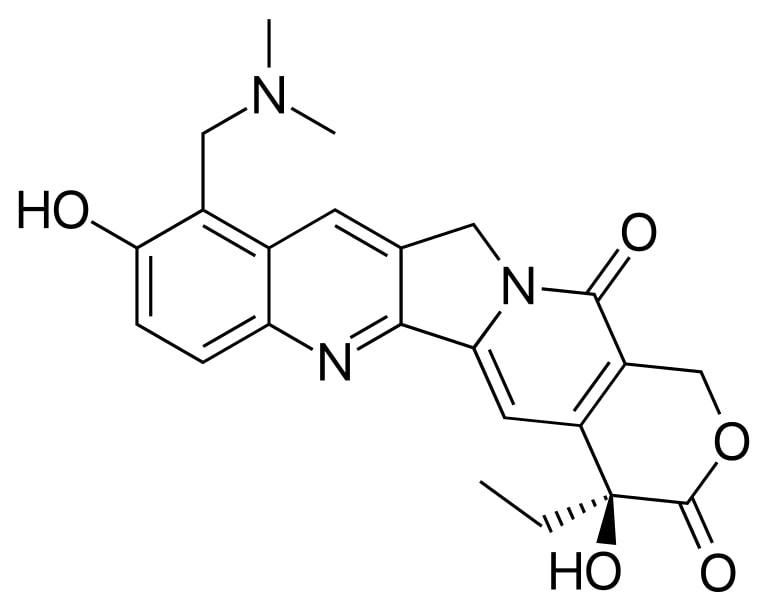
Estructura del topotecán
Imagen: “Topotecan” por Fvasconcellos. Licencia: Dominio Público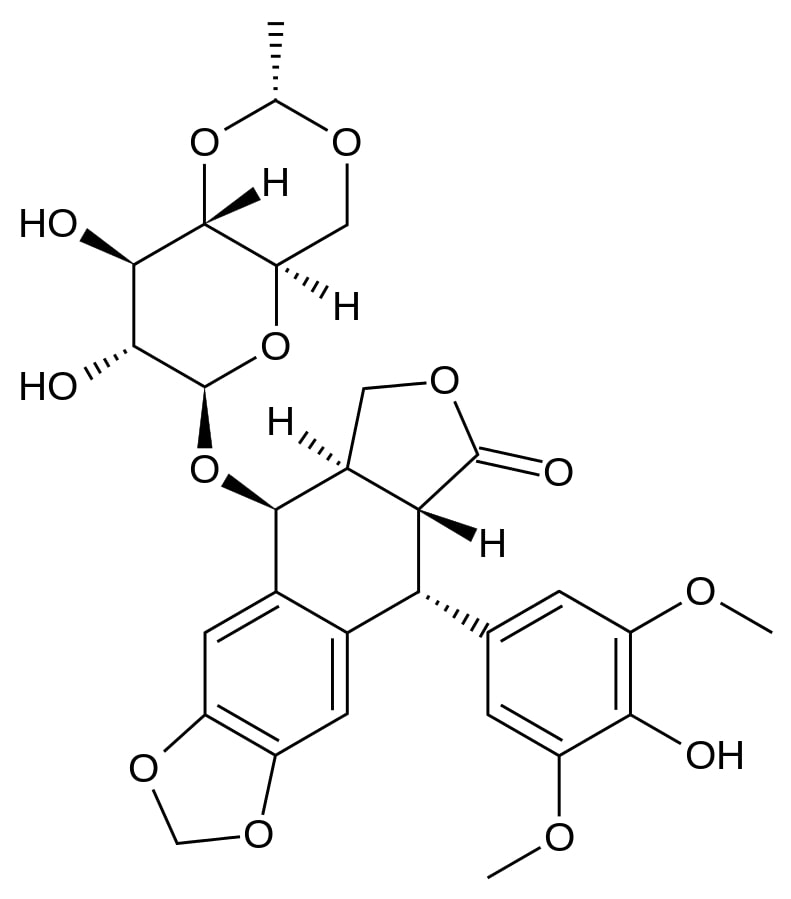
Estructura del etopósido
Imagen: “Etoposide” por Fvasconcellos. Licencia: Dominio Público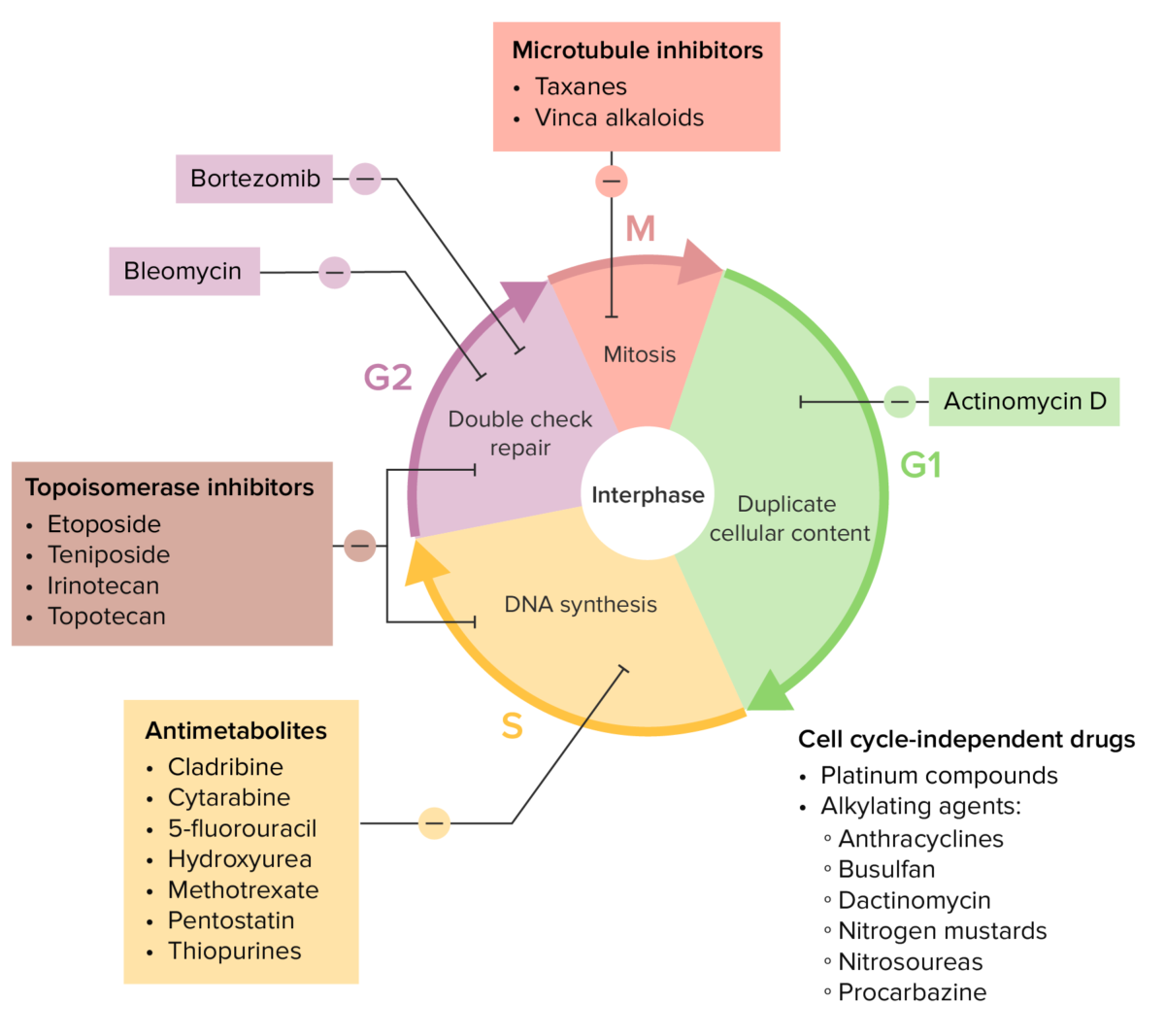
Diversos medicamentos de quimioterapia y sus efectos sobre el ciclo celular
Imagen por Lecturio.| Clase del medicamento | Mecanismo |
|---|---|
Antibióticos antitumorales:
|
Se intercalan entre bases, lo que provoca el bloqueo de la síntesis de ADN o ARN y la prevención de la replicación del ADN |
| Antraciclinas |
|
| Agentes alquilantes |
|
| Clase del medicamento | Fase del ciclo celular afectada | Mecanismo de acción |
|---|---|---|
| Antifolatos | Detención del ciclo celular en la fase S | Inhiben:
|
| Bleomicina | Detiene del ciclo celular en la fase G2 | Se une al ADN, lo que lleva a roturas de las cadenas simples y dobles |
| Fluoropirimidinas | Detienen el ciclo celular en la fase S | Inhiben la timidilato sintasa |
| Análogos de la desoxicitidina | Detienen el ciclo celular en la fase S | Inhiben:
|
| Análogos de la purina | Detienen del ciclo celular en la fase S | Inhiben la síntesis de purinas de novo |
| Inhibidores de la topoisomerasa II | Detienen el ciclo celular en las fases S y G2 | Inhiben la topoisomerasa II |
| Taxanos | Detienen el ciclo celular en la metafase de la fase M | Hiperestabilizan los microtúbulos |
| Alcaloides de la vinca | Detienen el ciclo celular durante la metafase de la fase M | Se unen a la beta-tubulina y previenen la polimerización de los microtúbulos |