La amebiasis o disentería amebiana, es una infección causada por el parásito Entamoeba histolytica. La transmisión se produce por la vía fecal-oral o por el consumo de agua y alimentos contaminados. La mayoría de los pacientes infectados por E. histolytica son asintomáticos, pero alrededor del 10% pueden desarrollar disentería. Las infecciones invasivas se caracterizan por dolor abdominal, fiebre y diarrea sanguinolenta, las cuales pueden provocar complicaciones graves, como abscesos hepáticos, fístulas intestinales o colitis fulminante. El diagnóstico suele realizarse mediante el estudio de las heces o por la detección de marcadores inmunológicos. El tratamiento consiste en administrar un agente amebicida absorbible como el metronidazol y un agente amebicida intraluminal como la paromomicina.
Última actualización: Sep 1, 2022
Agente causal: parásitos protozoarios anaerobios del género Entamoeba
La transmisión se produce mediante la ingestión de quistes:
Factores de riesgo y poblaciones de alto riesgo:
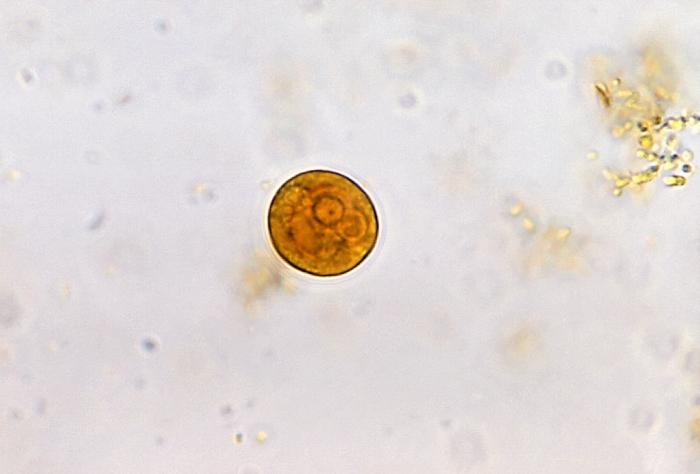
Microfotografía de Entamoeba histolytica, en la fase de quiste
Imagen: “Entamoeba histolytica cyst” por Yasser. Licencia: CC BY 2.0
Trofozoítos de Entamoeba histolytica con eritrocitos ingeridos teñidos con tricrómico:
Los eritrocitos ingeridos aparecen como inclusiones oscuras. Los parásitos contienen núcleos que tienen el típico cariosoma pequeño, situado en el centro, con una cromatina periférica fina y uniforme. La eritrofagocitosis o la ingestión de eritrocitos, es la característica que distingue a E. histolytica de E. dispar.
El ciclo de vida de la Entamoeba spp. depende de la infección de un huésped, porque la transición a través de las distintas etapas de vida se producen dentro del tracto intestinal del huésped.
Fase de quiste:
Fase de trofozoíto:
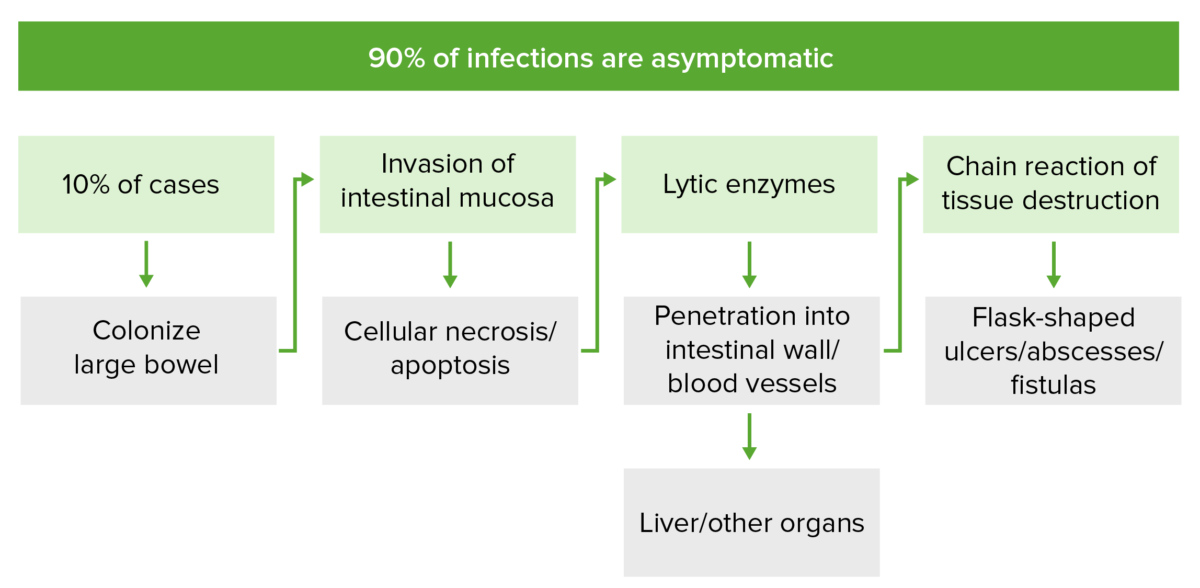
Patogénesis de la infección invasiva por Entamoeba histolytica:
En el 10% de los casos, E. histolytica coloniza la mucosa del intestino grueso e invade mediante la secreción de proteinasas y enzimas líticas. Esto provoca la necrosis celular y la lisis de las membranas, respectivamente. Esta cadena de acontecimientos inducen la apoptosis de las células de la mucosa y alteran las estrechas uniones entre las células, lo que permiten la formación de úlceras en forma de botella, abscesos y fístulas. La invasión puede alcanzar el sistema venoso portal, a través del cual E. histolytica puede extenderse a otros órganos.
El periodo de incubación suele ser de 2–4 semanas una vez ingerido, pero los síntomas pueden desarrollarse hasta 1 año después de la infección.
El 90% de las infecciones por Entamoeba son asintomáticas:
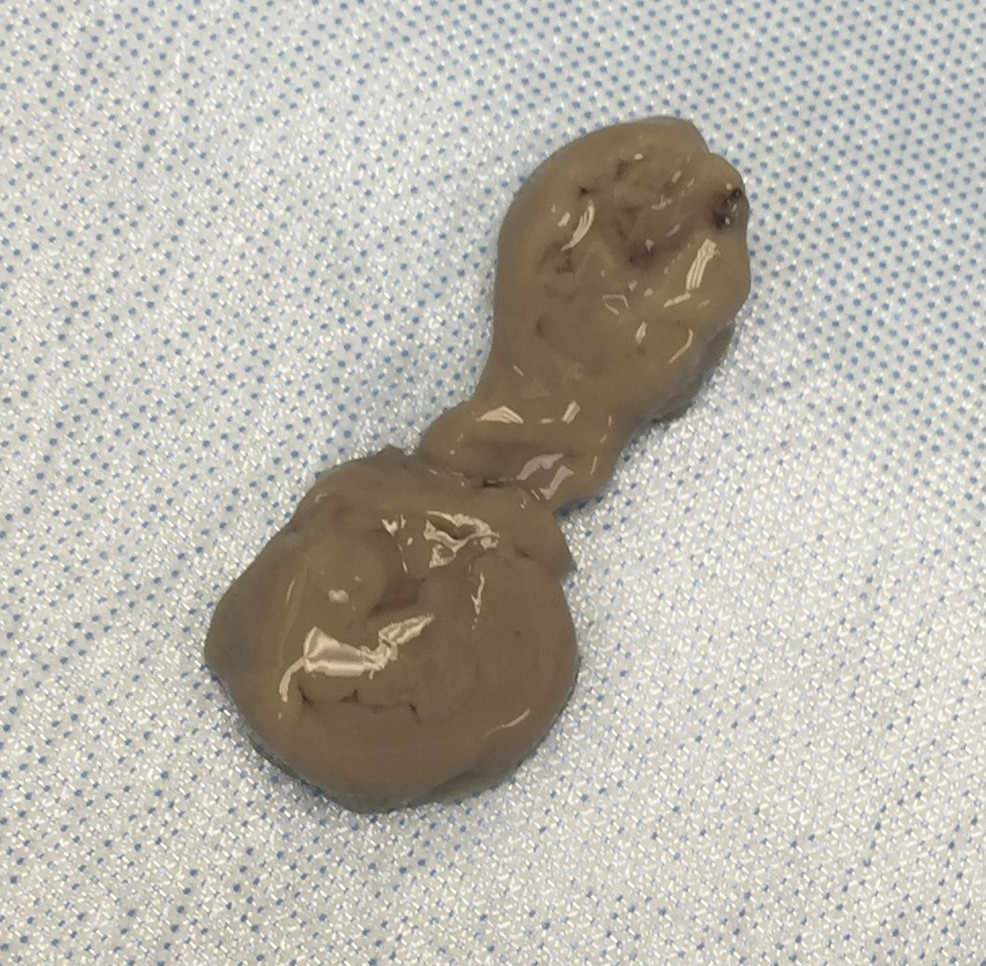
Aspirado de “pasta de anchoas” del absceso hepático de un paciente con una infección invasiva por E. histolytica
Imagen: “Aspirate of “anchovy paste” por Palak Patel et al. Licencia: CC BY 4.0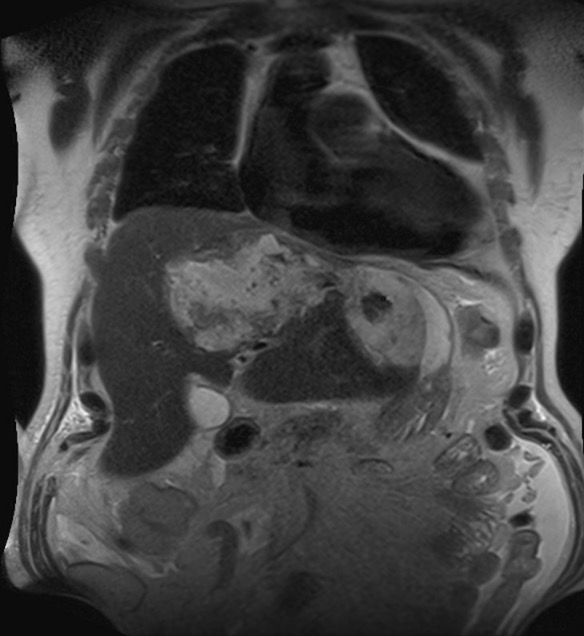
Absceso amebiano en el lóbulo izquierdo del hígado:
Colangiopancreatografía por resonancia magnética coronal ponderada en T2 que muestra una colección de material heterogéneo en el lóbulo izquierdo del hígado
El diagnóstico de la amebiasis se basa en la sospecha clínica y en las pruebas confirmatorias. Se pueden utilizar distintas modalidades de pruebas.
Todas las infecciones por E. histolytica deben ser tratadas independientemente de la ausencia o gravedad de los síntomas; sin embargo, las infecciones por E. dispar no necesitan ser tratadas.
Todas las acciones que causan diarrea inespecífica o sanguinolenta son diagnósticos diferenciales para la amebiasis.