La talasemia es una causa hereditaria de anemia microcítica hipocrómica y es el resultado de una deficiencia en las cadenas de globina α o β, lo que provoca una hemoglobinopatía. La presentación de la talasemia depende del número de cadenas defectuosas presentes y puede variar desde ser asintomática hasta provocar que los pacientes más gravemente afectados sean dependientes de transfusiones. El diagnóstico puede confirmarse mediante una electroforesis de hemoglobina, que revelará la presencia de cadenas de α o β-globina anormales.
Última actualización: Abr 13, 2022
| Número de genes eliminados/genotipo | Enfermedad | Resultado |
|---|---|---|
| 1 (αα/α-) |
α-Talasemia mínima | Portador silencioso |
| 2 (α-/α-; trans) (αα/–; cis) |
α-Talasemia menor |
|
| 3 (α-/–) |
Hemoglobina H (4 cadenas β) | Anemia moderada a severa |
| 4 (–/–) |
Hemoglobina Barts (4 cadenas γ) | Hidropesía fetal (incompatible con la vida) |
| Número de genes eliminados/genotipo | Enfermedad | Resultado |
|---|---|---|
| β0/β o β+/β | Talasemia menor | Asintomático (leve) |
| β0/β0 o β+/β+ | Talasemia mayor (anemia de Cooley) | Dependiente de transfusiones |
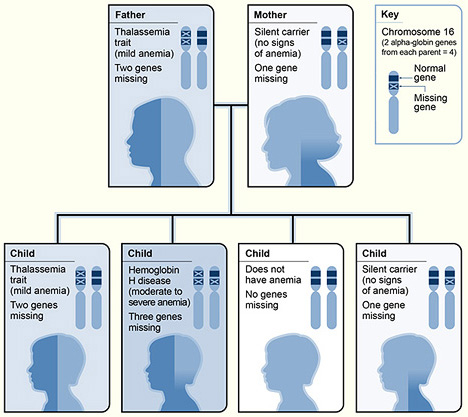
Un ejemplo de herencia de la α-talasemia
Imagen: “The picture shows one example of how alpha thalassemia is inherited” por National Heart Lung and Blood Institute (NIH). Licencia: Dominio Público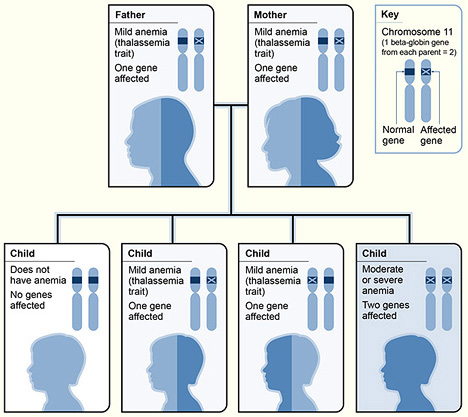
Un ejemplo de herencia de la β-talasemia
Imagen: “The picture shows one example of how beta thalassemia is inherited” por National Heart Lung and Blood Institute (NIH). Licencia: Dominio Público| Enfermedad | Presentación |
|---|---|
| α-Talasemia mínima | Asintomática |
| α-Talasemia menor |
|
| Enfermedad hemoglobina H |
|
| Hemoglobina Barts |
|
| β-Talasemia menor |
|
| β-Talasemia mayor (anemia de Cooley) |
|
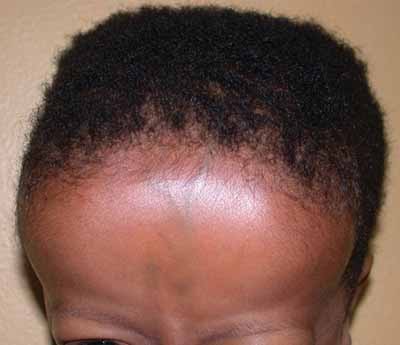
La prominencia frontal se debe a una necesidad excesiva de hematopoyesis
Imagen: “Frontal bossing (abnormally enlarged forehead) in a child” por National Human Genome Research Institute (NIH). Licencia: Dominio Público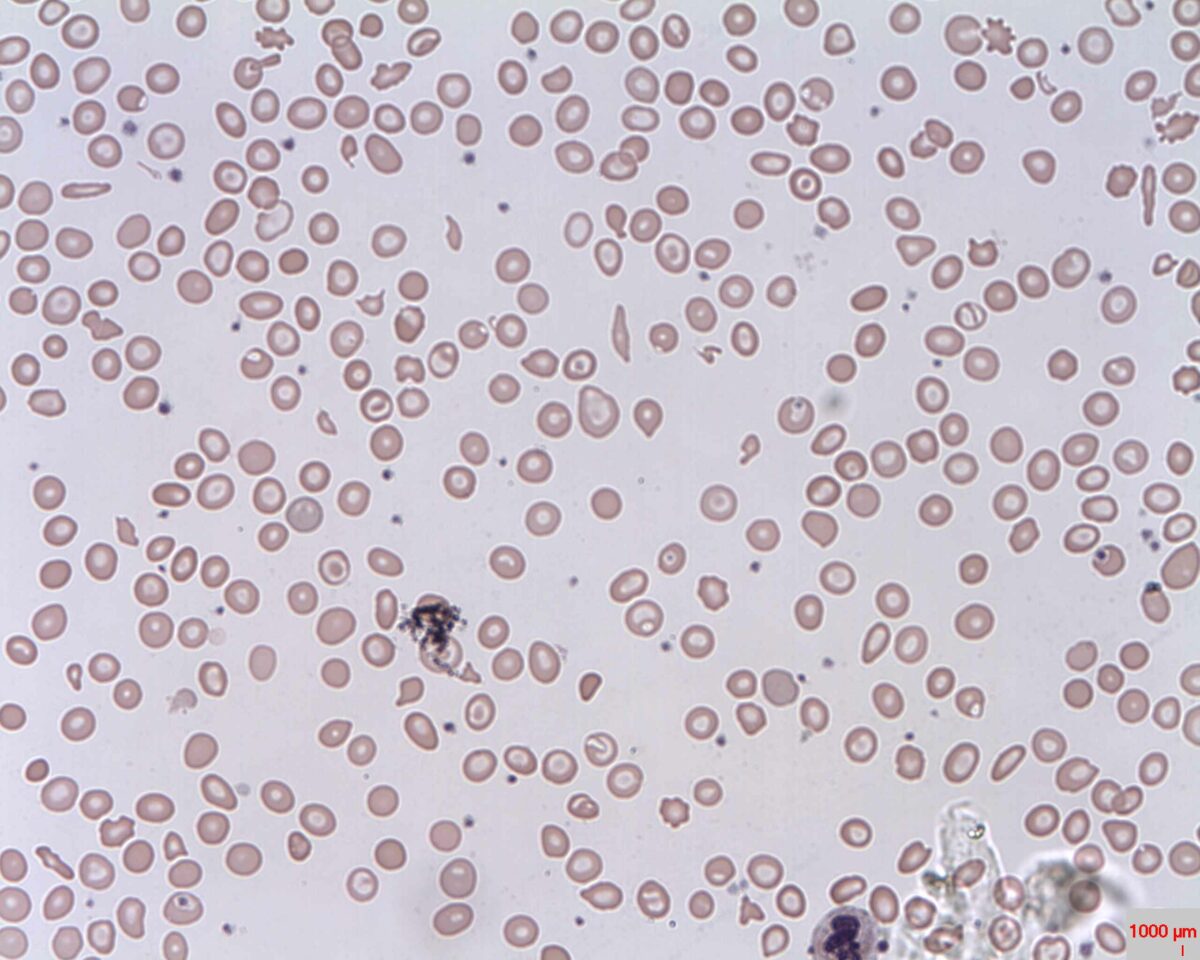
Frotis periférico: anemia microcítica hipocrómica con codocitos (ojo de buey); también se observa anisocitosis (eritrocitos de tamaño desigual)
Imagen: “Target cells (Codocytes, Leptocytes or Mexican hat cells)” por Prof. Osaro Erhabor. Licencia: CC0 1.0El diagnóstico diferencial incluye otras afecciones asociadas a la anemia microcítica o a codocitos.