Los síndromes mielodisplásicos son un grupo de neoplasias clonales con defectos de maduración caracterizados por displasia, citopenia y precursores de médula ósea inmaduros. Pueden ser idiopáticos o secundarios a diversas exposiciones dañinas, como quimioterapia citotóxica, radiación ionizante o toxinas ambientales. La mediana de edad de los pacientes es de 70 años. La presentación incluye síntomas de anemia (fatiga), neutropenia (infección) o trombocitopenia (sangrado). El diagnóstico se basa en la evaluación de la médula ósea, que revela citopenia, displasia en al menos 1 linaje y células blásticas en < 20% de la celularidad de la médula ósea. Se requieren estudios citogenéticos y moleculares para la clasificación, el pronóstico y las decisiones relacionadas con el tratamiento. Existe un mayor riesgo acumulativo de transformación a leucemia mieloide aguda y varía según el subtipo de síndrome mielodisplásico. El tratamiento incluye medidas de soporte, uso de factores de crecimiento hematopoyéticos, terapia inmunosupresora y trasplante alogénico de células hematopoyéticas.
Última actualización: Dic 14, 2024
Los síndromes mielodisplásicos son enfermedades clonales de la médula ósea caracterizadas por la presencia de precursores displásicos, inmaduros de la médula ósea y citopenias periféricas. La Organización Mundial de la Salud (OMS) publicó una actualización en 2022 en la que renombró los síndromes mielodisplásicos como «Neoplasias mielodisplásicas».
La mayoría de los síndromes mielodisplásicos se atribuyen a deleciones y translocaciones cromosómicas o mutaciones genéticas.
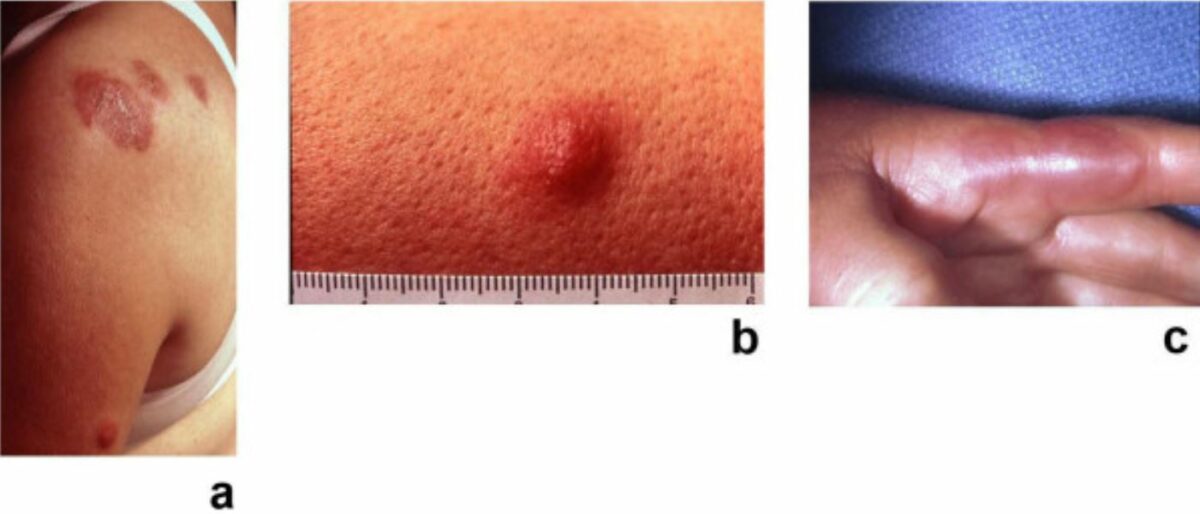
Síndrome de Sweet: placas dolorosas, eritematosas, seudovasculares de dermatosis neutrofílica febril aguda
Imagen: “Sweet’s syndrome–a comprehensive review of an acute febrile neutrophilic dermatosis” por Cohen PR. Licencia: CC BY 2.0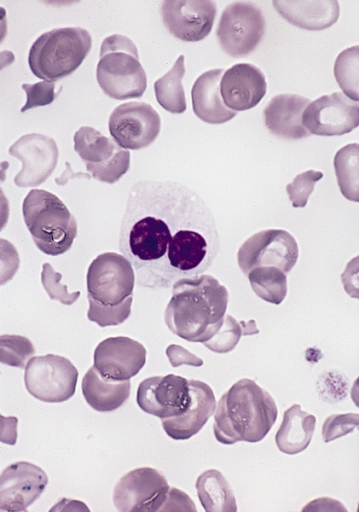
Frotis periférico en síndrome mielodisplásico que muestra un neutrófilo displásico con núcleo bilobulado y granulación alterada (pseudo–anomalía de Pelger-Huët)
Imagen: “Hypogranular neutrophil with a pseudo-Pelger-Huet nucleus in MDS” por The Armed Forces Institute of Pathology (AFIP) Licencia: Dominio Público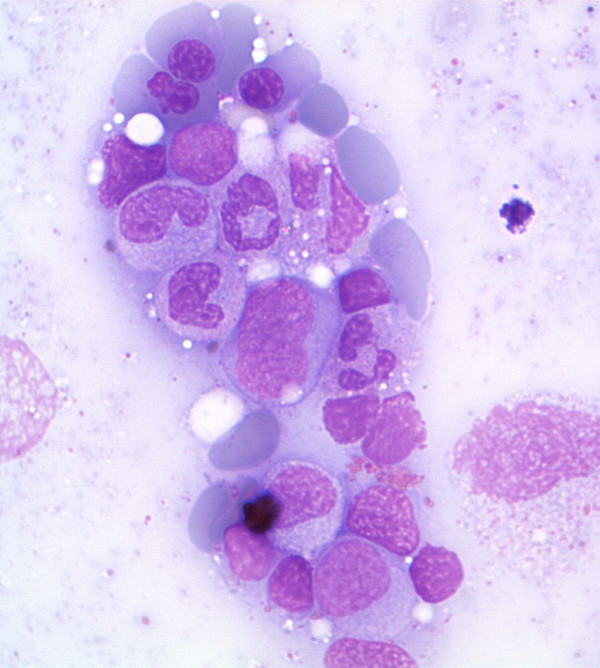
Aspirado de médula ósea en síndrome mielodisplásico que muestra células eritroides displásicas y precursores mieloides
Imagen: “Antiretroviral activity of 5-azacytidine during treatment of a HTLV-1 positive myelodysplastic syndrome with autoimmune manifestations” por Diamantopoulos, P.T. et al. Licencia: CC BY 2.0Después de confirmar el diagnóstico de neoplasia mielodisplásica, los pacientes se clasifican según la quinta edición de la clasificación de tumores hematolinfoides de la Organización Mundial de la Salud (OMS), publicada en 2022.
La clasificación se basa en:
Tipos: