La autoinmunidad es una respuesta inmunitaria patológica hacia los autoantígenos, que resulta de una combinación de factores: inmunológicos, genéticos y ambientales. El sistema inmunitario está equipado con autotolerancia, lo que permite que las células inmunitarias, como las células T y las células B, reconozcan los autoantígenos y no generen una reacción contra ellos. Los defectos en este mecanismo, junto con los desencadenantes ambientales (como las infecciones) y los factores de susceptibilidad genética (los más notables son los genes del antígeno leucocitario humano (HLA)) pueden conducir a enfermedades autoinmunes. Estas condiciones son más comunes en las mujeres. Las enfermedades autoinmunes son crónicas, con manifestaciones clínicas consistentes con la respuesta inmune asociada. Entre estas condiciones se encuentran la enfermedad de Graves (autoanticuerpos contra los receptores de la hormona tiroidea), la miastenia gravis (anticuerpos contra los receptores de la acetilcolina), la diabetes tipo 1 (destrucción de las células β pancreáticas por parte de las células inmunitarias) y el lupus eritematoso sistémico (daño multiorgánico provocado por inmunocomplejos y autoanticuerpos).
Última actualización: Jul 12, 2022
La autoinmunidad es la respuesta inmunitaria patológica a uno mismo, o contra las propias células, que produce inflamación, daño celular o disfunción de tejidos/órganos.
El sistema inmunitario utiliza la activación de los linfocitos para la defensa contra los patógenos, pero al mismo tiempo mantiene la autotolerancia, que es la ausencia de respuesta a los antígenos propios. La tolerancia inmunológica es protectora y tiene diferentes mecanismos (cuya falla es un factor en la autoinmunidad).
La aparición de trastornos autoinmunitarios implica la interacción de diferentes factores (genéticos, ambientales e inmunológicos) que conducen a una respuesta inmunitaria activada, con manifestaciones.
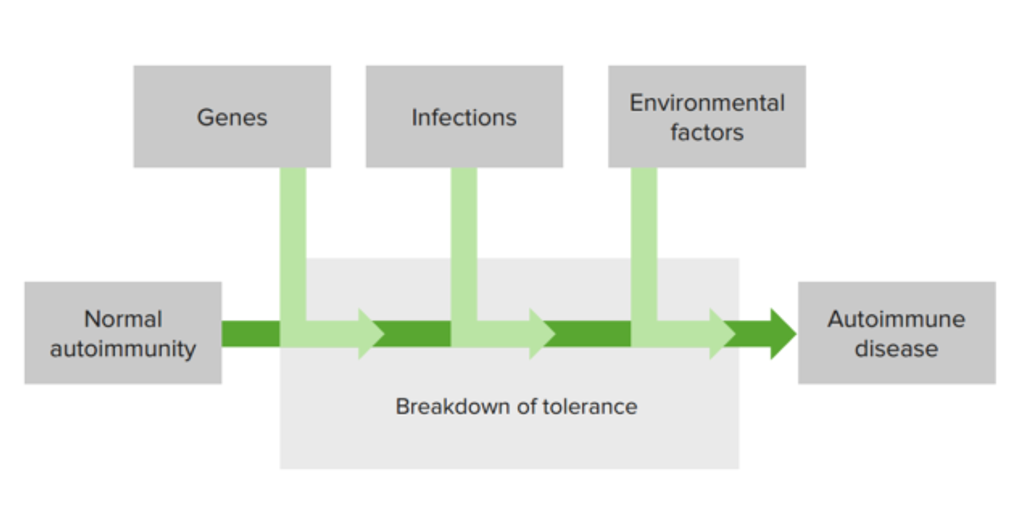
Múltiples factores afectan el desarrollo de la enfermedad autoinmune:
La combinación de factores de susceptibilidad genética, el medioambiente y un defecto en la tolerancia inmunológica conducen a la activación de linfocitos autorreactivos y al desarrollo de trastornos autoinmunitarios.
| Genes | Enfermedad autoinmune asociada |
|---|---|
| CMH/HLA | La mayoría de las enfermedades autoinmunes |
| PTPN22 |
|
| CTLA4 |
|
| IL2RA |
|
| IL2/IL21 |
|
| BLK |
|
Los enfoques utilizados en el tratamiento de enfermedades autoinmunes son: